Irving Kirsch University of Connecticut, Alan Scobria University of Connecticut, Thoma J. Moore George Washington University
Pubblicato su Prevention & Treatment 2002
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
Siamo molto rincuorati dalle risposte ponderate al nostro articolo. A differenza di alcune delle risposte a una precedente meta-analisi degli effetti dei farmaci antidepressivi (Kirsch & Sapirstein, 1998), ora c’è un accordo unanime tra i commentatori che la differenza media tra la risposta ai farmaci antidepressivi e la risposta al placebo inerte è molto piccola. È così piccola che, nonostante le dimensioni del campione che coinvolge centinaia di partecipanti, il 57% degli studi finanziati dall’industria farmaceutica non è riuscito a mostrare una differenza significativa tra farmaco e placebo. La maggior parte di questi dati negativi non sono stati pubblicati (vedi Thase, 2002) e sono stati accessibili solo ottenendo l’accesso ai documenti della Food and Drug Administration (FDA) degli Stati Uniti.
La piccola differenza tra la risposta al farmaco e la risposta al placebo è stata un “piccolo sporco segreto” (Hollon, DeRubeis, Shelton, & Weiss, 2002), noto ai ricercatori che conducono studi clinici, ai revisori della FDA e a un piccolo gruppo di critici che hanno analizzato i dati pubblicati e raggiunto conclusioni simili alle nostre (per esempio, Greenberg & Fisher, 1989). Non era noto al grande pubblico, ai pazienti depressi e nemmeno ai loro medici. 1 Siamo lieti che il nostro sforzo faciliti la diffusione di queste informazioni.
I dati delle aziende farmaceutiche che abbiamo analizzato rivelano una differenza media farmaco/placebo di meno di 2 punti sulla scala della depressione di Hamilton (HAM-D), una differenza che non è clinicamente significativa (vedi Jacobson, Roberts, Berns, & Mcglinchey, 1999). Un altro modo di descrivere questa differenza è in termini di tassi di risposta. Thase (2002), per esempio, nota che il 35% – 50% dei pazienti risponde ai farmaci rispetto al 25% – 30% che risponde al placebo (vedi anche Brown, 2002; Hollon et al., 2002). Questo viene interpretato come indicativo del fatto che il 10% – 20% dei pazienti depressi in studi clinici mostra un vero effetto del farmaco, nel qual caso ne consegue che l’80% – 90% di questi pazienti non lo fa.
Incrementi del tasso di risposta del 10% – 20% sembrano clinicamente importanti per alcuni commentatori (per esempio, Thase, 2002) che li hanno interpretati come indicanti la percentuale di pazienti che mostrano una forte risposta agli antidepressivi ma non sarebbero aiutati dal placebo. Questa interpretazione è errata (Moncrieff, 2002). Per classificare i pazienti come rispondenti o non rispondenti, si deve stabilire un punto di cutoff (per esempio, una diminuzione del 50% dei sintomi depressivi; Mulrow et al., 1999). Consideriamo due pazienti con punteggi HAM-D al basale di 20. Uno è randomizzato alla condizione del farmaco e mostra un miglioramento di 10 punti sull’HAM-D. L’altro è assegnato al gruppo placebo e mostra un miglioramento di 9 punti. Il primo verrebbe classificato come un responder e il secondo come un non responder, ma in realtà, la differenza di risposta (1 punto) è trascurabile.
Ciò che rende questo esempio particolarmente importante è che questi due pazienti sono tipici, piuttosto che eccezioni. Una risposta al farmaco del 50% è la mediana negli studi clinici pubblicati (Mulrow et al., 1999), e la diminuzione di 10 punti è stata la risposta media al farmaco nel set di dati della FDA. Così, la differenza del 10%-20% tra i tassi di risposta al farmaco e al placebo potrebbe essere dovuta interamente a quei pazienti che mostrano una risposta moderatamente forte (appena sopra il criterio) al farmaco e quelli che mostrano una risposta quasi altrettanto forte (appena sotto il criterio) al placebo. Sarebbe ottenuto se non ci fosse nemmeno un paziente con un forte effetto reale del farmaco. 2 Naturalmente, potrebbe anche essere ottenuto se ci fossero alcuni pazienti con un maggiore effetto vero del farmaco e altri su cui il farmaco avesse un effetto negativo o nessun effetto. Questo sarebbe vero se ci fosse una variabile moderatrice nascosta, una possibilità sollevata da alcuni revisori e discussa da noi più avanti.
Abbiamo suggerito due possibili spiegazioni per le piccole differenze tra la risposta al farmaco e la risposta al placebo: O gli effetti del farmaco e del placebo non sono additivi (nel qual caso, gli studi clinici convenzionali sono un mezzo inappropriato per valutare gli effetti del farmaco perché potrebbero portare al rifiuto di farmaci veramente efficaci, i cui benefici sono ampiamente mascherati dal placebo), o l’effetto del farmaco è molto piccolo. I commentatori hanno sollevato tre ulteriori possibilità. Essi suggeriscono che
(a) ci possono essere difetti nei modi in cui le prove sponsorizzate dalle aziende farmaceutiche sono condotte,
(b) le piccole differenze medie tra farmaco e placebo oscurano i forti effetti del farmaco prodotti da alcuni antidepressivi in un sottoinsieme di pazienti depressi, e
(c) gli effetti del farmaco possono essere più stabili di quelli del placebo.
Nella presente risposta ai commenti, consideriamo ciascuna di queste possibilità. Consideriamo anche il suggerimento che l’uso di antidepressivi è giustificato, non importa quanto piccolo sia l’effetto, purché sia statisticamente significativo (Brown, 2002; Moerman, 2002; Salamone, 2002; Thase, 2002).
L’adeguatezza degli studi clinici
I farmaci valutati negli studi clinici che compongono l’insieme di dati della FDA sono stati sponsorizzati dalle aziende che li producono e quindi sono in grado di beneficiare finanziariamente da un risultato positivo. Quindi, se ci fossero dei pregiudizi in questi studi, ci si aspetterebbe che favoriscano il farmaco in esame (Antonuccio, Burns, & Danton, 2002). Infatti, una revisione quantitativa dei fattori che influenzano la risposta agli antidepressivi negli studi clinici ha indicato che la sponsorizzazione di uno studio da parte di una casa farmaceutica tendeva a produrre effetti favorevoli al prodotto dello sponsor (Freemantle, Anderson, & Young, 2000). Alcuni dei commentatori della nostra analisi del set di dati della FDA hanno suggerito che potrebbe essere il contrario. Brown (2002) suggerisce che i ricercatori zelanti gonfiano i punteggi di base in modo che i potenziali partecipanti leggermente depressi non vengano scartati (vedi anche Thase, 2002). Hollon et al. (2002) sostengono che basse dosi possono essere usate per minimizzare gli effetti collaterali.
Hollon et al. (2002) suggeriscono che i produttori di fluoxetina potrebbero aver usato basse dosi nei loro studi clinici, in modo da poter rivendicare bassi livelli di effetti collaterali quando commercializzavano il loro prodotto. Di conseguenza, anche l’effetto terapeutico potrebbe essere stato sottostimato. Questa possibilità è contraddetta dai dati. La fluoxetina è prescritta in dosaggi che vanno da 20 a 60 mg al giorno. I due studi dose-risposta presentati da Eli Lilly alla FDA hanno valutato dosi di fluoxetina di 20, 40 e 60 mg. In uno di questi studi (condotto su pazienti lievemente depressi), non sono state trovate differenze significative tra le dosi o tra qualsiasi dose e il placebo. Nell’altro studio (condotto su pazienti da moderatamente a gravemente depressi), le due dosi inferiori erano significativamente più efficaci della dose alta, che non era significativamente più efficace del placebo. Secondo l’etichetta della confezione della fluoxetina, una dose particolarmente alta (80 mg) è stata usata in altri studi clinici presentati alla FDA.
Variabili moderatrici
È stato suggerito che alcuni pazienti possono essere più reattivi di altri ai farmaci o che alcuni antidepressivi sono più efficaci di altri (Brown, 2002; Hollon et al., 2002; Thase, 2002). Se questo è il caso, allora le differenze farmaco/placebo, collassate tra pazienti e farmaci, potrebbero sottostimare l’effetto che alcuni farmaci hanno su alcuni pazienti.
La nostra analisi ha incluso sei diversi farmaci antidepressivi. Tra i farmaci per i quali sono stati riportati dati completi, la gamma di differenze farmaco/placebo era compresa tra 1 e 3 punti sull’HAM-D. Anche per quei farmaci per i quali i dati sulle prove con risultati negativi sono stati trattenuti, la differenza media più alta era di 3,21 punti. Quindi, se ci sono differenze medie tra questi farmaci, devono essere molto piccole.
Hollon et al. (2002) esprimono la preoccupazione che l’esclusione delle stime per i tre farmaci per i quali non sono stati riportati i punteggi per gli studi non andati a buon fine potrebbe risultare nell’omissione involontaria di “molti dei più potenti farmaci attuali” (10). Fanno specifico riferimento alla venlafaxina come un farmaco che potrebbe “produrre gli effetti più robusti” (10) perché lavora su più sistemi neurotrasmettitoriali. Questa preoccupazione non è ben fondata. In primo luogo, la venlafaxina non era uno dei farmaci che sono stati esclusi nella stima degli effetti tra farmaci.
Secondo, una meta-analisi di 105 studi clinici (Freemantle et al., 2000) indica che i farmaci che lavorano su sistemi neurotrasmettitoriali multipli non sono più efficaci dei farmaci puramente serotoninergici. In terzo luogo, la differenza media ponderata farmaco/placebo per i tre farmaci esclusi era di 2,31 punti HAM-D. Poiché questa è una sovrastima, in cui un terzo degli studi (quelli che mostrano risultati particolarmente scarsi per il farmaco attivo) sono stati esclusi, la differenza reale farmaco/placebo per i farmaci esclusi non può essere significativamente maggiore di quella dei farmaci per i quali sono stati riportati dati completi.
Se i farmaci non producono risposte significativamente diverse, forse ci sono differenze tra i pazienti che mascherano effetti farmacologici più potenti. A sostegno di questa tesi, Hollon et al. (2002) hanno presentato i dati di uno studio non pubblicato sulla paroxetina, in cui i pazienti sono stati abbinati (post hoc) in base all’ordine dei punteggi di cambiamento (cioè, il paziente che mostrava il minor miglioramento nella condizione del farmaco attivo è stato abbinato al paziente che mostrava il minor miglioramento nella condizione del placebo, ecc.) Le differenze farmaco/placebo tra i punteggi di cambiamento dei pazienti abbinati variavano in funzione del rango del punteggio di cambiamento, ma anche tra quelle coppie di partecipanti che mostravano il maggior cambiamento, la differenza media era solo 3,39 punti sulla HAM-D.
Hollon et al. (2002) riportano anche percentuali di coppie di pazienti che mostrano differenze di 4 punti o superiori e differenze di 6 punti o superiori. Essi interpretano l’esistenza di queste differenze come indicazione che alcuni pazienti mostrano un effetto maggiore del farmaco rispetto ad altri. Tuttavia, l’errore di misurazione produce sempre una distribuzione intorno a una media, e i dati di Hollon et al. non forniscono alcuna ragione per sospettare qualsiasi altra spiegazione.
Anche se le vere differenze farmaco/placebo fossero sempre tra 2 e 3 punti, alcune delle differenze osservate sarebbero maggiori e altre minori. Inoltre, c’è un eccezionalmente alto grado di errore nei punteggi valutati da Hollon et al. I punteggi di cambiamento sono notoriamente inaffidabili, anche quando i punteggi pre e post test sono altamente affidabili (Campbell & Kenny, 1999). Le differenze tra i punteggi di cambiamento sono doppiamente inaffidabili. Questa inaffidabilità è evidente nello studio descritto da Hollon et al., in cui il modello delle differenze tra i punteggi di cambiamento del farmaco e del placebo variava sostanzialmente tra i due siti in cui lo studio è stato condotto.
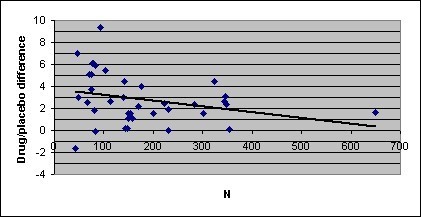
Un metodo per far fronte all’inaffidabilità è quello di esaminare i punteggi medi di grandi gruppi di partecipanti piuttosto che di singoli partecipanti o (come nel caso dei dati di Hollon et al. [2002]) di coppie di partecipanti. Anche con campioni relativamente grandi, le differenze nelle dimensioni del campione producono differenze nell’affidabilità dei dati. La figura 1 mostra le differenze farmaco/placebo nel set di dati FDA in funzione della dimensione del campione.
Queste differenze variano ampiamente nei campioni piccoli, ma sono sostanzialmente più affidabili nei campioni grandi. Inoltre, c’è una tendenza per i campioni grandi a mostrare differenze farmaco/placebo più piccole. Come si vede nella Figura 1, una differenza media di circa 2 punti sull’HAM-D caratterizza le differenze farmaco/placebo negli studi più grandi (e quindi più affidabili).
L’ipotetico moderatore proposto più frequentemente è la gravità al basale. L’ipotesi è che i pazienti più gravemente depressi mostrano una maggiore risposta al farmaco e una minore risposta al placebo. Nella serie di dati della FDA, c’era solo uno studio condotto su pazienti lievemente depressi. Tre studi sono stati condotti su pazienti ricoverati gravemente depressi, ma i dati di due di questi studi non sono stati riportati perché non sono state trovate differenze significative farmaco/placebo. La maggior parte degli studi è stata condotta su pazienti giudicati da moderatamente a gravemente depressi, ed è con questi pazienti che la differenza farmaco/placebo è stata di circa 2 punti sull’HAM-D. Quindi, la differenza farmaco/placebo sembra essere trascurabile per la maggior parte dei pazienti a cui vengono prescritti antidepressivi.
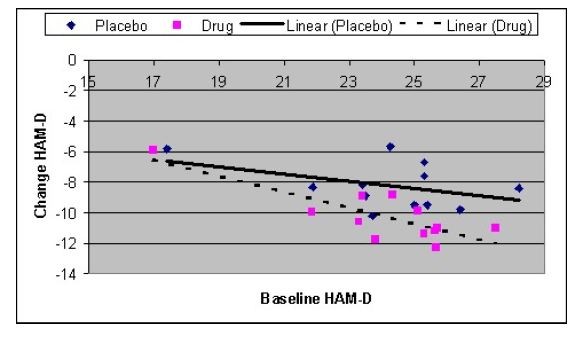
La figura 2 mostra la relazione tra i punteggi al basale e il miglioramento negli studi clinici più grandi (N= 200 o più), e quindi più affidabili, descritti nel set di dati della FDA. I pazienti più gravemente depressi hanno mostrato un miglioramento maggiore, ma questo è vero sia per i pazienti trattati con placebo che per quelli trattati con farmaci. Ciò è dovuto alla regressione verso la media (Campbell & Kenny, 1999), che quasi sempre produce una correlazione tra i punteggi di base e i punteggi di cambiamento. 3
La pendenza della linea di regressione appare più ripida per il farmaco che per il placebo, suggerendo una maggiore differenza farmaco/placebo tra i pazienti più gravemente depressi, ma un’analisi di regressione indica che questa differenza non è statisticamente significativa (p> .20). Tuttavia, poiché i test delle differenze di pendenza hanno una potenza molto bassa, non si può escludere una maggiore differenza farmaco/placebo tra i pazienti più gravemente depressi.
Pertanto, abbiamo calcolato le differenze farmaco/placebo osservate nei sei grandi studi con i punteggi di depressione di base più bassi (range = 17,21 – 24,25) e le abbiamo confrontate con le differenze osservate nei sei grandi studi con i punteggi di depressione di base più alti (range = 25,15 – 27,85). Le differenze medie farmaco/placebo erano di 1,46 punti negli studi con punteggi di base più bassi e 2,56 negli studi con punteggi di base più alti. Inoltre, è probabile che questa sia una sovrastima della differenza farmaco/placebo per i pazienti più gravemente depressi perché non include i dati non riportati di due studi condotti su pazienti ospedalizzati gravemente depressi, nessuno dei quali ha mostrato una differenza significativa tra farmaco e placebo. La linea di fondo è che anche negli studi con pazienti più gravemente depressi, c’è una forte risposta del placebo e una differenza relativamente piccola tra farmaco e placebo.
Infine, è possibile che pazienti diversi rispondano a farmaci diversi (Hollon et al., 2002). Anche se ci sono pochi dati sperimentali a sostegno di questa ipotesi, i medici riferiscono che i pazienti che non rispondono a un particolare antidepressivo a volte rispondono quando viene dato un farmaco diverso. I risultati di un primo studio sulla prevenzione della nausea sono pertinenti a questo problema (Wolf, Doering, Clark, & Hagans, 1957). Ai pazienti furono somministrati successivamente sette diversi trattamenti per la nausea, dopo i quali fu somministrato Ipecacuana? La risposta è stata definita come il blocco degli effetti emetici dell’ Ipecacuana.
C’era una sostanziale variabilità nei tassi di risposta. Alcuni partecipanti hanno risposto a tutti i trattamenti, altri a nessuno. La maggior parte ha risposto ad alcuni trattamenti ma non ad altri. Così, il modello di risposta era simile a quello osservato clinicamente, dopo la somministrazione di antidepressivi: I pazienti che non rispondevano a un dato farmaco spesso rispondevano a un altro. Nello studio di Wolf et al. (1957), tuttavia, tutti e sette i trattamenti erano noti per essere inefficaci per la condizione da trattare. Erano placebo. Questi dati dimostrano che la risposta al placebo è incoerente. Quindi, trovare che i pazienti a volte rispondono dopo il passaggio a un antidepressivo diverso è esattamente ciò che ci si aspetterebbe se gli antidepressivi non fossero altro che placebo attivi.
Lo studio più ampio dell’ipotesi che pazienti diversi rispondono a farmaci diversi è la meta-analisi di Freemantle et al. (2000). Hanno esaminato 105 studi clinici in cui gli inibitori dell’assorbimento della serotonina (SSRI) sono stati confrontati con altri tipi di antidepressivi e hanno usato l’analisi di regressione per trovare i predittori del risultato differenziale. I predittori ipotizzati includevano l’azione farmacologica (inibizione della ricaptazione della noradrenalina, inibizione della ricaptazione della serotonina e antagonismo del recettore 5-HT2, doppia azione e tripla azione), impostazione del trattamento (ricovero vs. ambulatorio), dose del farmaco di confronto, metodo di analisi (LOCF vs. dati completi), età del paziente, scala di misurazione (HAM-D vs. qualsiasi altro) e sponsor dello studio. Solo uno di questi fattori ha rasentato la significatività: C’era “una tendenza verso una maggiore efficacia del farmaco dello sponsor” (Freemantle et al., 2000, p. 294).
Freemantle et al. (2000) non hanno usato alcuni dei fattori che i commentatori hanno citato come potenziali predittori di risultati differenziali, e non si può mai escludere la possibilità di variabili moderatrici non rilevate. Ma se ci sono moderatori nascosti, la differenza media complessiva tra farmaco e placebo (2 punti sull’HAM-D) limita le conclusioni che possono essere tratte da essi. Se la differenza media farmaco/placebo è maggiore di 2 punti per un sottoinsieme di farmaci o pazienti, allora deve essere inferiore a 2 punti per gli altri. Per esempio, se la differenza media tra farmaco e placebo è di 4 punti per la metà dei pazienti (che è ancora un effetto del farmaco piuttosto piccolo), allora l’effetto medio degli antidepressivi sugli altri pazienti deve essere 0, e se è più di 4 punti per la metà dei pazienti, allora i farmaci devono causare danni ad almeno alcuni altri che starebbero meglio con il placebo.
La risposta del farmaco è più stabile di quella del placebo?
La nostra analisi era limitata agli studi di efficacia acuta presentati alla FDA. È possibile che le differenze farmaco/placebo a breve termine siano trascurabili, ma che gli effetti del farmaco siano più stabili di quelli del placebo, con conseguenti tassi di ricaduta inferiori (Brown, 2002; Hollon et al., 2002; Thase, 2002), proprio come gli effetti della psicoterapia sembrano essere più stabili di quelli dei farmaci (Hollon, Shelton, & Loosen, 1991). Prima di esaminare i dati, tuttavia, è necessario considerare due questioni: il modo in cui l’esito è descritto e il disegno degli studi a lungo termine.
Ci sono due modi in cui l’esito a lungo termine può essere descritto. Uno è in termini di ricaduta dopo il miglioramento iniziale; l’altro è in termini di risposta continua al trattamento. Thase (1999), per esempio, ha riportato tassi di ricaduta a 12 mesi del 20% con venlafaxina e 34% con placebo in un’analisi collettiva di quattro studi clinici. Quindi, c’erano 1,5 volte più ricadute con il placebo che con il farmaco. Descritti in termini di efficacia continuata, tuttavia, questi stessi dati indicano che, dopo 12 mesi, l’80% dei pazienti che ricevono farmaci è rimasto in remissione, rispetto al 66% dei pazienti con placebo. Quindi, l’83% dell’effetto dei farmaci è stato duplicato dal placebo. 4 Il fatto che questo effetto sia simile a quello visto negli studi a breve termine esclude la possibilità che gli effetti dei farmaci antidepressivi possano essere sostanzialmente maggiori in un periodo di trattamento più lungo.
Una seconda questione che deve essere considerata nella comprensione dei risultati degli studi a lungo termine è il disegno dello studio. Ci sono due disegni sperimentali che sono stati utilizzati. Il disegno più comune è lo studio di prevenzione delle ricadute, in cui i pazienti che hanno risposto ai farmaci sono poi randomizzati per continuare con i farmaci o passare al placebo. Un metodo meno comune per valutare la risposta a lungo termine è quello degli studi di continuazione o di estensione, in cui i pazienti che hanno risposto al farmaco o al placebo durante uno studio di efficacia acuta continuano il trattamento a cui erano stati originariamente assegnati.
Il disegno della prevenzione delle ricadute è particolarmente sfavorevole alla ricerca di effetti placebo. In primo luogo, gli studi clinici da cui i pazienti sono tratti iniziano tipicamente con periodi di washout con placebo, in cui tutti i pazienti che rispondono al placebo vengono eliminati dallo studio. Quindi, la partecipazione allo studio di prevenzione delle ricadute è limitata ai pazienti che non solo hanno risposto al farmaco attivo, ma non hanno nemmeno risposto al placebo. In secondo luogo, questo disegno può esacerbare il problema della rottura del cieco sulla base degli effetti collaterali percepiti. Sembra probabile che una persona che ha assunto un farmaco attivo e poi è passata al placebo sarà in grado di rilevare il cambiamento.
Nonostante questo bias, gli studi di prevenzione delle ricadute spesso mostrano grandi risposte al placebo. Per esempio, uno dei due studi di prevenzione delle ricadute di 24 settimane riportati alla FDA dal produttore del citalopram ha mostrato tassi di risposta a 2 anni del 69% per il placebo e del 90% per il citalopram. L’altro ha mostrato tassi di risposta del 76% per il placebo e dell’86% per il citalopram. Così, in questi studi, la risposta a lungo termine del placebo tra i pazienti che erano stati trattati con successo con un antidrepressivo attivo era tra il 77% e l’88% della risposta del farmaco.
Risultati simili sono stati riportati da Walach e Maidhof (1999) in una meta-analisi di studi di prevenzione delle ricadute pubblicati tra il 1973 e il 1990. In questi studi, il 71% della risposta al farmaco è stata duplicata dal placebo. Walach e Maidhof hanno anche esaminato la risposta al trattamento in funzione della durata dello studio. I loro dati indicano che le risposte sia al farmaco che al placebo diminuiscono nel tempo. Contrariamente alla saggezza convenzionale, tuttavia, la correlazione tra la durata dello studio e la risposta al trattamento era più alta per i farmaci attivi ( r= -.84) che per il placebo ( r= -.62), suggerendo un declino più ripido dell’efficacia per i farmaci attivi che per il placebo.
Gli studi di continuazione sono relativamente rari, ma i dati confermano la relativa stabilità della risposta al placebo nel tempo. Come notano Antonuccio et al. (2002), il follow-up di 18 mesi del NIMH Collaborative Depression Study (Shea et al., 1992) ha riportato risultati a lungo termine equivalenti sia per il farmaco che per il placebo, con un tasso di ricaduta più basso tra i pazienti che hanno rimesso nel gruppo placebo. Uno studio più recente ha confrontato l’iperico, la sertralina e il placebo (Hypericum Depression Trial Study Group, 2002) e ha riportato dati di continuazione a 26 settimane per pazienti che avevano risposto al trattamento durante lo studio clinico di 8 settimane. Dei 79 pazienti che sono entrati nella fase di continuazione, nessuno dei pazienti con placebo ha avuto una ricaduta, nessuno dei pazienti con setralina ha avuto una ricaduta, e solo uno che assumeva iperico ha avuto una ricaduta.
Cosa facciamo ora?
Come molti commentatori hanno notato, i risultati di base della nostra analisi sono chiari e indiscussi. La differenza media tra la risposta ai farmaci antidepressivi e la risposta al placebo è molto piccola. Questo solleva la questione di cosa dovrebbe essere fatto nella pratica clinica. La risposta sia al farmaco che al placebo è sostanziale. Come si può ottenere questo beneficio terapeutico se questi farmaci, che possono essere poco più che placebo attivi, vengono abbandonati? Alcuni commentatori hanno sostenuto che dovrebbero essere dati ai pazienti depressi, anche se il loro effetto farmacologico è trascurabile. Se non altro, possono essere il veicolo attraverso il quale viene suscitata la risposta placebo (Hollon et al., 2002; Moerman, 2002).
Questo argomento si basa sul presupposto che un effetto farmacologico genuino sia stato provato. I vestiti nuovi dell’imperatore possono non essere l’abito elegante che i suoi soggetti erano portati ad aspettarsi, ma almeno sono fatti con tessuto vero (Thase, 2002). Non abbiamo negato che i farmaci antidepressivi possano avere effetti farmacologici genuini. Infatti, abbiamo sollevato la possibilità che i suoi effetti potrebbero essere molto più grandi e affidabili di quanto i dati suggeriscano. Il problema è che gli effetti dei farmaci antidepressivi sono sconosciuti. Potrebbero essere molto grandi, irrisori, o completamente inesistenti. L’imperatore potrebbe indossare un elegante abito invisibile, una foglia di fico, o niente del tutto.
È vero che, in media, c’è una risposta significativamente maggiore ai farmaci che al placebo. Quello che non si sa ancora è la ragione di questa differenza di risposta. Può essere un effetto del farmaco, ma può anche essere un effetto placebo rafforzato associato alla percezione degli effetti collaterali e alla rottura del cieco (Greenberg, 2002; Greenberg & Fisher, 1989). 5 È noto che gli antidepressivi producono significativamente più effetti collaterali di quelli osservati nei gruppi di controllo placebo inerti (Mulrow et al., 1999), i pazienti assegnati ad antidepressivi convenzionali sono in grado di rompere il cieco in misura significativa (Rabkin et al., 1986), e un effetto farmaco non è stato dimostrato in modo convincente negli studi che utilizzano placebo attivi (Moncrieff, Wessely,& Hardy, 2001), nonostante il fatto che i farmaci usati come placebo attivi potrebbero non impedire ai pazienti di diventare ciechi (Hollon et al., 2002). Questi dati non provano che la differenza farmaco/placebo sia dovuta alla rottura del cieco, ma suggeriscono questa come una possibilità ragionevole, che deve essere esclusa prima che l’affermazione di un’efficacia anche minima del farmaco possa essere considerata provata (Greenberg, 2002).
Inoltre, l’ipotesi di additività deve essere testata direttamente. I dati indiretti sono misti. Come nota Brown (2002), i dati che mostrano diversi cambiamenti cerebrali in coloro che rispondono al placebo e ai farmaci (Leuchter, Cook, Witte, Morgan, & Abrams, 2002) suggeriscono che gli effetti potrebbero non essere additivi. Al contrario, i dati che mostrano cambiamenti cerebrali simili nei rispondenti al placebo e ai farmaci (Mayberg et al., 1999) suggeriscono un meccanismo comune, che è coerente con l’ipotesi di additività. L’additività è anche suggerita dagli aumenti paralleli dei tassi di risposta per SSRI e placebo nel corso degli anni (Walsh, Seidman, Sysko, & Gould, 2002). Poiché la composizione del farmaco non è cambiata, il cambiamento deve essere dovuto ad altri fattori. Sospettiamo che sia dovuto alla diffusione di informazioni (o disinformazione) sul meraviglioso successo dei nuovi antidepressivi.
Abbiamo sollevato la possibilità di usare il disegno del placebo bilanciato, forse con placebo attivi come aiuto per preservare la manipolazione, come il test più diretto dell’ipotesi di additività. Hollon et al. (2002) hanno sollevato alcune utili preoccupazioni sul successo dell’uso di placebo attivi a questo scopo. Salamone (2002) ha fornito suggerimenti che potrebbero affrontare alcune di queste preoccupazioni, e Antonuccio et al. (2002) hanno suggerito un’alternativa (valutare il grado di rottura del cieco) che dovrebbe essere implementata di routine nella ricerca farmacologica, ma che non ovvia alla necessità di test diretti dell’ipotesi di additività.
Ci sono anche altre domande che hanno bisogno di una risposta. Abbiamo bisogno di sapere di più sull’effetto placebo e sui suoi meccanismi sottostanti. Rehm (2002) ha fornito molti suggerimenti di ricerca perspicaci che mirano ad affrontare questo problema, e noi speriamo che i ricercatori clinici li implementino. Pensiamo anche che i suggerimenti di Salamone (2002) per nuovi studi sulla relazione dose-risposta siano utili. I dati inviati alla FDA dalle case farmaceutiche includevano studi in cui sono state valutate fino a quattro diverse dosi, e tranne la scoperta che dosi più basse di fluoxetina erano più efficaci di una dose alta, non sono riusciti a trovare differenze lineari o quadratiche affidabili tra le dosi. È possibile, come suggerisce Salamone (2002), che studi che coinvolgono sei o sette dosi diverse rivelino relazioni più complesse. Inoltre, c’è bisogno di ulteriori test di possibili variabili moderatrici (cronicità, secrezione di cortisolo, ecc.).
Nel frattempo, quali sono le alternative per il trattamento dei pazienti? Immaginate di dover scegliere tra quattro trattamenti. Il trattamento A produce una grande risposta terapeutica ma anche un gran numero di effetti avversi, tra cui diarrea, nausea, anoressia, sudorazione, dimenticanza, sanguinamento, convulsioni, ansia, mania, interruzione del sonno e disfunzioni sessuali. I trattamenti B e C producono risposte terapeutiche quasi uguali a quelle prodotte dal trattamento A, ma senza gli effetti collaterali. Infatti, gli effetti collaterali prodotti dal trattamento B sono benefici (ad esempio, una migliore salute fisica generale). Tuttavia, gli effetti terapeutici dei trattamenti B e C sono stati valutati in relativamente pochi studi. Il trattamento D è stato valutato in molti studi comparativi, in cui è stato trovato efficace quanto il trattamento A nel breve termine e più efficace nel lungo termine. Non produce effetti avversi. Dovendo scegliere tra queste alternative, quale scegliereste?
Naturalmente, queste alternative non sono solo ipotetiche. Il trattamento A corrisponde agli SSRI, e l’elenco degli effetti collaterali è tratto da quelli che è stato dimostrato essere prodotti da questi farmaci (Antonuccio, Danton, DeNelsky, Greenberg, & Gordon, 1999; Mulrow et al., 1999). Il trattamento B è l’esercizio fisico, che è stato segnalato per avere benefici terapeutici duraturi nel trattamento della depressione maggiore (Babyak et al., 2000). Potrebbe non essere altro che un placebo, ma se è così, è uno con effetti collaterali desiderabili piuttosto che avversi.
Il trattamento C è la biblioterapia (per esempio, Burns, 1999), un altro trattamento a basso costo con efficacia dimostrata (Jamison & Scogin, 1995; Smith, Floyd, Jamison, & Scogin, 1997) e poco pericolo di effetti collaterali. Il trattamento D è la psicoterapia. Come notato da Antonuccio et al. (2002), “la psicoterapia (in particolare la terapia cognitiva, l’attivazione comportamentale e la terapia interpersonale) si confronta favorevolmente con i farmaci nel breve termine, anche quando la depressione è grave (ad esempio, DeRubeis, Gelfand, Tang, & Simons, 1999), e appare superiore ai farmaci in studi comparativi a lungo termine (Antonuccio et al. 1995; Hollon, Shelton, & Loosen, 1991)” (http://journals.apa.org/prevention/volume5/pre525c.html#p24¶ 24).
Dati questi dati, i farmaci antidepressivi potrebbero essere considerati l’ultima risorsa, limitata ai pazienti che rifiutano o non rispondono ad altri trattamenti.
Può essere che gli effetti della psicoterapia siano dovuti all’aspettativa, al condizionamento e ad altri fattori psicologici che sono stati ipotizzati come base dell’effetto placebo (Kirsch, 1997). Infatti, cambiare le aspettative disadattive è una pietra miliare essenziale della terapia cognitiva. Ma questo non nega la sua efficacia. L’affermazione (per esempio, Salamone, 2002; Thase, 2002) che la logica della valutazione controllata con placebo dovrebbe essere estesa alla psicoterapia è errata (Kirsch, 1978).
Nella ricerca sui farmaci, i placebo sono usati per distinguere gli effetti prodotti farmacologicamente dalla somministrazione della sostanza dai suoi effetti prodotti psicologicamente. Tuttavia, non ci sono effetti prodotti farmacologicamente della psicoterapia. Gli effetti di un intervento psicologico possono essere dovuti solo a fattori psicologici. Le condizioni di controllo che consistono in trattamenti psicologici alternativi (compresi quelli erroneamente chiamati placebo) sono utili per stabilire quali fattori psicologici sono importanti nel produrre gli effetti di una particolare terapia, ma non per valutare l’efficacia di quel trattamento. Come i placebo, le psicoterapie efficaci possono ottenere i loro effetti cambiando le aspettative (Kirsch, 1985, 1990, 1999), ma a differenza dei placebo, lo fanno senza inganno.
1 Un memorandum interno del Direttore della Divisione dei Prodotti Farmaceutici Neurofarmacologici indica la consapevolezza della FDA di questa situazione: La sottosezione “Clinical Efficacy Trials” all’interno della sezione “Clinical Pharmacology” non solo descrive gli studi clinici che forniscono prove degli effetti antidepressivi del citalopram, ma fa menzione di studi clinici adeguati e ben controllati che non sono riusciti a farlo. Sono consapevole, sulla base di precedenti discussioni sulla questione, che il direttore dell’ufficio è incline a ritenere che la fornitura di tali informazioni non abbia alcun valore pratico né per il paziente né per il prescrittore. Non sono d’accordo. Credo che sia utile per il prescrittore, il paziente e il terzo pagatore sapere, senza dover accedere ai documenti ufficiali di revisione della FDA, che gli effetti antidepressivi del citalopram (sic) non sono stati rilevati in ogni studio clinico controllato destinato a dimostrare tali effetti. Sono consapevole che gli studi clinici spesso non riescono a documentare l’efficacia di farmaci efficaci, ma dubito che il pubblico, o anche la maggioranza della comunità medica, sia consapevole di questo fatto. Sono convinto che non solo hanno il diritto di sapere, ma che dovrebbero sapere. Inoltre, credo che l’etichettatura che descrive selettivamente gli studi positivi ed esclude la menzione di quelli negativi possa essere vista come potenzialmente “falsa e fuorviante” (Leber, 1998, p. 11). Siamo d’accordo che il pubblico e la comunità medica dovrebbero essere informati di questi dati.
2 L’effetto del farmaco è convenzionalmente interpretato come la differenza tra la risposta al farmaco e la risposta al placebo. È quella parte della risposta al farmaco che è dovuta all’azione farmacologica del farmaco. Al contrario, la risposta al farmaco include l’effetto del farmaco, l’effetto placebo, la remissione spontanea, la regressione alla media, e qualsiasi altro fattore che potrebbe contribuire ai cambiamenti osservati dopo la somministrazione del farmaco. Allo stesso modo, l’effetto placebo è quella parte della risposta placebo che è effettivamente dovuta alla somministrazione di un placebo.
3 Gli artefatti di regressione influenzano anche la correlazione tra la risposta al farmaco e la risposta al placebo. Moerman ha esaminato le meta-analisi precedenti mostrando che queste correlazioni variano tra .43 e .90. Allo stesso modo, se l’analisi è limitata agli studi clinici più affidabili nel set di dati FDA – quelli con campioni di 200 o più – la correlazione tra la risposta al farmaco e la risposta al placebo nel set di dati FDA è .72. Tuttavia, poiché i punteggi di base sono necessariamente correlati ai punteggi di cambiamento (Campbell & Kenny, 1999), quando i punteggi di base di due gruppi sono correlati (come lo sono nelle meta-analisi delle risposte al farmaco e al placebo), anche i punteggi di cambiamento saranno correlati. Per esempio, quando i punteggi di base normalmente distribuiti in due campioni sono perfettamente correlati tra loro, e i punteggi post test normalmente distribuiti in questi campioni non sono correlati né tra loro né con i punteggi della linea di base, la correlazione tra le due serie di punteggi di cambiamento sarà .50.
4 Il modo in cui questo metodo di descrivere i dati può essere fuorviante può essere illustrato applicandolo all’analisi di Khan, Warner e Brown (2000) dei dati presentati alla FDA. Questi dati indicano che c’erano il doppio dei tentativi di suicidio tra i pazienti a cui è stato dato un farmaco attivo rispetto a quelli a cui è stato dato un placebo. Questo potrebbe essere interpretato come un’indicazione che i farmaci raddoppiano il rischio di tentativi di suicidio, ma questo metodo di descrivere i dati è fuorviante. I tassi effettivi erano 0,8% con farmaci antidepressivi e 0,4% con placebo. Così, i tentativi di suicidio erano assenti nel 99,2% dei pazienti trattati con farmaci e 99,6% dei pazienti trattati con placebo, e come notato da Khan et al. (2000), la differenza non era statisticamente significativa.
5 Contrariamente all’implicazione nel commento di Muñoz (2002), questa ipotesi non suggerisce doppiezza da parte dei pazienti o dei ricercatori.
La corrispondenza relativa a questo articolo deve essere indirizzata a Irving Kirsch, Dipartimento di Psicologia, Università del Connecticut 406 Babbidge Road, U-20, Storrs, CT 06269-1020
E-mail: irving.kirsch@uconn.edu
Bibliografia: vedi articolo originale