D. Healya,∗, J. Le Nourya and D. Manginb
Pubblicato su International Journal of Risk & Safety in Medicine 2016
traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
aNorth Wales Department of Psychological Medicine, Bangor University, Wales, UK
bDavid Braley Nancy Gordon Chair in Family Medicine, Department of Family Medicine, McMaster University, Hamilton, ON, Canada
OBIETTIVO: indagare i possibili collegamenti tra ritardo dello sviluppo neurologico e disturbi dello spettro dello sviluppo neurologico e l’esposizione a farmaci con effetti sull’inibizione della ricaptazione della serotonina durante la gravidanza.
METODI: Abbiamo rivisto sistematicamente la letteratura epidemiologica per gli studi relativi a questa relazione nei bambini nati con disturbo dello spettro dello sviluppo neurologico e condizioni correlate, nonché studi sugli animali che somministravano inibitori della ricaptazione della serotonina ad animali gravidi e inoltre abbiamo rivisto la letteratura per proposte sui possibili meccanismi che potrebbe collegare gli effetti sulla ricaptazione della serotonina con i cambiamenti cognitivi post-partum. Gli studi epidemiologici sono stati analizzati per produrre Forest plot per illustrare le possibili relazioni.
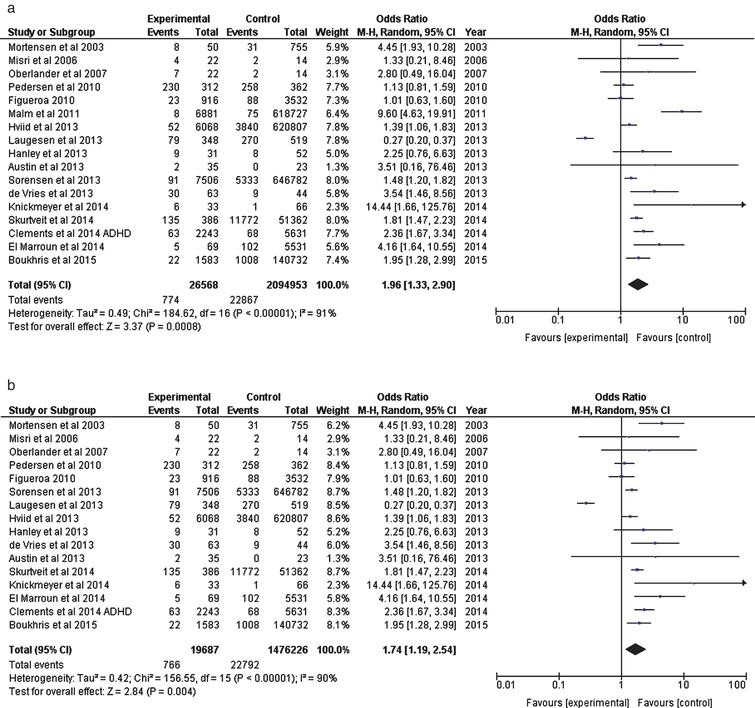
Risultati. L’odds ratio dello spettro autistico o dei disturbi correlati nei bambini nati da donne che assumevano antidepressivi inibitori della ricaptazione della serotonina durante la gravidanza negli studi caso controllo era 1,95 (IC 95% 1,63, 2,34) e negli studi di coorte prospettici era 1,96 (IC 95% 1,33, 2,90).
CONCLUSIONI: Sembra esserci un legame tra l’inibizione della ricaptazione della serotonina in gravidanza e ritardo dello sviluppo e disturbi dello spettro nell’infanzia che portano a difficoltà cognitive nell’infanzia. Occorre lavorare di più per stabilire con maggiore precisione la natura delle difficoltà ei possibili meccanismi attraverso i quali questo collegamento potrebbe essere mediato.
1. Sfondo
La sindrome clinica in seguito chiamata autismo fu segnalata per la prima volta nel 1943 [ 1 ]. I primi studi sulla prevalenza dell’autismo o del disturbo autistico (AD) negli anni ’60 indicavano un tasso di 4 su 10.000 [ 2, 3 ]. Studi successivi hanno indicato l’esistenza di uno spettro di disturbi e hanno introdotto il termine disturbo dello spettro autistico (ASD) a metà degli anni ’90 [ 4 ]. La diagnosi di ASD si è probabilmente ampliata da allora, e ora l’ASD include anche altre sindromi come il Disturbo Pervasivo dello Sviluppo e il Disturbo di Aspergers, quindi è difficile sapere quanto l’uso clinico attuale di una diagnosi di ASD sia mappato su AD e ASD come inizialmente concepito. Le stime attuali indicano che l’ASD negli studi di ricerca si verifica a un tasso di oltre 1 bambino su 70 [ 5, 6].
L’autismo di Kanner è stato riconosciuto prima dell’emergere dei moderni farmaci psicotropi e, data la sua sommersione nell’ASD, potrebbe non essere ora possibile stabilire se sia collegato ai farmaci psicotropi comunemente usati. Dal 1970 sono stati descritti numerosi quadri clinici legati all’uso di droghe psicotrope, alla sindrome anticonvulsivante fetale (FACS), alla sindrome da valproato fetale (FVS), alla sindrome alcolica fetale (FAS) e al disturbo dello spettro alcolico fetale (FASD) sono stati descritti a partire dal 1970. A parte il legame con il trattamento, le caratteristiche cliniche di questi disturbi sono coerenti con una diagnosi di ASD ma non di autismo di Kanner. Un numero crescente di studi epidemiologici indica un aumento dei tassi di ASD. Ciò si traduce comunemente in preoccupazioni per un cambiamento nella prevalenza dell'”autismo”.[7 ],
Non è chiaro se l’incidenza dell’autismo di Kanner sia cambiata. Non è inoltre chiaro se la rete dei nuovi strumenti attraversi i casi di FASD, FACS o FVS non riconosciuti come tali e dove possano stare in queste coorti i bambini affetti da assunzione materna gestazionale di SSRI.
L’ASD non è un’entità patologica tradizionale. In questo contesto sembra prudente ampliare la portata di qualsiasi indagine per guardare non solo all’ASD ma anche al ritardo dello sviluppo neurologico e forse ai disturbi dello spettro dello sviluppo neurologico.
Sembra inoltre opportuno allargare l’indagine a tutti i domini che potrebbero far luce su qualsiasi valutazione della probabilità di una vera associazione: studi epidemiologici sull’uomo, studi sugli animali e prove a sostegno della plausibilità biologica di un collegamento. Una combinazione di questi domini è importante quando l’associazione ha serie implicazioni.
1.1 Plausibilità biologica
Per quanto riguarda un legame tra uso di antidepressivi e problemi di sviluppo neurologico, la serotonina è in particolare il più primitivo dei neurotrasmettitori; ha un ruolo nella riproduzione precoce e, di conseguenza, è stato a lungo riconosciuto che agire sulla serotonina durante il periodo gestazionale ha il potenziale per causare problemi significativi [ 8, 9 ].
Nel 1960, legato a studi sugli effetti degli antidepressivi sulla serotonina, Ashcroft suggerì che ci potesse essere un abbassamento della serotonina nella depressione [ 10 ]. Nel 1970, Ashcroft e altri avevano scartato questo legame [ 11 ].
Al contrario, nel 1961, fu pubblicato un primo rapporto sui livelli elevati di serotonina nell’autismo [ 12 ]. Questo risultato è stato costantemente replicato [ 13-15 ].
All’inizio degli anni ’60, è stato fatto un primo collegamento tra serotonina e difetti alla nascita negli studi sugli animali [ 16-18 ]. All’inizio degli anni ’70 apparvero i primi rapporti che collegavano gli antidepressivi inibitori della ricaptazione della serotonina ai difetti alla nascita [ 19 ]. Nel 1990 è stato pubblicato il primo studio indipendente che collegava l’assunzione di SSRI al potenziale teratogeno negli studi sugli animali [ 20 ].
A partire dagli anni ’80, in seguito alle descrizioni della sindrome fetale anticonvulsivante (FACS) e della sindrome fetale da valproato (FVS), caratterizzate da notevoli deficit nella comunicazione sociale e altre caratteristiche ASD [ 21, 22 ], è emerso un consenso sul fatto che i farmaci psicotropi potrebbero produrre effetti teratologici comportamentali anche se non mostravano chiare anomalie anatomiche come anomalie cardiache o del tubo neurale dopo l’uso durante la gravidanza [ 23 ].
Questi sviluppi hanno portato le aziende produttrici di nuovi farmaci ad azione centrale negli anni ’80, inclusi gli SSRI, a intraprendere studi sugli animali. Nel caso degli SSRI, gli studi sugli animali hanno esaminato la letalità embrionale e le malformazioni grossolane, ma un obiettivo associato era quello di indagare sul comportamento dei cuccioli appena nati. Molti di questi studi aziendali mostrano una morte fetale correlata alla dose e altre caratteristiche coerenti con una capacità teratogena. L’esistenza di questi studi progettati per cercare prove delle conseguenze comportamentali dell’assunzione di SSRI durante la gravidanza rimane per la maggior parte sconosciuta con gli studi non pubblicati e i dati inaccessibili.
Esiste tuttavia una serie crescente di studi indipendenti sugli animali che dimostrano difetti alla nascita legati all’uso di SSRI con una serie di meccanismi che possono sostenere questi effetti [ 24 ].
Coerentemente con questi studi e meccanismi, una serie di studi epidemiologici dal 1998 in poi hanno dimostrato che gli SSRI sono dotati di un potenziale teratogeno [ 25-52 ]. Questi risultati sono riassunti in Healy et al. [ 53 ] e Berard et al. [ 24 ].
Gli studi sugli animali finalmente pubblicati mostrano costantemente che i cuccioli nati da animali a cui sono stati somministrati antidepressivi durante la gravidanza mostrano una serie di cambiamenti comportamentali indicativi di una ridotta fiducia sociale e deficit di comunicazione coerenti con una diagnosi di disturbi dello spettro dello sviluppo neurologico negli esseri umani [ 54-61 ].
1.2 Obiettivi
Domanda: Esistono prove che suggeriscano un legame tra l’ingestione materna di antidepressivi SSRI durante la gravidanza e gli effetti successivi sulle misure della funzione cognitiva che possono portare a diagnosi di deficit comportamentali nei bambini esposti in utero, principalmente una diagnosi di ASD?
Domanda: Se esiste un collegamento, ci sono prove da studi di intervento sugli animali di meccanismi biologici che potrebbero essere alla base dell’effetto?
3. Metodi
2.1 Progettazione
Abbiamo effettuato una ricerca sistematica di tutti gli studi epidemiologici che collegano l’uso di antidepressivi che inibiscono la ricaptazione della serotonina durante la gravidanza all’ASD e costrutti correlati come ritardo dello sviluppo o disturbo pervasivo dello sviluppo nella prole. Inoltre abbiamo cercato pubblicazioni rilevanti per la gamma di possibili meccanismi attraverso i quali l’uso di antidepressivi potrebbe dar luogo a una diagnosi di ASD nella prole. Abbiamo seguito le linee guida MOOSE per le meta-analisi e le revisioni sistematiche degli studi osservazionali [ 62 ].
2.2 Strategia di ricerca
Abbiamo cercato Embase, OVID e la Cochrane Library per identificare gli abstract in lingua inglese pubblicati fino a dicembre 2015. I termini di ricerca e la strategia sono stati determinati dagli investigatori con la consulenza di un bibliotecario. Abbiamo applicato i seguenti termini di ricerca in varie combinazioni adattate per ciascun database: Termini di ricerca: antidepressivi, inibitori selettivi della ricaptazione della serotonina, SSRI, gravidanza, disturbo dello spettro autistico, ritardo dello sviluppo, autismo, ADHD, difetti alla nascita. Abbiamo anche cercato manualmente elenchi di riferimenti di articoli inclusi ed esclusi per articoli di potenziale rilevanza.
2.3 Gestione dei dati
Gli abstract sono stati recuperati e vagliati e gli articoli ritenuti di potenziale rilevanza sono stati conservati. Questi articoli sono stati vagliati in dettaglio e sono stati inclusi articoli che soddisfacevano i criteri di inclusione. Ogni abstract vagliato e ogni articolo potenzialmente rilevante recuperato è stato rivisto indipendentemente da due autori (JLN e DM). Le discordanze sono state risolte mediante discussione tra i tre autori. Gli articoli di revisione sono stati esclusi, sebbene i riferimenti siano stati cercati a mano per altri studi contenenti dati originali pertinenti.
Gli abstract sono stati inclusi per l’analisi (umani) se soddisfacevano i seguenti criteri di inclusione:
- Fornito dati sull’esposizione all’uso gestazionale di SSRI
- Fornite misure quantitative della funzione cognitivo comportamentale o di sviluppo nei bambini esposti in utero
- Controllato per l’esposizione ad altri farmaci potenzialmente teratogeni
Gli abstract sono stati inclusi per l’analisi (animale) se essi:
- Fornivano dati sull’uso gestazionale di antidepressivi
- Fornivano misure quantitative rilevanti per i risultati cognitivi comportamentali o di sviluppo
Non abbiamo limitato il disegno dello studio, ma dovevano essere disponibili risultati quantitativi. Abbiamo escluso gli articoli di cui non siamo riusciti a ottenere una traduzione in inglese, gli articoli di revisione e gli studi di cui disponevamo di abstract.
I dati degli articoli inclusi sono stati estratti utilizzando un modulo standardizzato che descrive le seguenti caratteristiche dello studio: anno, popolazione target, posizione, dimensione del campione, disegno dello studio, misura dei risultati, lacune nelle conoscenze, conclusioni chiave e impostazione dello studio. Abbiamo valutato le citazioni e gli strumenti duplicati.
Laddove i dati sui risultati erano disponibili all’interno dello studio pubblicato, li abbiamo estratti da ciascuno di questi studi. Dove i dati non erano disponibili, abbiamo scritto agli autori per richiederlo.
2.4 Analisi statistiche
Tutte le analisi sono state condotte utilizzando Review Manager 5.2 (Copenhagen: The Nordic Cochrane Centre, The Cochrane Collaboration, 2012).
Abbiamo eseguito due analisi principali, una per valutare l’associazione tra uso materno di SSRI in gravidanza e ASD e l’altra per valutare l’associazione tra uso materno di SSRI in gravidanza e altre anomalie dello sviluppo neurologico correlate all’autismo.
Ci sono problemi metodologici nel tracciare questi dati. Negli studi sui bambini, alcuni di età inferiore a un anno, è possibile solo osservare il ritardo dello sviluppo piuttosto che i risultati che, per consenso, indicano specifici fallimenti della comunicazione sociale piuttosto che il deterioramento cognitivo in generale. Alcuni studi presentano risultati attraverso una serie di indicatori neurologici morbidi (fino a 10 in uno studio). Per tracciare i dati è quindi necessario ricavare una misura rappresentativa da ogni studio da inserire nel forest plot. Ciò è stato delineato nelle tabelle allegate. Tutti i dati sono disponibili presso gli autori che consentiranno ad altri di inserire diversi set di dati nel grafico, come indicato.
3. Risultati
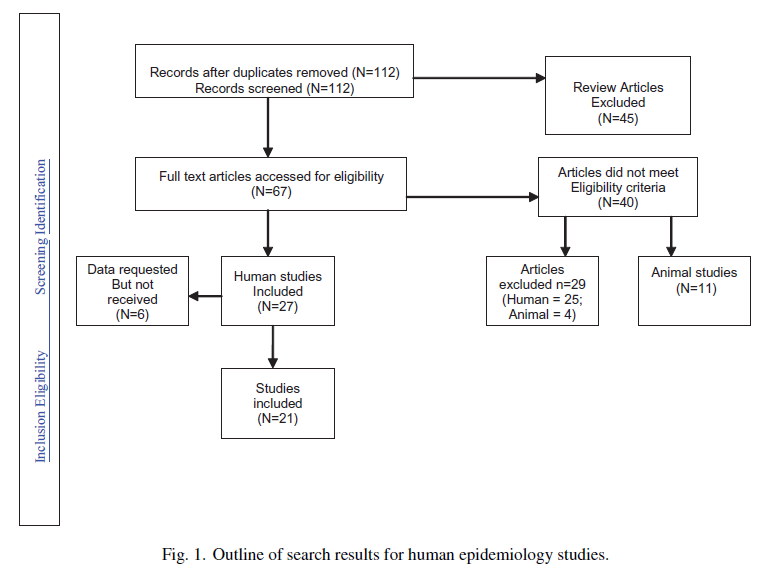
Il diagramma di flusso ( Fig. 1 ) mostra i risultati della ricerca dello studio. La nostra ricerca ha recuperato 112 citazioni di cui 67 erano abstract potenzialmente rilevanti. Di questi 67 abstract selezionati, 38 articoli soddisfano i criteri di inclusione. Di questi 27 erano studi sull’uomo e 11 erano studi sugli animali. Dati adatti erano disponibili per l’estrazione nei documenti di 21 studi e inclusi nel set di dati sull’uomo. Non abbiamo ricevuto risposte alle richieste di dati dai tre studi Motherisk [ 64-66 ] e Suri et al. [ 67 ]. Casper et al. [ 68 ] e Galbally et al. [ 69 ] ha indicato l’impossibilità di accedere ai dati al momento della richiesta.
Undici studi sugli animali sono stati identificati con dati adeguati per l’astrazione dai documenti pubblicati.
La dimensione dei partecipanti allo studio umano variava da 36 a 654.000. 16 dei 21 studi inclusi nell’analisi utilizzavano un disegno di coorte e 5 erano caso controllato.
La maggior parte degli studi inclusi indica un legame tra SSRI e ASD, con quasi tutti gli studi pubblicati che indicano un aumento del rischio anche se nei singoli studi l’aumento non è significativo [ 68-83 ].
Alcuni studi hanno riferito di non aver riscontrato alcun aumento del rischio [ 64-66 ], tuttavia i dati non erano disponibili dalle pubblicazioni di questi studi e una richiesta di dati agli autori non ha ricevuto risposta.
Uno studio di Malm e colleghi ha rilevato che le donne che assumono SSRI mostrano un’incidenza 10 volte maggiore di disturbi dello spettro alcolico fetale (FASD) rispetto alle donne che non assumono SSRI [ 43 ]. Questi risultati sono supportati da segnalazioni di eventi avversi di FASD ed effetti comportamentali coerenti con FASD alla FDA per tutti gli SSRI e segnalazioni di SSRI che causano l’assunzione compulsiva di alcol [ 84 ]. I risultati di Malm suggeriscono che altri studi dovrebbero cercare questa sindrome clinica che si sovrappone all’ASD e in particolare non dovrebbero scartare gli effetti dell’assunzione di alcol come confondente.
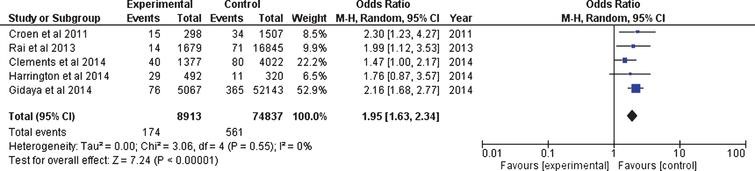
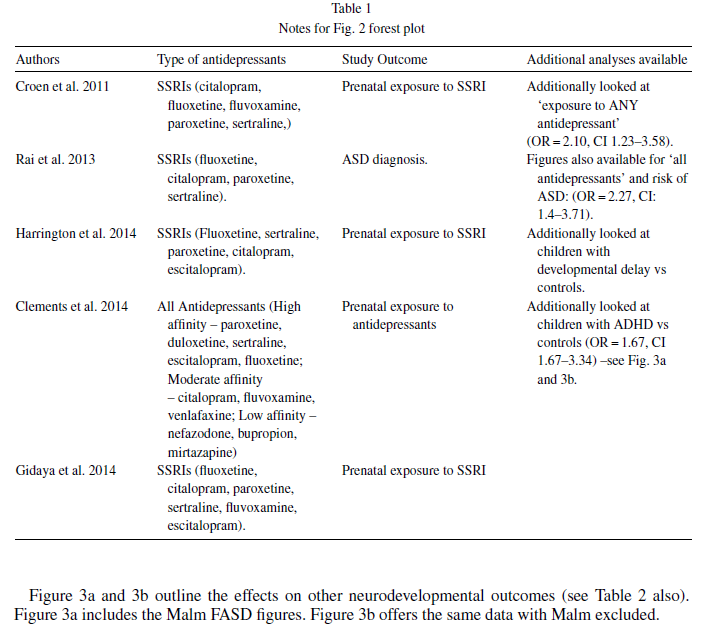
I risultati dei singoli studi epidemiologici caso-controllo, nonché l’effetto combinato e le statistiche sono presentati nella figura 2 (vedere anche la tabella 1 ).
3.1 Potenziali meccanismi
In termini di effetti degli antidepressivi sullo sviluppo neurologico, abbiamo estratto una serie di meccanismi attraverso i quali gli SSRI gestazionali potrebbero avere un impatto sulla funzione cognitiva che la letteratura recente supporta.
Innanzitutto, come notato sopra, la serotonina ha un ruolo nell’embriogenesi e ci sono prove convincenti che il disturbo di questa funzione porta a difetti in molti sistemi, da quello cardiaco a quello neurologico [ 24 ]. Oltre alle prove di gravi difetti congeniti, ci sono state prove da studi sugli animali per oltre un decennio che gli SSRI possono portare ad anomalie nell’architettura cerebrale [ 85-87 ]. Non abbiamo trovato studi che dimostrino la normale architettura del cervello. Questi cambiamenti sembrano collegati a un ridotto comportamento esplorativo e a una ridotta reattività [ 88 ].
In secondo luogo, gli SSRI hanno effetti profondi sul comportamento sessuale e ci si può aspettare che questo abbia conseguenze a lungo termine nel dominio sociale [ 55, 56, 89 ].
In terzo luogo, gli SSRI possono indurre l’assunzione compulsiva di alcol [ 84 ] e ci si potrebbe aspettare che questo contribuisca in qualche modo al quadro epidemiologico. Lo studio di Malm et al. [ 43 ] suggerisce di sì.
In quarto luogo, una caratteristica nota degli SSRI è che producono l’esperienza di un’emozione smorzata [ 90 ]. Collegati a questo sembrerebbe, portano a decrementi nelle nostre capacità di leggere le emozioni [ 91 ]. Questi effetti comportamentali sono in sintonia con i cambiamenti che si registreranno sugli strumenti attualmente utilizzati per rilevare le difficoltà di comunicazione e probabilmente porteranno a una diagnosi di ASD.
Questo punto è diventato di maggiore interesse alla luce delle prove che collegano il paracetamolo (paracetamolo) all’ASD [ 92 ]. Mentre il collegamento qui potrebbe sorgere indirettamente, se il paracetamolo viene usato per trattare la febbre, questo medicinale sembra anche avere effetti paragonabili agli SSRI sulla socialità negli animali [ 93 ] e sulla capacità delle persone di leggere le emozioni [ 94 ]. Il paracetamolo ha anche effetti sui recettori S-1, quindi c’è una notevole sovrapposizione nel suo meccanismo di azione con gli SSRI.
Sia il paracetamolo che gli SSRI possono quindi mediare i loro effetti attraverso cambiamenti comportamentali allo stadio terminale. Questi cambiamenti comportamentali possono durare per mesi dopo l’interruzione del trattamento negli adulti. Se somministrato in utero, una possibilità è che tali cambiamenti possano avere ancora più probabilità di durare e produrre un quadro clinico ASD.
In quinto luogo, dato che le attuali diagnosi di ASD possono includere bambini con problemi cognitivi generali piuttosto che disturbi specifici di una discreta funzione comunicativa, una serie di fattori correlati al trattamento, dall’astinenza da SSRI agli interventi chirurgici postnatali per correggere i difetti congeniti, può contribuire al potenziale di questi farmaci dare origine a quadri clinici di ASD.
Infine, quando si considerano questi meccanismi, sarebbe un errore concentrarsi esclusivamente su un presunto ASD. È importante stabilire l’intera gamma di effetti che questi farmaci hanno e vi è letteratura emergente ma non ancora pubblicata secondo cui i tassi di ADHD, ad esempio, possono essere aumentati nei bambini nati da madri che assumono SSRI. Tutti i meccanismi proposti devono essere in grado di tenere conto anche di tali cambiamenti.
4. Discussione
I Forest plot mostrano la coerenza dei risultati fino ad oggi. Sia che si guardi a una diagnosi rigorosa di ASD, includendo solo il caso-controllo o tutti gli studi osservazionali o valutando altri esiti dello sviluppo neurologico, gli SSRI hanno un modello coerente di associazione con esiti peggiori. L’aumento dei tassi di ritardo dello sviluppo legato all’uso di SSRI in gravidanza può anche essere coerente con l’aumento dei tassi di diagnosi di ASD nella prole delle donne esposte a questi trattamenti. Non è chiaro cosa significhi questo collegamento. Alcuni dei dati possono riflettere disprassia o segni neurologici molli correlati che non devono necessariamente essere accompagnati da menomazioni cognitive o sociali e possono scomparire in età avanzata.
Questi risultati sono supportati da risultati coerenti negli studi sugli animali esaminati e dall’esistenza di una serie di meccanismi biologicamente plausibili negli esseri umani.
Questa revisione si basa su precedenti revisioni di Gentiles [ 95 ] e Mann et al. [ 96 ]. Gentiles ha fornito una revisione narrativa delle prove, sebbene non abbia eseguito una meta-analisi. Contrariamente a Mann et al. abbiamo incluso due importanti studi nella revisione [ 70, 73 ] e incluso meta-analisi o revisione di studi su altri esiti dello sviluppo neurologico, nonché revisione sistematica delle prove quantitative da studi sugli animali.
Esiste inoltre una serie di meccanismi attraverso i quali gli effetti degli SSRI potrebbero portare a risultati che attirano una diagnosi di ASD. Per far progredire la nostra comprensione sarà necessario prendere in considerazione sia i risultati epidemiologici che gli studi fisiologici. La ragione per rivedere questi meccanismi fisiologici è che l’evidenza epidemiologica è a un punto in cui è ormai chiaro che è necessaria una maggiore specificità nei fenotipi clinici per dare un senso ai possibili collegamenti tra trattamento e risultati.
Lo stato della scienza in via di sviluppo mappa sui rispettivi ruoli dell’epidemiologia e della biologia nel chiarire il rischio di difetti alla nascita sulla doxilamina (Bendectin). La doxilamina è usata per la nausea in gravidanza. Negli anni ’70 era collegato a difetti cardiaci e degli arti [ 97 ]. Tuttavia, diversi primi studi epidemiologici mettono in dubbio il legame tra doxilamina e difetti congeniti [ 98-101 ].
Esaminando tutti gli studi epidemiologici sulla doxilamina, è chiaro che mentre molti studi non mostrano alcun aumento del rischio, la maggioranza mostra un certo aumento del rischio rispetto al non trattamento [ 102-114 ].
Ora c’è una maggiore comprensione dei periodi di tempo critici in cui i farmaci possono portare a difetti cardiaci e di altro tipo, chiarendo che i risultati epidemiologici devono essere interpretati in un contesto che riconosce che le donne raramente iniziano a prendere la doxilamina prima della settimana 6-8 e da questo tempo il rischio di difetti cardiaci è stato quasi eliminato [ 115 ]. Questo fatto rende notevole qualsiasi aumento del rischio.
C’è un ulteriore sfondo. La doxilamina è un antistaminico. Sembra esserci un aumento del rischio di difetti alla nascita con gli antistaminici che inibiscono la ricaptazione della serotonina, come la doxilamina, rispetto agli antistaminici che non inibiscono la ricaptazione della serotonina [ 116 ] e analogamente un aumento del rischio con gli antidepressivi che inibiscono la ricaptazione della serotonina, non riscontrato negli antidepressivi che sono inattivi sul sistema della serotonina [ 53, 117 ].
Poiché l’assunzione di doxilamina inizia relativamente tardi nel primo trimestre, gli studi epidemiologici, pur indicando che è improbabile che causi difetti alla nascita, potrebbero da soli non essere in grado di risolvere la questione se abbia il potenziale di causare difetti alla nascita. Nel giudicare se questo farmaco presenti dei rischi, le prove biologiche sono informative, sebbene abbiano anche i loro limiti.
Come indica il caso del paracetamolo, a questo punto non sappiamo se gli effetti fisiologici dei farmaci che inibiscono la ricaptazione della serotonina sul ritardo dello sviluppo siano mediati a livello molare alterando le nostre percezioni sociali o a livello ionico. Difetti cardiaci grossolani potrebbero essere collegati a cambiamenti nel flusso di ioni sodio, ad esempio con effetti comportamentali derivanti dagli effetti cognitivi dei farmaci.
È necessario che l’epidemiologia rimanga biologicamente informata e che i biologi siano consapevoli del fatto che le diagnosi di ASD e gli strumenti utilizzati negli studi epidemiologici potrebbero fuorviarli su quali fattori fisiologici debbano essere ulteriormente esplorati. Niente lo illustra meglio delle prove di Malm et al. studio [ 43 ], che è coerente con gli effetti noti degli SSRI nell’indurre l’assunzione di alcol in una sottopopolazione di soggetti e un recente RCT che mostra esiti di consumo peggiori con il trattamento con citalopram per il disturbo da dipendenza da alcol [ 118 ].
Questo studio di Malm indica anche che, sebbene sia stato di routine aggiustare per fattori confondenti come l’assunzione di alcol, tali aggiustamenti potrebbero essere sbagliati nel caso di antidepressivi che inibiscono la ricaptazione della serotonina con SSRI che hanno effetti sia sull’assunzione di alcol e nicotina che sui livelli di glucosio.
4.1 SSRI in gravidanza
Affinché l’uso di SSRI abbia avuto un ruolo nell’aumento dei tassi di ASD, ci aspetteremmo che ci siano prove che probabilmente c’è stato un aumento nell’uso di questi farmaci nelle donne in età fertile e un atteggiamento medico e pubblico più rilassato nei confronti l’uso di questi farmaci durante la gravidanza.
A differenza dei precedenti antidepressivi in cui il mercato era in gran parte nelle fasce di età più avanzata, era chiaro che gran parte del mercato degli SSRI sarebbe stato per le donne in età fertile.
All’inizio degli anni ’90, quando gli SSRI furono commercializzati per primi, l’opinione prevalente era che la somministrazione di psicofarmaci in gravidanza doveva essere evitata; le autorità di regolamentazione hanno sostenuto l’evitamento [ 119 ], gli organismi professionali hanno sostenuto l’evitamento [ 120 ] e i principali psichiatri hanno avvertito del potenziale teratogeno degli psicofarmaci [ 121-123 ].
Non si pensava che ci fosse alcun aumento nell’incidenza dei disturbi dell’umore durante la gravidanza [ 124 ]. Non si pensava che ci fosse alcun rischio di disturbi dell’umore per il feto; il rischio di disturbi dell’umore risiedeva nel rischio posto alla madre come il suicidio [ 125 ].
Al contrario oggi è comune sentire affermazioni secondo cui la depressione provoca direttamente o indirettamente difetti alla nascita; vedere una fusione di sintomi depressivi con malattie depressive, in modo che i tassi del 15-20% per i disturbi depressivi siano citati quando questo dovrebbe applicarsi solo ai sintomi depressivi [ 53 ]; e non è ampiamente notato che la maggior parte degli stati trattati con questi farmaci non trattati si risolve spontaneamente entro poche settimane.
Nel 2015, in assenza di dati intermedi sul fatto che la depressione causi malformazioni congenite o che gli SSRI siano efficaci nella depressione prenatale, è possibile trovare gli stessi autori che all’inizio degli anni ’90 sostenevano cautela sull’uso di antidepressivi, a sostegno delle affermazioni secondo cui:
- La depressione può causare malformazioni congenite [ 126 ]
- Gli antidepressivi non causano difetti congeniti o problemi cognitivi [ 127 ]
- Che eliminare gli antidepressivi è sconsigliabile [ 128 ]
- Gli organismi professionali approvano l’uso di antidepressivi [ 129 ]
Se gli SSRI funzionano, come sostiene il marketing, cioè correggendo un’anomalia serotoninergica, si potrebbe pensare che riducano il rischio che le cose vadano male. Ma non esiste tale anomalia e il trattamento con un SSRI a conti fatti lascerà i sistemi della serotonina più anormali di quanto fossero all’inizio [ 130 ].
Se lavorare significa che gli SSRI riducono i comportamenti rischiosi tra cui l’assunzione di alcol e droghe, l’evidenza è in qualche modo contraria; Gli SSRI possono aumentare il consumo di alcol e droghe [ 84, 131 ].
4.2 Spiegazioni alternative
Le preoccupazioni su un legame tra SSRI e difetti congeniti hanno incontrato le seguenti contro argomentazioni che sono facilmente applicabili qui.
In primo luogo, i tassi di ASD di questi studi, come nel caso dei tassi di difetti alla nascita con SSRI, rientrano nel tasso di base della popolazione in generale e su questa base si sostiene che anche laddove i tassi nel gruppo trattato superano quelli nel il gruppo di controllo, questi tassi possono essere scontati [vedi 128, 132]. Questo argomento non è valido per gli studi sui difetti congeniti in cui il tasso di base è determinato dal disegno dello studio. L’argomento è fuori luogo per una condizione come ASD o disturbi dello spettro dello sviluppo neurologico in cui il tasso di base sembra cambiare di anno in anno.
In secondo luogo, gli studi sull’uso di SSRI durante la gravidanza mostrano un tasso costante di problemi e che quando tutti gli studi vengono meta-analizzati i rischi scompaiono. Non siamo stati in grado di analizzare tutti gli studi poiché alcuni gruppi, come il gruppo Motherisk, si rifiutano di condividere i propri dati.
In terzo luogo, si afferma che la depressione causi sia difetti alla nascita che ASD ed è endemica nelle donne in gravidanza con tassi del 15-20%. Crediamo che non ci siano prove valide per queste proposizioni.
In quarto luogo, si propone che non vi siano studi adeguati e ben condotti in questo settore. Questa affermazione significa che non ci sono RCT e presuppone che il lettore accetterà la proposizione che solo gli RCT possono dimostrare se un antidepressivo causa difetti alla nascita o ASD o meno. A nostro avviso questa posizione non è corretta. Gli RCT possono ottenere la risposta tanto sbagliata quanto qualsiasi altro studio epidemiologico [vedi 133]. Per stabilire cosa sta accadendo serviranno giudizi che tengano conto sia dei dati epidemiologici sia di quelli biologici. È solo quando c’è una buona comprensione di ciò che sta accadendo che può essere progettato un RCT appropriato.
Infine, si afferma che i risultati citati dalla maggior parte degli studi non mostrano alcuna differenza statisticamente significativa tra le donne trattate e quelle non trattate. Per alcuni, se un aumento del rischio non è significativo, ritengono che in realtà non vi sia alcun aumento del rischio. Questa non è la visione più ampiamente accettata nel campo [134]. Le trame visive delle meta-analisi dimostrano chiaramente questo punto.
5. Conclusioni
L’ASD è attualmente un’entità amorfa e ha alcune radici nell’autismo classico, ma ora sembra comprendere aree precedentemente denominate difficoltà di apprendimento o ritardo dello sviluppo. In tutto questo spettro ci sono prove che l’assunzione di farmaci che inibiscono la ricaptazione della serotonina può portare a risultati peggiori, anche se al momento c’è poca chiarezza sui meccanismi più probabili coinvolti.
Ulteriori progressi in quest’area richiederanno una maggiore precisione in termini di fenotipi clinici e sforzi per controllare le variabili intervenienti come interventi operativi per difetti alla nascita o assunzione di alcol in gravidanza. L’area richiede l’istituzione di registri di gravidanza completi.
Bibliografia
Vedi l’originale, disponibile a questo link