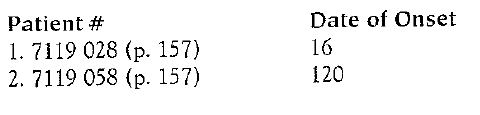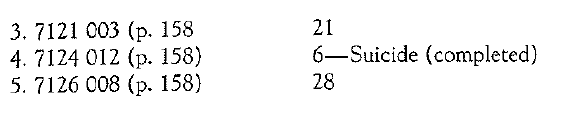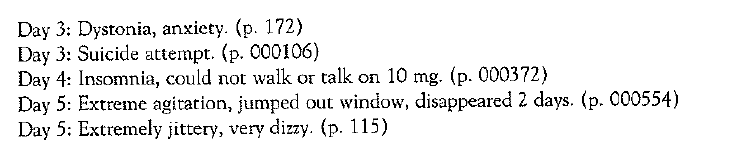Peter R. Breggin, MD
lthaca, New York
Pubblicato su Ethical Human Psychology and Psychiatry 2006
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
Questa è la seconda di una serie di relazioni speciali sui dati precedentemente soppressi relativi all’antidepressivo Paxil (Paroxetina), inibitore selettivo della ricaptazione della serotonina (SSRI) e la sua capacità di causare violenza e suicidio.
I dati sono stati riportati in una relazione che ho scritto come esperto medico per una causa di responsabilità del prodotto contro il produttore del Paxil, Lacuzong contro GlaxoSmithKline (GSK). 1 Dopo aver preso Paxil 10 mg per 3 giorni, il signor Lacuzong ha annegato i suoi due figli e se stesso in una vasca da bagno. Il caso fu infine “risolto” senza che i dettagli dell’accordo fossero resi pubblici. La compagnia farmaceutica ha negato tutte le accuse.
Il mio rapporto sulla responsabilità del prodotto si basava su numerose fonti, in particolare su un viaggio di 3 giorni negli uffici della casa farmaceutica per esaminare i suoi file interni che spiegano come il Paxil è stato ricercato, sviluppato e commercializzato. Fino a questi rapporti speciali, le informazioni in questi file non erano state rese pubbliche.
Dopo la pubblicazione del mio primo rapporto speciale su come il produttore del Paxil ha nascosto e manipolato i dati relativi al suicidio indotto dal Paxil (Breggin, 2006), la FDA e la casa farmaceutica GlaxoSmithKline hanno rilasciato dichiarazioni che confermano che gli adulti depressi di tutte le età che assumono l’antidepressivo hanno un tasso aumentato di suicidalità rispetto agli adulti depressi che assumono placebo (Kraus, 2006).
Questi adulti con disturbo depressivo maggiore hanno subito un aumento di 6,4 volte nel tasso di ideazione e comportamento suicidario rispetto ai controlli che ricevevano la pillola di zucchero (0,32% contro 0,05%). Questa meta analisi di studi clinici controllati con placebo si è anche concentrata su giovani adulti a cui era stato prescritto il Paxil per i disturbi d’ansia oltre che per la depressione. In questo gruppo diagnostico più ampio, giovani adulti (età 18-24) a cui è stato dato Paxil erano anche ad aumentato rischio di suicidalità.
Riassumendo questi dati, il Paxil ha aumentato la suicidalità negli adulti depressi di tutte le età e anche nei giovani adulti con depressione, distimia, disturbo di panico, disturbo d’ansia generalizzato e disturbo ossessivo compulsivo.
I tassi di suicidalità indotta da Paxil saranno molto più alti nella pratica clinica reale dove l’esposizione al farmaco dura tipicamente molto più di 4-6 settimane, il monitoraggio del paziente è molto meno accurato, i farmaci multipli spesso esacerbano le reazioni avverse al farmaco, e molti pazienti sono già suicidi.
Ammettendo che il Paxil causa suicidalità negli adulti, la FDA e la GlaxoSmithKline hanno confermato le osservazioni che ho fatto nelle mie pubblicazioni e nelle testimonianze in tribunale per più di un decennio (per esempio, Breggin, 1997, 2001; Breggin & Breggin, 1994). La FDA e la compagnia farmaceutica hanno rilasciato i loro risultati poche settimane dopo la pubblicazione del mio primo rapporto speciale su EHPP, che mostrava che la casa farmaceutica aveva soppresso i dati rilevanti per molti anni (Breggin, 2006).
Il mio primo rapporto speciale, “Court Filing Makes Public My Previously Suppressed Analysis of Paxil’s Effects”, ha descritto come un recente procedimento giudiziario abbia reso disponibile al pubblico il mio rapporto sulla responsabilità del prodotto, nonostante i precedenti sforzi della GSK per sopprimerlo.
Il mio rapporto speciale iniziale forniva stralci della mia analisi di responsabilità del prodotto su come la casa farmaceutica ha manipolato i dati relativi alla suicidalità indotta dal Paxil. Per esempio, l’analisi della GSK sulla suicidalità ha lasciato aut aut due tentativi di suicidio e due suicidi completati con il Paxil, ed ha esagerato il numero di atti suicidari con il placebo. L’azienda ha anche ridotto l’apparente importanza degli eventi legati al suicidio fornendo analisi separate di overdose, tentativo di suicidio e suicidalità. È più utile e significativo combinare tutte le attività legate al suicidio in una sola categoria, la suicidalità.
Per la parte II del rapporto speciale, ho estratto delle sezioni dal mio rapporto sulla responsabilità del prodotto su come la compagnia farmaceutica ha nascosto sia i tassi di acatisia indotta dal Paxil che la relazione tra acatisia e suicidalità.
L’acatisia è un’agitazione interiore indotta dal farmaco o una disforia che induce una persona a sentirsi costretta a muoversi. Le sensazioni dolorose associate all’acatisia sono state paragonate alla tortura e spesso fanno sentire le persone come se stessero diventando “pazze”. Le persone che soffrono di acatisia spesso danno voce a descrizioni drammatiche come “elettricità che scorre nelle mie vene”, “orribili sensazioni frastagliate nella mia testa” o “qualcosa che pizzica i miei nervi in tutto il corpo”. Queste descrizioni vivide e disperate possono essere scambiate per deliri o allucinazioni (American Psychiatric Association, 1994, 2000; Breggin, 1997).
Quando la FDA approvò inizialmente il Paxil il 29 dicembre 1992, era già stato riportato che gli antidepressivi SSRI tendono ad indurre tassi estremamente alti di acatisia. Per esempio, Lipinski, Mallaya, Zimmennan e Pope (1992) hanno descritto cinque casi e, basandosi su una revisione della letteratura, hanno stimato che il Prozac (fluoxetina) causa acatisia nel 9,7%-25% dei pazienti.
Dagli anni ’70, gli studi sull’acatisia indotta da neurolettici hanno dimostrato che l’acatisia causa gravi disturbi emotivi, tra cui aggressività, suicidalità e un peggioramento della psicosi (van Putten, 1975; van Putten & Marder, 1987; Breggin, 1983, 1997). Nei primi anni ’90, i rapporti clinici cominciarono a collegare l’acatisia indotta dal Prozac alla suicidalità grave, acuta e ossessiva (per esempio, Rothschild & Locke, 1991; Teicher, Glod & Cole, 1990).
Nel 1994, il Diagnosdc and Statistical Manunl ofMental Disorders, Fourth Edidon (DSM IV, 1994, pp. 744-746) ha tentato di riassumere i dati clinici e di ricerca disponibili riguardanti l’acatisia indotta da farmaci. Ha dichiarato: “L’acatisia può essere associata a disforia, irritabilità, aggressività o tentativi di suicidio”. Il manuale si concentrava sull’acatisia indotta dai neurolettici, ma chiariva che gli stessi problemi sono associati all’acatisia indotta dagli antidepressivi SSRI: “I farmaci antidepressivi inibitori della ricaptazione della serotonina possono produrre acatisia che sembra essere identica, per fenomenologia e risposta al trattamento, all’acatisia acuta indotta dai neurolettici”.2
Poiché era già noto che l’acatisia indotta dagli SSRI provoca suicidalità, violenza e deterioramento mentale generale, la GSK era tenuta a condurre un’attenta analisi di acatisia indotta dal Paxil. L’azienda era anche tenuta a cercare un legame tra l’acatisia indotta dal Paxil e le anomalie mentali o comportamentali. Invece, GSK ha fatto di tutto per nascondere il fatto che il Paxil provoca acatisia e che alcuni casi di acatisia del Paxil erano associati a suicidalità.
Gli antidepressivi SSRI possono causare suicidalità e violenza con mezzi diversi dall’acatisia, compresa l’agitazione indotta dal farmaco, la depressione e la mania. I pazienti che erano precedentemente depressi possono essere spinti in stati di depressione agitata o in reazioni maniacali (Breggin, 2003). Gli effetti stimolanti dei SSR, dall’acatisia e agitazione alla mania, sono responsabili di causare alcune delle più gravi aberrazioni mentali e comportamentali.
Alcuni progressi sono stati fatti dalla Food and Drug Administration (FDA) nel mettere in guardia sui rischi associati alla stimolazione o attivazione degli SSRI (rivisto in Breggin, 2005). L’agenzia ora richiede che le etichette degli antidepressivi riportino diverse avvertenze relative alla stimolazione media e all’acatisia, incluse le seguenti:
Peggioramento clinico e rischio di suicidio: I pazienti, le loro famiglie e chi si prende cura di loro devono essere incoraggiati ad essere attenti all’emergere di ansia, agitazione, attacchi di panico, insonnia, irritabilità, ostilità, aggressività, impulsività, acatisia (irrequietezza psicomotoria), ipomania, mania, e altri cambiamenti insoliti nel comportamento, peggioramento della depressione e ideazione suicidaria, specialmente all’inizio del trattamento con antidepressivi e quando la dose viene regolata su o giù. (FDA, 2005a, p. 2)
La FDA richiede anche che le etichette degli antidepressivi riportino un’avvertenza “scatola nera” sull’aumentato rischio di suicidalità nei bambini che prendono questi farmaci (FDA, 2005a). Sebbene non sia richiesto un avvertimento specifico sull’aumentato rischio di suicidalità negli adulti che prendono questi antidepressivi, la FDA ha emesso un Public Health Advisory sul potenziale pericolo negli adulti (FDA, 2005b). I dati divulgati in questo rapporto speciale dovrebbero conferire un peso scientifico alle preoccupazioni della FDA e incoraggiare un’avvertenza specifica in etichetta sull’aumentato rischio di suicidalità negli adulti che assumono antidepressivi SSRI come il Paxil.
I seguenti estratti dal mio rapporto sulla responsabilità del prodotto datato 21 luglio 2001, si concentrano sull’acatisia. Oltre ad esaminare come la GSK ha manipolato o soppresso i dati riguardanti l’acatisia, questi risultati confermano un legame tra l’acatisia indotta dal Paxil e la suicidalità. I dati confermano anche che queste reazioni gravi possono verificarsi a partire dalla prima dose del farmaco e che spesso si verificano nei primi giorni dell’esposizione iniziale.
Il mio rapporto sulla responsabilità del prodotto può essere trovato nella sua interezza sul mio sito web, www.breggin.com. Esso copre numerose preoccupazioni aggiuntive su come GSK ha ricercato, sviluppato e commercializzato il Paxil.
III. Eliminare l’acatisia come termine preferito e come termine dello sperimentatore
(l) Definizione di Akathisia. L’acatisia è un disturbo neurologico causato dai farmaci. Stedman’s Medicai Dictionary, 27th edition (2000) definisce l’acatisia come “Una sindrome caratterizzata da un’incapacità di rimanere in una postura seduto, con irrequietezza motoria e una sensazione di tremolio muscolare”. L’American Psychiatric Association Diagnostic and Sta tistical Manual ofMental Disorders, IV (DSM-IV) (1994; 2000) descrive l’acatisia nel contesto dei farmaci neurolettici, ma [come notato nel DSM IV] le manifestazioni cliniche sono le stesse quando l’acatisia è indotta da antidepressivi SSRI.
Il DSM-IV osserva che l’acatisia comprende i seguenti sintomi:
lamentele soggettive di irrequietezza e almeno uno dei seguenti movimenti osservati: movimenti agitati o oscillazione delle gambe mentre si è seduti, dondolio da un piede all’altro o “camminare sul posto” mentre si è in piedi, camminare per alleviare l’irrequietezza, o un’incapacità di stare in piedi per almeno diversi minuti. (p. 744)
In generale, se l’esperienza soggettiva di agitazione, ansia, irritabilità o sensazioni simili è accompagnata da movimenti motori volontari, come il camminare o il dondolio dei piedi, la sindrome viene identificata come acatisia.
(2) Acatisia, violenza e suicidio. Il DSM-IV afferma senza qualificazioni,
“L’acatisia può essere associata a disforia, irritabilità, aggressività o tentativi di suicidio” (p. 745). C’è un considerevole corpo di letteratura che conferma l’associazione tra acatisia e violenza e suicidio. Ho esaminato parte della letteratura in Breggin e Breggin (1994) e Breggin (1997) [più recentemente in Breggin 2003] per quanto riguarda gli psicofarmaci in generale e in particolare i SSR di cui fa parte il Paxil. Teicher et al. (1993) hanno esaminato la violenza e il suicidio indotti dagli SSRI. Più recentemente, Glenmullen (2000) ha dedicato una parte significativa di un libro alla revisione della letteratura e alla discussione della violenza e del suicidio indotti dagli SSRI.
(3) L’espurgo dell’acatisia. È estremamente importante che i medici sappiano che un farmaco può causare acatisia. L’acatisia, come termine, segnala i pericoli di angoscia emotiva e il potenziale di indurre al suicidio e alla violenza. Non è solo fraudolento ma anche pericoloso per i pazienti nascondere che un farmaco può causare acatisia. È particolarmente pericoloso quando il farmaco è usato per trattare la depressione, perché l’acatisia nei pazienti depressi è particolarmente probabile che li spinga al suicidio o ad atti violenti.
Akathisia è stato sistematicamente eliminato dalla SKB (ora GSK) come termine preferito dagli studi statunitensi e non statunitensi. Questo significava che i sintomi tipici dell’acatisia non sarebbero stati codificati come acatisia, ma come qualcos’altro, come agitazione o stimolazione del sistema nervoso centrale. (I termini preferiti sono le parole usate per descrivere specifici effetti avversi, come acatisia, agitazione o mania. Sono selezionati da un libro di codici fornito dalla FDA. Se l’acatisia non è elencata dall’azienda come termine preferito nel suo piano o protocollo per uno studio, allora gli investigatori codificheranno o elencheranno l’acatisia come qualcos’altro, come l’agitazione. Quasi ogni termine è meno minaccioso di acatisia).
Sorprendentemente, l’acatisia non appare nemmeno come termine dell’investitore su nessuno dei rapporti statunitensi che ho trovato. Appare solo come termine dell’investigatore in circa una dozzina di rapporti non statunitensi, mentre i sintomi attribuibili all’acatisia abbondano nei riassunti dei rapporti statunitensi di reazioni avverse ai farmaci. Da ciò si deve concludere che SKB non solo ha rimosso l’acatisia da qualsiasi elenco di termini preferiti, ma deve anche aver comunicato agli sperimentatori principali che il termine non doveva essere usato in nessuno dei rapporti di farmaci avversi o riassunti clinici.
Chiaramente la SKB ha preferito non far sapere alla FDA o alla professione medica che il Paxil causa acatisia. Infatti, l’hanno lasciato fuori dalla sezione intitolata “Adverse Experiences in Clinical Trials: Dati mondiali” (Sezione V-NDA. PAR Safety Summary 20-Nov- 1989, pp. 83-88; vedi anche Tabella V.7, p. 114).
Allo stesso modo, l’acatisia è stata lasciata fuori dalla sezione intitolata “Adverse Experience verificatesi durante il trattamento attivo – studi di fase II e III negli Stati Uniti”, “Sistema nervoso” (Appendice V.8, in NDA 20031-Vol422 novembre 1989, pp. 189/190-275/276). Non c’è nessun elenco per l’acatisia, ma molti rapporti di irrequietezza e nervosismo correlati.
(4) L’acatisia scivola nei rapporti non statunitensi. Tuttavia, alcune acatisia sono sfuggite nei rapporti non statunitensi. Nella sezione intitolata “Esperienze avverse verificatesi durante il trattamento attivo – Studi di fase II-III non statunitensi”, V.1, pp. 129-199, abbiamo trovato 13 rapporti espliciti di acatisia e acatisia motoria (un sinonimo). Inoltre, c’erano molte descrizioni di acatisia elencate sotto altri termini preferiti.
(5) La FDA aggiunge l’acatisia all’etichetta di Paxil Label. Alla fine la FDA ha insistito che SKB aggiungesse l’acatisia come reperto post-marketing senza insistere sulla causalità. La richiesta viene in una lettera nel settembre 1993 dal Paul Leber alla SKB (SB 0000247). Se la FDA fosse stata informata durante il premarketing del gran numero di casi di acatisia in associazione con il Paxil, sarebbe stata in grado di determinare più fermamente la causalità.
In risposta, una versione di label creata dalla SKB e datata 2.05.94 aggiunge acatisia ed EPS come risultati postmarketing.3 Avrebbero dovuto essere messi nel label come un risultato premarketing che coinvolgeva più casi (p. 000022).Uno dei due rapporti citati dalla FDA è stato ricevuto dall’Irlanda. Tuttavia, l’azienda aveva già molti rapporti di acatisia in suo possesso dall’Europa, ma deve aver omesso di informare la FDA.
Per ripetere, la FDA ha richiesto una menzione di acatisia nell’etichetta basata solo su due rapporti post-marketing, anche se SKB aveva già in suo possesso una dozzina di rapporti di acatisia esplicitamente identificati dagli studi pre-marketing non statunitensi e, come documenteremo, decine di altri casi di acatisia codificati con diversi termini preferiti, come agitazione e stimolazione del sistema nervoso centrale, negli studi pre-marketing statunitensi.
(6) Come la FDA codifica l’acatisia. La FDA ha sviluppato un sistema di codifica per i termini di reazione avversa. Il dizionario si intitola “COSTART: Coding Symbols far The saurus of Adverse Reactian Terms” Ho la quinta edizione (1995) nella mia biblioteca, ma non è cambiato per quanto riguarda l’acatisia. Come ogni altra azienda farmaceutica, SKB è stata supposta di basare la sua raccolta e analisi dei dati sulle reazioni avverse sul sistema COSTART.
Questo è discusso, per esempio, in un memorandum di SKB, “FDA Conversation Record” (9.5.91), che memorizza una conversazione con Thomas Laughren della FDA in cui si parla, tra le altre cose, dell’uso dei termini COSTART (SB 0000158). In effetti, il memo commenta che Laughren (la “Divisione”, cioè la Divisione dei Prodotti Farmaceutici Neurofarmacologici della FDA) avrebbe preso decisioni su quali termini tagliare dall’etichetta.
Fin dall’inizio, COSTART ha codificato l’acatisia come acatisia. Cioè, il termine preferito per acatisia è acatisia. Questo era vero durante lo sviluppo del primo SSRI, il Prozac. Pertanto, SKB deviateci dal sistema di classificazione della FDA per classificare i casi di acatisia come qualcos’altro, come l’agitazione. Riclassificando l’acatisia, così come fermando l’uso del termine in generale, SKB ha reso impossibile alla FDA o a chiunque altro determinare con precisione il numero totale di pazienti che hanno sofferto di acatisia in seguito all’assunzione di Paxil. Questo è stato estremamente fraudolento.
(7) Scopo della frode sull’acatisia. La frode doveva essere effettuata con piena conoscenza, perché era ben noto che l’SSRI originale, Prozac, ha causato l’acatisia. La label originale del Prozac elencava l’acatisia ma stimava la sua occorrenza come “infrequente.” È diventato rapidamente evidente, tuttavia, che l’acatisia indotta dal Prozac era comune e pericoloso.
Nel 1989, Joseph Lipinksi e i suoi colleghi del McLean Hospital e della Harvard Medicai School pubblicarono cinque casi di acatisia indotta da Prozac che comportavano notevoli disturbi emotivi. Sulla base di una revisione della letteratura, i ricercatori stimano il tasso di acatisia indotta dal Prozac tra il 9,7% e il 25%. Nel 1990, il Public Citizen Health Research Group (collegato all’organizzazione di Ralph Nader) nella sua Healt Letter stimò similmente il tasso di acatisia indotta dal Prozac al 15%-25%. Inoltre, come illustrano i rapporti di Teicher et al. (1990) e Rothschild e Locke (1991), l’acatisia indotta dagli SSRI come potenziale causa di suicidio e violenza era un argomento di discussione in letteratura anche prima dell’approvazione del Paxil.
Nella prossima sezione, troveremo un legame diretto tra il suicidio e la stimolazione, inclusa l’acatisia, nei file NDA della SKB stessa.4
IV. Rianalisi dei termini preferiti nelle sperimentazioni statunitensi
Oltre all’acatisia, il Paxil causa comunemente una varietà di sintomi correlati di stimolazione del sistema nervoso centrale (SNC), tra cui la stessa stimolazione SNC, ansia, agitazione, nervosismo, irritabilità e insonnia. Questi sintomi di stimolazione sono estremamente importanti perché anch’essi sono associati al suicidio e alla violenza (Breggin & Breggin 1994; Breggin 1997 [e più recentemente, Breggin 2003]).
È risaputo nella professione medica che la stimolazione può indurre i pazienti depressi a compiere atti di suicidio Pertanto, è estremamente importante che i medici sappiano che un farmaco antidepressivo provoca stimolazione, ed è fraudolento e pericoloso nascondere loro questa informazione
Sfortunatamente, la SKB non solo ha cercato di nascondere i fatti sulla stimolazione indotta dal Paxil e sull’acatisìa, ma la società ha rilasciato false clausole sul Paxil a questo proposito. Ho già documentato che la FDA ha protestato a volte contro queste false affermazioni. Come altro esempio, SKB ha sviluppato un lungo documento intitolato “Paxil (paroxetina cloridrato) Hospital Formulary Product Infonnation” (SB 0000261, datato dicembre Il, 1992). I
esso, SKB sostenne che Paxil era efficace in “pazienti depressi con sintomo associato di ansia” (SB 0000271) e che il farmaco possedeva un profilo di reazione avversa con “bassa incidenza di nervosismo, agitazione e ansia”. Queste affermazioni sono false. Infatti, come la FDA ha dichiarato (vedi precedente) e come continueremo a documentare, il Paxil causa nervosismo, agitazione, irritabilità, ansia e sintomi di stimolazione correlati in una grande percentuale di pazienti depressi, spesso nei primi 3 giorni.
Scopriremo anche che i casi di acatisia sono stati nascosti in termini preferenziali definiti dall’azienda (cioè i termini preferiti dalla casa farmaceutica come agitazione, ansia, stimolazione nervosismo e tremore).
Quanto segue è una rianalisi di diverse categorie di effetti avversi legati al SNC che l’azienda ha organizzato secondo i suoi termini preferiti selezionati:
(l) Termine preferito Agitazione. Agitazione aveva 75 voci (pp. 191-193). Un totale di 49 dei 75 pazienti con agitazione erano infatti affetti da acatisia. Di questi, 47 erano descritti dal termine “irrequieto” e menzionavano il movimento delle gambe o dei piedi (un caso). Come indicato dalla definizione di acatisia (vedi precedente), questi casi sono molto probabilmente acatisia. Coerentemente con il caso Lacuzong, 21 si sono verificati nei primi l-3 giorni. Altri 11 si sono verificati tra i 4 e i 5 giorni. Sempre in linea con il caso Lacuzong, sette casi si sono sviluppati a basse dosi di 10 mg.
(2) Ansia a termine preferito. Delle 86 segnalazioni nella categoria “ansia”, 24 sono state descritte come “tensione” e 1 come “inquietudine”. Anche se non è così definitivo come nel caso del termine preferito “agitazione”, molti di questi casi erano probabilmente acatisia. Di grande importanza, 26 si sono verificati nei primi 1 a 3 giorni. Altri 9 si sono verificati in 4 a 5 giorni; 8 si sono verificati alla dose di 10 mg.
(3) Termine preferito Nervosismo. Sotto la categoria “nervosismo” (pp. 235-238), 44 su 91 erano probabilmente collegati all’acatisia. Sono stati identificati con i seguenti termini: pacing, jumpy, jittery, e fidgety. L’agitazione era la più comune. In tutto, 23 dei 91 rapporti si sono verificati nei primi 1-3 giorni. Altri 15 si sono verificati in 4 o 5 giorni.
(4) Termine preferito tremore. Sotto il “ Preferito termine Tremore”, c’era un numero molto grande di segnalazioni (pp. 268-273) che non ho valutato completamente. Molti erano legati all’acatisia.
V. Analisi dell’acatisia negli studi clinici non statunitensi di fase II e III
l) Rapporti di acatisia secondo il termine dello sperimentatore. A differenza degli Stati Uniti, alcuni casi di acatisia sono stati riportati utilizzando il termine di acatisia dello sperimentatore negli studi di fase II-III non statunitensi (per Aropax, un altro nome commerciale della paroxetina, novembre 1989, Appendice V.l). Sono stati codificati sotto il termine preferito di stimolazione del SNC piuttosto che sotto acatisia:
(2) L’acatisia legata al tentativo di suicidio. Degli otto pazienti con diagnosi di acatisia, solo quattro sono stati identificati dal numero di paziente [e quindi potevano essere ricondotti ai loro rapporti clinici dettagliati]. Dei quattro pazienti identificati con diagnosi di acatisia, uno (25%) ha tentato il suicidio. Inoltre, il paziente ha tentato il suicidio lo stesso giorno del rapporto sull’acatisia (vedi NDA Suicide Report, Appendice 2, pagina 17).
E’ molto importante che il comitato identifichi gli altri quattro pazienti.
(3) Rapidità di insorgenza dell’acatisia. Di particolare importanza per il caso Lacuzong, l’acatisia inizia spesso nei primi giorni di trattamento. Dei quattro pazienti identificati, uno non aveva dati di insorgenza. Dei sette pazienti con dati di insorgenza, tutti sono stati diagnosticati in 9 o meno giorni di trattamento. Sei sono stati diagnosticati entro una settimana dal trattamento. Tre sono stati diagnosticati entro 1 o 2 giorni dal trattamento.
(4) Rapporti di “acatisia motoria” come termine investigativo. L’acatisia motoria è identica alla acatisia. Il termine sottolinea semplicemente la manifestazione esterna dei sintomi. Ci sono stati cinque casi:
(5) Acatisia motoria collegata al suicidio. Dei cinque pazienti con diagnosi di “acatisia motoria”, 1 (20%) si è suicidato. Così, dei 13 pazienti identificati con diagnosi di<acatisia o acatisia motiria” 2 (15%) hanno tentato o completato il suicidio.
(6) Suicidi completati legati agli effetti avversi del SNC, inclusa l’acatisia. Siamo stati in grado di rintracciare cinque casi di suicidio completato ai loro riepiloghi di caso originali. Dei cinque pazienti che si sono suicidati con successo con Paxit, a tutti sono stati diagnosticati AERs (Adverse Event Reports) legati al SNC prima del suicidio. Di questi cinque casi, almeno due diagnosi pre-suicidio (40%), agitazione e acatisia motoria, erano legate alla stimolazione e/o acatisia. Tutti avevano reazioni avverse ai farmaci del SNC.
I seguenti sono i cinque casi di suicidio completati seguiti dai termini dello sperimentatore per le loro reazioni avverse ai farmaci.
VI. Insorgenza rapida di reazioni avverse ai farmaci (ADR) documentate dal sistema di segnalazione spontanea
I dati post-marketing dallo Spontaneous Reporting System dateci luglio 1993 confermano che gravi ADRs possono svilupparsi nel primo giorno o due di trattamento, incluse reazioni che influenzano negativamente il comportamento (NDA20031; SB 0000912). Ecco un piccolo campione estratto dai rapporti sulle esperienze avverse.
VII. Il ruolo della “stimolazione del sistema nervoso centrale”, “lrritabilità” e “Eccitazione” nel suicidio e nella violenza
(l) Stimolazione e Irritabilità negli US Trials. “L’irritabilità è usata in psichiatria per descrivere l’iper-reattività emotiva degli individui che può portare ad ostilità e violenza inappropriate o smodate. (Vedere, per esempio, Stedman’s Medica! Dictionary, 2000, o il PDR Medica! Dictionary, 1995).
L’irritabilità è un termine molto più forte in psichiatria che nell’uso comune. Nel Diagnostic and Statistical Manual of Menta! Disorders, IV (1994), una diagnosi di Disturbo dell’Umore Indotto da Sostanze può essere fatta sulla base di qualsiasi “umore irritabile” da solo (p. 374).
Appendice V.8, “Esperienze avverse verificatesi durante il trattamento attivo: U.S. Phase II-Ill Trials” (SB 0000669, p. 198, timbrato 199), elenca la Stimolazione del SNC come termine preferito. Nella categoria della stimolazione del SNC, i termini dello sperimentatore erano di solito legati a reazioni comportamentali anormali, come “irritabile”, “irritabilità” e “aumento dell’irritabilità”.
Ci sono stati 19 rapporti relativi all’irritabilità. C’erano 7 rapporti relativi a “eccitazione” e “intense scariche di eccitazione”. Altre segnalazioni riguardavano la sensazione di essere “eccitati” e “agitati”.
Di questi circa 41 pazienti con 50 rapporti di stimolazione del sistema nervoso centrale, molti si sono verificati all’inizio del trattamento. Otto si sono verificati entro 1 o 2 giorni dall’inizio del trattamento. Cinque eventi avversi si sono verificati alla dose di 1 mg, nessuno dei quali nel periodo da 1 a 2 giorni.
(2) Ansia e suicidio da studi non statunitensi di fase II e III. Un conteggio manuale di “agitazione” come termine preferito (NDA 420 novembre 1989, p. 128 e seguenti) ha rivelato 43 rapporti, compreso un suicidio completato (2406 149) il 32° giorno di esposizione al Paxil.
Un conteggio manuale di “ansia, come termine preferito, ha rivelato 63 rapporti, con tre suicidi tentati nello stesso giorno, 3 giorni dopo il rapporto e 19 giorni dopo il rapporto. Ancora una volta c’è la prova che il suicidio è legato alla stimolazione (acatisia, agitazione, ansia) del Paxil.
Bibliografia
Vedi l’articolo originale disponibile a questo link