Irving Kirsch Harvard Medical School, Boston, MA, United States
Pubblicato su Frontiers in Psychiatry 2019
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
Introduzione
Lo scopo di questa recensione è di valutare l’effetto placebo nel trattamento dell’ansia e della depressione. Il 19 febbraio 2012, Leslie Stahl ha aperto un segmento del programma di notizie della CBS 60 minuti dicendo: “La comunità medica è in guerra, in lotta per la ricerca scientifica e gli scritti di uno psicologo di nome Irving Kirsch. La lotta riguarda gli antidepressivi e le domande di Kirsch sul loro funzionamento.” A quel tempo, avevo scritto tre meta-analisi e un libro sull’effetto placebo nel trattamento della depressione (1 – 4). Due di queste meta-analisi (2 , 3) sono stati condotti sui dati inviati alla Food and Drug Administration (FDA) dai produttori di quelli che a quel tempo erano i sei antidepressivi più ampiamente prescritti, dati che abbiamo ottenuto utilizzando il Freedom of Information Act. Abbiamo scoperto che sebbene le persone a cui erano stati somministrati antidepressivi mostrassero un notevole miglioramento negli studi clinici sottoposti alla FDA dai produttori, anche le persone a cui era stato somministrato il placebo, e la differenza nei risultati tra farmaco e placebo era al di sotto del criterio di significatività clinica utilizzato dal National Institute for Health and Care Excellence (NICE), l’organizzazione che stabilisce le linee guida per il trattamento del National Health Service nel Regno Unito.
Ora c’è una crisi riguardante la mancanza di replicabilità di molti studi in psicologia e medicina ( 5 , 6 ). Sono lieto di segnalare che le meta-analisi antidepressive che abbiamo pubblicato non hanno contribuito a questa crisi. Ora ci sono almeno nove successive meta-analisi volte a replicare o screditare i nostri studi ( 7 – 16). Alcuni di questi sono stati limitati ai cambiamenti della scala di valutazione Hamilton per la depressione (HAM-D), mentre altri includevano dati provenienti da una varietà di scale. Alcuni erano meta-analisi convenzionali in cui venivano utilizzate medie e deviazioni standard per calcolare le dimensioni degli effetti, mentre altri erano analisi a livello di paziente. Sebbene le interpretazioni dei dati variavano da uno studio all’altro, i risultati sono stati coerenti in tutti loro. Avevamo riportato una differenza media farmaco-placebo di 1,80 punti sull’HAM-D e una differenza media standardizzata (SMD) di 0,32. Le differenze riportate nelle repliche variavano da 1,62 a 2,56 punti HAM-D, con dimensioni dell’effetto SMD comprese tra 0,23 e 0,34. Per mettere questo in prospettiva, i criteri NICE per la significatività clinica delle differenze antidepressive-placebo sono tre punti su HAM-D o SMD di almeno 0,50, 17) proposto come effetto moderato.
Particolare attenzione è dovuta ai risultati preliminari di una meta-analisi a livello di paziente riportata da Stone et al. (15). Marc Stone è vicedirettore per la sicurezza presso la divisione dei prodotti psichiatrici della FDA. Lui e i suoi colleghi hanno riportato un’analisi a livello di paziente dei dati di tutti gli studi randomizzati controllati con placebo su antidepressivi nel trattamento del disturbo depressivo maggiore che erano stati sottoposti alla FDA tra il 1979 e il 2016. La somiglianza nei risultati tra i dati della Stone et al. e quelli che i miei colleghi e io avevamo riportato nel 2002 e nel 2008 sono sorprendenti. Avevamo riportato una risposta farmacologica di 10,1 punti sull’HAM-D e una risposta placebo di 8,3 punti, una differenza farmaco-placebo di 1,8 punti. Nell’analisi completa di Stone et al. Sui dati dei 73.178 pazienti nei 228 studi sottoposti alla FDA, la risposta al farmaco era di 10,1 punti, la risposta al placebo era di 8,3 punti, con una differenza farmaco-placebo di 1.2).
Gli antidepressivi sono anche usati per trattare i disturbi d’ansia. Potrebbero essere più efficaci nel trattamento dell’ansia che nel trattamento della depressione? I miei colleghi e io abbiamo valutato questo problema in una meta-analisi degli effetti della paroxetina nel trattamento dei disturbi d’ansia (18). Abbiamo scelto di limitare la nostra analisi alla paroxetina in modo da poter valutare un set di dati completo di studi pre e post-marketing non pubblicati, nonché quelli pubblicati. Come parte di una transazione legale del 2004, GlaxoSmithKline doveva pubblicare online i risultati di tutti gli studi clinici che coinvolgono i suoi farmaci nel suo registro di prova clinica (19). Esaminando questi dati, abbiamo trovato una dimensione dell’effetto farmaco-placebo (SMD) di 0,27, simile a quelle riportate per gli antidepressivi nel trattamento della depressione. In uno studio successivo, Roest et al. (20) analizzato i dati ottenuti dalla FDA per studi di pre-marketing su nove antidepressivi di seconda generazione nel trattamento dei disturbi d’ansia. Hanno riportato un SMD di 0,33, simile a quello riportato da Sugarman e colleghi per la paroxetina (18) e a quelli riportati nelle meta-analisi degli antidepressivi nel trattamento della depressione citata sopra. Successivamente, Sugarman e colleghi (21) replicato da Roest et al. studiare e trovare un SMD di 0,34 tra tutti gli antidepressivi e tutti i disturbi d’ansia, con dimensioni degli effetti individuali comprese tra 0,26 e 0,39. Pertanto, gli antidepressivi non sono migliori nel trattamento dei disturbi d’ansia rispetto al trattamento della depressione.
L’impatto dei fattori placebo nel trattamento dell’ansia può anche essere visto in uno studio di Faria et al. (22). I partecipanti con diagnosi di disturbo d’ansia sociale (DAU) sono stati trattati con un inibitore selettivo del reuptake della seratonina (SSRI) (escitalopram). Circa la metà dei pazienti è stata accuratamente informata che stavano assumendo un SSRI. Agli altri è stato detto che veniva loro somministrato un placebo attivo (cioè un farmaco che produce effetti collaterali ma non ha alcun effetto terapeutico sulla condizione da trattare). Dire ai pazienti che venivano curati da un farmaco attivo ha raddoppiato la sua efficacia su una misura continua di ansia e ha triplicato il tasso di risposta.
I critici hanno notato che i criteri proposti per il significato clinico da NICE (3 punti su HAM-D o SMD di almeno 0,50) sono arbitrari (23) e sono corretti. I criteri NICE sono arbitrari quanto il criterio di p <.05 per significatività statistica, l’uso di una riduzione del 50% dei sintomi come criterio di risposta clinica e l’uso di un punteggio HAM-D inferiore a 8 come il criterio di remissione. Dato che i limiti convenzionali per la significatività statistica sono arbitrari, così come quelli per la valutazione della “risposta” clinica e della “remissione”, perché dovremmo aspettarci che i criteri per la significatività clinica delle differenze farmaco-placebo siano meno arbitrari?
Tuttavia, Joanna Moncrieff e I.Kirsh (24) hanno proposto criteri empiricamente derivati per il significato clinico delle differenze antidepressive-placebo. Abbiamo usato i dati pubblicati da una grande analisi a livello di paziente (25) della corrispondenza tra i cambiamenti sulla scala HAM-D e Clinical Global Impressions-Improvement (CGI-I), una scala che valuta il miglioramento su una scala da 1 (molto migliorata) a 4 (nessuna modifica) a 7 (molto molto peggio). Questa analisi ha rivelato che un miglioramento di tre punti su HAM-D (SMD = 0,375) equivale a un punteggio clinico “nessun cambiamento” sul CGI-I. Un rating CGI-I di “minimamente migliorato” corrisponde a una differenza HAM-D di 7 punti (SMD = 0,873) e un rating di “molto migliorato” corrisponde a una differenza HAM-D di 14 punti (SMD = 1,75). Nessuna delle meta-analisi ha riportato differenze farmaco-placebo che si avvicinano al raggiungimento del criterio di valutazione CGI-I di miglioramento minimo, anche tra i pazienti più gravemente depressi.
Molti pazienti depressi riportano miglioramenti sostanziali dopo aver assunto farmaci antidepressivi, così come gli psichiatri quando descrivono i loro risultati. Come possiamo conciliare questo con la constatazione costante che le differenze tra la risposta agli antidepressivi e i placebo sono vanificanti? La risposta è la risposta placebo. Sebbene le differenze nei risultati tra farmaco e placebo non equivalgano affatto a nessuna differenza, sia le risposte del farmaco che quelle del placebo possono essere sostanziali. Il miglioramento di 8,3 punti dopo il trattamento con placebo e 10,1 punti sui farmaci attivi riportati da Kirsch et al. (3) e Stone et al. (15) corrisponde ai rating CGI-I tra minimamente migliorato e molto migliorato. È solo la differenza di 1,8 punti che corrisponde a un rating CGI-I di nessuna variazione. Pertanto, il miglioramento clinicamente significativo osservato in seguito alle prescrizioni di antidepressivi è in gran parte dovuto alla risposta al placebo (cioè all’effetto placebo, alla regressione verso la media e alla remissione spontanea). L’incapacità di trovare differenze significative tra antidepressivi e placebo è stata attribuita all’aumento delle risposte al placebo nel corso degli anni (26) e alcune meta-analisi hanno mostrato nel tempo aumenti sia della risposta del placebo che della risposta del farmaco [ad es., Rif. (27)]. Tuttavia, l’analisi completa di tutte le prove presentate alla FDA dal 1979 al 2016 racconta una storia diversa (15). La risposta placebo è stata di 8,3 punti HAM-D sia nel 1979 che nel 2016, con poche variazioni tra queste date. C’è stata una piccola diminuzione (0,8 punti) della differenza farmaco-placebo nel tempo, ma ciò era dovuto a una diminuzione di 0,8 punti nella risposta al farmaco (da 10,7 punti nel 1979 a 9,9 punti nel 2016), piuttosto che un aumento di la risposta al placebo.
Effetti placebo contro risposte placebo
Nel 1965, Fisher e colleghi (28 , pagg. 57–58) notarono che “una risposta clinica dopo il trattamento (risposta farmacologica) non è sinonimo di un effetto che può essere attribuito al trattamento (effetto farmacologico)”. Nel 1998, Kirsch e Sapirstein (4) hanno esteso questa distinzione alle risposte e agli effetti placebo, e nel 2018, un gruppo di 29 ricercatori placebo riconosciuti a livello internazionale hanno pubblicato una “dichiarazione di consenso”, in cui hanno approvato l’opinione che “la risposta placebo e nocebo include tutti i cambiamenti di salute che risultano dopo la somministrazione di un trattamento inattivo (cioè, differenze nei sintomi prima e dopo il trattamento), quindi, compresi la storia naturale e la regressione alla media. L’ effetto placebo e nocebo fa riferimento alle modifiche specificamente attribuibili ai meccanismi placebo e nocebo ”(29 , p. 206). Le meta-analisi sopra descritte indicano una forte risposta al placebo, ma con un’eccezione: non valutano l’effetto placebo.
Nell’unica eccezione (4), Guy Sapirstein e io abbiamo valutato l’effetto placebo confrontando la risposta placebo negli studi farmacologici con i cambiamenti osservati in condizioni di controllo della storia naturale senza trattamento negli studi di psicoterapia. Abbiamo scoperto che il 25% della risposta farmacologica è stato duplicato nei gruppi senza trattamento e il 75% della risposta farmacologica è stata trovata nei gruppi placebo. Pertanto, l’effetto placebo è stato del 50% della risposta farmacologica, il doppio dell’effetto farmacologico e anche il doppio della risposta riscontrata nei controlli di non trattamento. È stato un vero effetto placebo.
Una limitazione del nostro studio era che i dati nei gruppi senza trattamento e quelli nei gruppi placebo provenivano da studi diversi. Tale limitazione è stata superata in uno studio clinico riportato da Leuchter e dai suoi colleghi (30). Questo è stato uno studio a tre bracci, in cui i pazienti depressi sono stati randomizzati in antidepressivi più terapia di supporto, placebo più terapia di supporto o terapia di supporto da sola. Il miglioramento medio di HAM-D è stato di 10,05 punti nel gruppo antidepressivo e 7,59 nel gruppo placebo, ma solo 1,37 nel solo gruppo di terapia di supporto. Come nello studio di Kirsch e Sapirstein, la risposta nel gruppo placebo è stata per lo più un vero effetto placebo e non semplicemente dovuto al miglioramento spontaneo o alla regressione verso la media.
C’è un effetto farmacologico?
Sebbene la differenza tra antidepressivo e placebo non sia clinicamente significativa, è statisticamente significativa. Possiamo interpretare quella piccola ma statisticamente significativa differenza come dovuta al farmaco? Sebbene ciò non possa essere escluso, esiste un’altra possibilità. Gli studi clinici in cui ai pazienti e/o ai loro medici o ad altri esattori viene chiesto di giudicare se al paziente sia stato somministrato un farmaco attivo o un placebo sono coerenti nel dimostrare che tali giudizi sono molto accurati. Ciò indica che le prove non sono realmente in doppio cieco. Numerosi studi hanno dimostrato che quando i pazienti sanno di ottenere un farmaco, sono più sensibili al farmaco rispetto a quando sanno che potrebbero essere sempre un placebo (31 – 35). Ciò indica un componente con effetto placebo nella risposta al farmaco. Allo stesso modo, la risposta al placebo è ridotta quando le persone sanno che potrebbero assumere un placebo rispetto a quando sono portati a credere di assumere il farmaco attivo (31 , 36). Pertanto, la piccola differenza tra farmaco e placebo nei risultati potrebbe essere dovuta all’aumentata risposta nel gruppo di farmaci e alla ridotta risposta nel gruppo di placebo prodotta da ciò che i partecipanti raccontano degli studi.
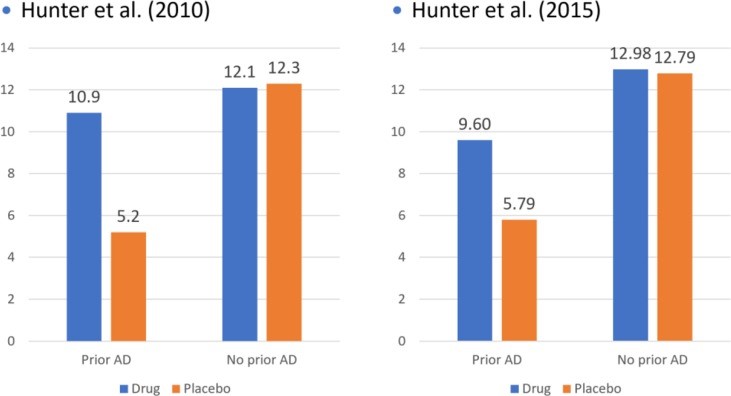
Nel 1986 Rabkin e i suoi colleghi (1986) pubblicarono uno studio in cui ai medici e ai loro pazienti depressi che erano stati randomizzati a imipramina, fenelzina o placebo fu chiesto di indovinare il gruppo a cui erano stati assegnati i pazienti. Complessivamente, il 78% dei pazienti e l’87% dei medici hanno identificato con precisione se ai pazienti fosse stato somministrato un farmaco attivo o un placebo. Come mostrato nella Figura 1 , i pazienti randomizzati a gruppi di farmaci attivi hanno avuto particolare successo nel rompere il cieco, mentre quelli che assumono placebo sembrano semplicemente indovinare. Al contrario, i medici hanno mostrato alti livelli di accuratezza nell’identificare l’assegnazione di gruppo per i pazienti nei gruppi placebo e quelli nei gruppi di farmaci. Inoltre, questo modello di risultati è stato replicato con successo in studi successivi (38- 41), indicando che sono affidabili. Rabkin et al. ha concluso che “alla luce di questi risultati raccomandiamo che gli investigatori registrino e riferiscano sistematicamente le opinioni di medici e pazienti sull’assegnazione del trattamento in studi randomizzati, preferibilmente sia all’inizio dello studio che alla fine” (p. 86). Sfortunatamente, questa raccomandazione è stata ampiamente ignorata.
Dati questi tassi eccezionalmente elevati di non vedenti, la domanda successiva è se questo fenomeno è associato all’esito degli studi clinici. Nel 2013, Baethge e colleghi (42) hanno riportato i risultati di una meta-analisi che affronta questo problema. In 47 studi clinici su disturbi psichiatrici in cui è stata valutata l’accecamento, la correlazione tra l’accuratezza del paziente e la dimensione dell’effetto farmaco-placebo era di .51 (p = .002) e quella tra l’accuratezza del rater e la dimensione dell’effetto era di .55 (p = .067 ). Pertanto, maggiore è la probabilità di non vedenti, maggiore è la differenza farmaco-placebo.
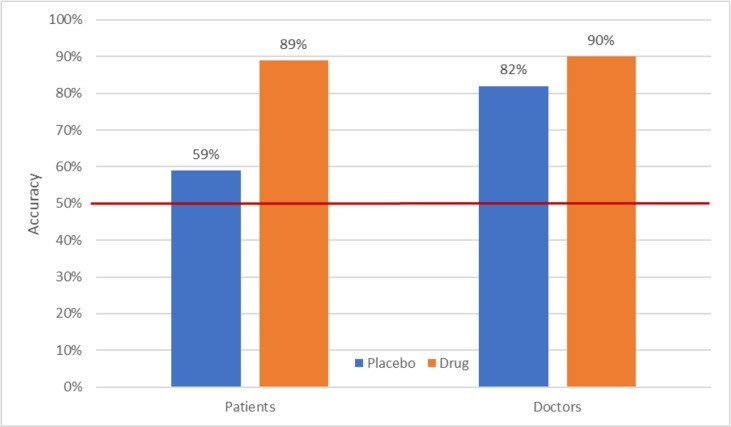
Tuttavia, esiste un problema interpretativo rispetto alla comprensione della direzione della causalità nei dati sull’accuratezza dei giudizi di assegnazione di gruppo. Nella maggior parte degli studi in cui è stato valutato l’accecamento, la valutazione è stata effettuata verso la fine della sperimentazione. Pertanto, è possibile che rompere il buio sia una conseguenza piuttosto che una causa delle differenze farmaco-placebo. Tuttavia, alcuni dei dati riportati da Rabkin et al. (37) indicano che il cieco non è solo una conseguenza delle risposte dei pazienti al trattamento. Figura 2 mostra l’accuratezza dei giudizi separatamente per i pazienti che hanno risposto al trattamento e quelli che non lo hanno fatto. Di particolare interesse è la capacità di entrambi i pazienti e i medici di indovinare con precisione l’assegnazione di gruppo di non rispondenti nel gruppo di farmaci. Il settantaquattro percento dei non rispondenti che hanno ricevuto un farmaco attivo si è giudicato sul farmaco, così come l’84% dei loro medici. Inoltre, quasi la metà dei pazienti che hanno risposto al placebo ha indovinato di assumere placebo. Anche se questo sarebbe prevedibile per caso, ciò indica che il miglioramento riscontrato da questi responder al placebo non li ha portati a pensare di assumere un farmaco attivo. Nel loro insieme, questi dati indicano che sebbene la risposta al trattamento influenzi i giudizi dei pazienti e dei medici sull’assegnazione del trattamento, non spiega completamente l’accuratezza di tali giudizi.
Io e altri ( 1 , 43 , 44 ) abbiamo ipotizzato che la presenza di effetti collaterali sia responsabile della rottura del cieco. Come parte dei processi di consenso informato, ai pazienti negli studi clinici viene detto che potrebbero ricevere un placebo. Gli viene anche detto che il farmaco in esame ha effetti collaterali e viene detto esattamente quali sono gli effetti collaterali noti. Ora i placebo possono anche generare effetti collaterali, un fenomeno noto come effetto nocebo, ma lo fanno in misura molto inferiore rispetto ai farmaci attivi (45). Questa differenza negli effetti collaterali potrebbe portare i pazienti negli studi clinici, così come i medici che valutano il loro miglioramento, a capire a quale gruppo sono stati randomizzati. Nella misura in cui ciò accade, il processo non è realmente in doppio cieco. In questa sezione, descrivo i dati che indicano che i pazienti negli studi clinici spesso fanno il cieco e che il cieco influisce sugli esiti degli studi.
Gli studi hanno mostrato risultati contrastanti per l’ipotesi e le differenze farmaco-placebo sono associate agli effetti collaterali riportati (46 – 5). Tuttavia, gli effetti collaterali possono essere solo uno degli spunti che portano i partecipanti agli studi clinici a non vedersi. Joanna Moncrief (52) ha ipotizzato che le persone imparino a riconoscere i cambiamenti a volte sottili prodotti dai farmaci senza riportare necessariamente i sintomi che sarebbero elencati come un effetto collaterale sulle liste di controllo utilizzate per valutarli.
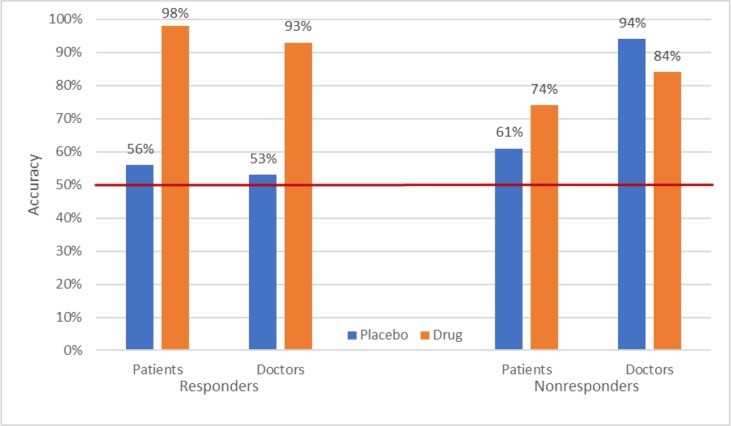
Due studi condotti da Aimee Hunter e colleghi dell’UCLA forniscono supporto indiretto a questa ipotesi (53 , 54). In ciascuno di questi studi, i pazienti depressi negli studi clinici sono stati raggruppati a seconda che non avessero mai assunto antidepressivi prima. Come mostrato in Figura 3, non vi erano praticamente differenze tra il farmaco e il placebo tra i pazienti che non avevano mai assunto antidepressivi prima. Al contrario, tra quelli con esperienza precedente, le differenze farmaco-placebo erano sia significative che sostanzialmente maggiori rispetto a quelle riportate in altri studi clinici, mentre le differenze combinate per i partecipanti con esperienza antidepressiva e ingenui antidepressivi sono nella stessa gamma di altri studi clinici. Nel loro insieme, i dati di entrambi gli studi suggeriscono fortemente che le prescrizioni per gli antidepressivi non dovrebbero essere date a persone depresse che non le hanno mai prese prima.
Che cosa si deve fare?
Come dovremmo trattare la depressione? Un suggerimento che mi è stato fatto in modo informale è di prescrivere antidepressivi come placebo attivi. Un placebo attivo è una sostanza farmacologicamente attiva che non ha attività specifica per la condizione da trattare. I farmaci antidepressivi hanno effetti farmacologici minimi o nulli sulla depressione o sull’ansia, ma suscitano un sostanziale effetto placebo. Non potremmo usarli come mezzo per capitalizzare sul potere del placebo?
Il problema con questo suggerimento è che le decisioni sul trattamento devono essere basate su una valutazione dei rischi, nonché sui benefici. I rischi del trattamento antidepressivo comprendono comportamenti aggressivi suicidi e violenti negli adolescenti e nei giovani adulti; ictus, morte per tutte le cause, cadute e fratture e convulsioni epilettiche negli anziani; e disfunzione sessuale, sintomi di astinenza, diabete, trombosi venosa profonda e sanguinamento gastrointestinale e intracranico in tutti gli altri ( 55 – 62 ). Si potrebbe sostenere che vale la pena prendere questi rischi per un trattamento efficace della depressione grave, ma vale la pena rischiare per un trattamento che non ha alcun beneficio rispetto al placebo per gli utenti alle prime armi?
Una seconda possibilità sarebbe quella di prescrivere placebo. Sono sicuri ed efficaci, con relativamente pochi effetti collaterali di nocebo e senza rischi per la salute. Il problema con la prescrizione di placebo dipende dall’assunto comunemente ritenuto che per essere efficaci nella pratica clinica, i placebo devono essere presentati ingannevolmente come farmaci attivi. Questo assunto è stato segnalato come falso in recenti studi clinici [rivisto in Rif. ( 63)]. In questi studi, i placebo sono stati presentati in modo non ingannevole come placebo senza ingredienti attivi. Come potrebbe mai funzionare? La risposta è che è stato accompagnato da una logica in cui è stato spiegato che i placebo sono stati trovati efficaci per la condizione da trattare, che è stato trovato che coinvolgono il condizionamento pavloviano e che potrebbe quindi essere efficace nel trattamento delle condizioni della persona. Questa logica è risultata critica per il successo dell’intervento in aperto di placebo (OLP) ( 64 ). Sono garantiti ulteriori studi OLP con campioni più grandi, durata più lunga e valutatori in cieco.
Sfortunatamente, solo uno degli studi sulla valutazione degli OLP ha coinvolto il trattamento della depressione e quello, sebbene abbia mostrato risultati promettenti, era solo un piccolo pilota ( 65 ). Tuttavia, ci sono molti altri trattamenti che eguagliano gli antidepressivi in termini di grado di riduzione dei sintomi ( 66 – 69 ). Questi includono psicoterapia, esercizio fisico, agopuntura, omega-3, omeopatia, tai chi, qigong e yoga. Non conosciamo i meccanismi di questi trattamenti alternativi e la loro efficacia potrebbe essere almeno in parte dovuta all’aspettativa, ma sono certamente più sicuri dei farmaci antidepressivi.
Il vantaggio a lungo termine della psicoterapia rispetto ai farmaci è stato dimostrato in numerosi studi [rivisto in Rif. ( 70 )]. Mentre i risultati a breve termine erano equivalenti tra i due trattamenti, i risultati a lungo termine erano significativamente migliori per i pazienti che avevano ricevuto psicoterapia rispetto a quelli che avevano ricevuto farmaci. Inoltre, il programma di ricerca collaborativa per il trattamento della depressione del National Institute of Mental Health (NIMH) ha riportato tassi di ricaduta rispettivamente del 36% e del 33% per la terapia comportamentale cognitiva e la terapia interpersonale, rispetto a un tasso di ricaduta del 50% per i farmaci antidepressivi (71). Tuttavia, il tasso di recidiva per i pazienti che si erano ripresi con il placebo era del 33%, lo stesso di quello della psicoterapia. Ci sono due messaggi da portare a casa da questi dati. Innanzitutto, dissipa il mito secondo cui le risposte al placebo hanno vita breve. In secondo luogo, solleva la questione se la psicoterapia riduca la ricaduta o se i farmaci la aumentano ( 72 ).
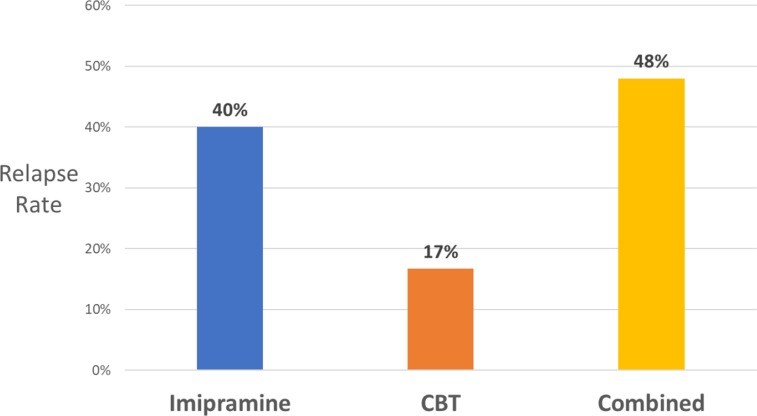
Il supporto all’ipotesi che i farmaci antidepressivi aumentino il rischio di recidiva proviene da altri studi che hanno confrontato il trattamento antidepressivo e placebo per i disturbi della depressione e dell’ansia. Coerentemente con i dati NIMH, una meta-analisi del 2011 ha riportato un tasso di ricaduta del 25% per i pazienti depressi trattati con successo con placebo rispetto a tassi di ricaduta che vanno dal 42% al 57% tra quelli trattati con vari antidepressivi ( 73 ). Un test diretto dell’effetto degli antidepressivi e della psicoterapia sul rischio di ricaduta proviene da uno studio sul trattamento del disturbo di panico 74). Lo studio ha confrontato i tassi di recidiva di 6 mesi per i pazienti che erano stati trattati con un antidepressivo triciclico (imipramina), terapia cognitivo comportamentale (CBT) o i due combinati. I risultati, mostrati in Figura 4 , indicano che il rischio di ricaduta a seguito di imipramina era più del doppio rispetto alla CBT. Tuttavia, l’aggiunta dell’antidepressivo all’imipramina ha completamente cancellato tale beneficio. Allo stesso modo, l’esercizio fisico come trattamento per la depressione ha dimostrato di avere un tasso di ricaduta molto più basso rispetto agli SSRI, ma questo beneficio scompare quando i due trattamenti sono combinati ( 75 ).
Questi studi rivelano un altro vantaggio di includere placebo nei test clinici dei farmaci. Possono rivelare situazioni in cui il trattamento fa più male che bene alla condizione da trattare. Ad esempio, i placebo hanno sovraperformato i farmaci antipsicotici (aloperidolo e risperidone) nel trattamento del delirio nei pazienti con cure palliative e nell’aggressione negli adulti con disabilità intellettiva ( 76 , 77 ). Allo stesso modo, il placebo è stato significativamente migliore di una combinazione di condroitina e glucosamina nel trattamento dell’osteoartrosi del ginocchio (78) e ha mostrato una superiorità simile in uno studio di nutraceutici nel trattamento della depressione (79).
Dati questi dati, suggerisco di utilizzare i seguenti principi nella selezione del trattamento. Quando i trattamenti sono ugualmente efficaci, raccomandare il più sicuro. Quando sono ugualmente sicuri, lascia che il paziente scelga quale preferisce. Prima di fare questa scelta, tuttavia, i pazienti devono essere accuratamente informati dei potenziali danni dei farmaci antidepressivi (ad esempio, aumento del rischio di recidiva, suicidalità, sanguinamento gastrointestinale e intracranico, trombosi venosa profonda, embolia polmonare, diabete, ictus, epilessia e morte per tutte le cause), nonché la scoperta che tutti questi trattamenti sembrano essere ugualmente efficaci a breve termine, ma che la psicoterapia e l’esercizio fisico potrebbero essere più efficaci degli antidepressivi a lungo termine.
Contributi dell’autore
IK ha scritto l’articolo.
Dichiarazione di conflitto di interessi
L’autore dichiara che la ricerca è stata condotta in assenza di relazioni commerciali o finanziarie che potrebbero essere interpretate come un potenziale conflitto di interessi.
Riferimenti
- Kirsch I. The emperor’s new drugs: exploding the antidepressant myth. New York: basic books (2010).
- Kirsch I, Deacon BJ, Huedo-Medina TB, Scoboria A, Moore TJ, Johnson BT. Initial severity and antidepressant benefits: a meta-analysis of data submitted to the Food and Drug Administration. PLoS Med (2008) 5. doi: 10.1371/ journal.pmed.0050045
- Kirsch I, Moore TJ, Scoboria A, Nicholls SS. The emperor’s new drugs: an analysis of antidepressant medication data submitted to the U.S. Food and Drug Administration. Prev Treat (2002) 5(1):23. Retrieved from http:// ezproxy.lib.uconn.edu/login?url=http://search.ebscohost.com/login. aspx?direct=true&db=pdh&AN=pre-5-1-23a&site=ehost-liveirving. kirsch{{{at}}}uconn.edu. doi: 10.1037/1522-3736.5.1.523a
- Kirsch I, Sapirstein G. Listening to Prozac but hearing placebo: a meta- analysis of antidepressant medication. In: Kirsch I, editor. How expectancies shape experience. American Psychological Association (1999). p. 303–20. doi: 10.1037/10332-012
- Ioannidis JPA. Contradicted and initially stronger effects in highly cited clinical research. JAMA (2005) 294(2):218–28. doi: 10.1001/jama.294.2.218
- Open science collaboration. Estimating the reproducibility of psychological science. Science (2015) 349(6251):aac4716. Retrieved from http://science. sciencemag.org/content/349/6251/aac4716.abstract. doi: 10.1126/science. aac4716
- Cipriani A, Furukawa TA, Salanti G, Chaimani A, Atkinson LZ, Ogawa Y, et al. Comparative efficacy and acceptability of 21 antidepressant drugs for the acute treatment of adults with major depressive disorder: a systematic review and network meta-analysis. Lancet (2018) 391(10128):1357–66. doi: 10.1016/S0140-6736(17)32802-7
- Fountoulakis KN, Möller HJ. Efficacy of antidepressants: a re-analysis and re-interpretation of the Kirsch data. Int J Neuro-Psychopharmacol (2011) 14(3):405. doi: 10.1017/S1461145710000957
- Fournier JC, DeRubeis RJ, Hollon SD, Dimidjian S, Amsterdam JD, Shelton RC, et al. Antidepressant drug effects and depression severity: a patient-level meta- analysis. J Am Med Assoc (2010) 303(1):47–53. doi: 10.1001/jama.2009.1943
- Furukawa TA, Maruo K, Noma H, Tanaka S, Imai H, Shinohara K, et al. Initial severity of major depression and efficacy of new generation antidepressants: individual participant data meta-analysis. Acta Psychiatr Scand (2018) 137(6):450–8. doi: 10.1111/acps.12886
- Gibbons RD, Hur K, Brown CH, Davis JM, Mann JJ. Benefits from antidepressants: synthesis of 6-week patient-level outcomes from double-blind placebo-controlled randomized trials of fluoxetine and venlafaxine. Arch Gen Psychiatry (2012) 69(6):572–9. doi: 10.1001/ archgenpsychiatry.2011.2044
- Jakobsen JC, Katakam KK, Schou A, Hellmuth SG, Stallknecht SE, Leth- Møller K, et al. Selective serotonin reuptake inhibitors versus placebo in patients with major depressive disorder. A systematic review with meta- analysis and trial sequential analysis. BMC Psychiatry (2017) 17(1):58. doi: 10.1186/s12888-016-1173-2
- Khin NA, Chen YF, Yang Y, Yang P, Laughren TP. Exploratory analyses of efficacy data from major depressive disorder trials submitted to the US Food and Drug Administration in support of new drug applications. J Clin Psychiatry (2011) 72(4):464. doi: 10.4088/JCP.10m06191
- NICE. Depression: management of depression in primary and secondary care. Clinical practice guideline No 23. (2004).
- Stone M, Kalaria S, Richardville K, Miller B. Components and trends in treatment effects in randomized placebo-controlled trials in major depressive disorder from 1979 to 2016. Paper presented at the American Society of Clinical Psychopharmacology, Miami (2018).
- Turner EH, Matthews AM, Linardatos E, Tell RA, Rosenthal R. Selective publication of antidepressant trials and its influence on apparent efficacy. N Engl J Med (2008) 358:252–60. doi: 10.1056/NEJMsa065779
- Cohen J. A power primer. Psychol Bull (1992) 112(1):155–9. doi: 10.1037// 0033-2909.112.1.155
- Sugarman MA, Loree AM, Baltes BB, Grekin ER, Kirsch I. The efficacy of paroxetine and placebo in treating anxiety and depression: a meta-analysis of change on the hamilton rating scales. PLoS One (2014) 9(8):e106337. doi: 10.1371/journal.pone.0106337
- Harris G. Maker of Paxil to release all trial results. N Y Times (2004).
- Roest AM, de Jonge P, Williams CD, de Vries Y, Schoevers RA, Turner EH. Reporting bias in clinical trials investigating the efficacy of second- generation antidepressants in the treatment of anxiety disorders: a report of 2 meta-analyses. JAMA Psychiatry (2015) 72(5):500–10. doi: 10.1001/ jamapsychiatry.2015.15
- Sugarman MA, Kirsch I, Huppert JD. Obsessive-compulsive disorder has a reduced placebo (and antidepressant) response compared to other anxiety disorders: a meta-analysis. J Affect Disord (2017) 218(Supplement C):217–26. Retrieved from http://www.sciencedirect.com/science/article/pii/S01650327 17303051. doi: 10.1016/j.jad.2017.04.068
- Faria V, Gingnell M, Hoppe JM, Hjorth O, Alaie I, Frick A, et al. Do You Believe It? Verbal suggestions influence the clinical and neural effects of escitalopram in social anxiety disorder: a randomized trial. EBioMedicine (2017) 179–88. doi: 10.1016/j.ebiom.2017.09.031
- Turner EH, Rosenthal R. Efficacy of antidepressants. BMJ (2008) 336(7643):516–7. Retrieved from http://www.bmj.com/content/336/7643/516.abstract. doi: 10.1136/ bmj.39510.531597.80
- Moncrieff J, Kirsch I. Empirically derived criteria cast doubt on the clinical significance of antidepressant-placebo differences. Contemp Clin Trials (2015) 43:60–2.
- Leucht S, Fennema H, Engel R, Kaspers–Janssen M, Lepping P, Szegedi A. What does the HAMD mean? J Affect Disord (2013) 148(2–3):243–8. Retrieved from http://www.sciencedirect.com/science/article/pii/S0165032712008348. doi: 10.1016/j.jad.2012.12.001
- Stahl SM, Greenberg GD. Placebo response rate is ruining drug development in psychiatry: why is this happening and what can we do about it? Acta Psychiatr Scand (2019) 139(2):105–7. doi: 10.1111/acps.13000
- Walsh BT, Seidman SN, Sysko R, Gould M. Placebo response in studies of major depression: Variable, substantial, and growing. JAMA (2002) 287(14):1840–7. Retrieved from http://ezproxy.lib.uconn.edu/login?url= http://search.ebscohost.com/login.aspx?direct=true&db=psyh&AN=2002- 12736-006&site=ehost-live. doi: 10.1001/jama.287.14.1840
- Fisher S, Lipman RS, Uhlenhuth E, Rickels K, Park LC. Drug effects and initial severity of symptomatology. Psychopharmacologia (1965) 7(1):57–60. doi: 10.1007/BF00404165
- Evers AWM, Colloca L, Blease C, Annoni M, Atlas LY, Benedetti F, et al. Implications of placebo and nocebo effects for clinical practice: expert consensus. Psychother Psychosomatics (2018) 87(4):204–10. doi: 10.1159/000490354
- Leuchter AF, Hunter AM, Tartter M, Cook IA. Role of pill-taking, expectation and therapeutic alliance in the placebo response in clinical trials for major depression. Br J Psychiatry (2014) 443–9. Retrieved from http://bjp.rcpsych. org/content/early/2014/08/27/bjp.bp.113.140343.abstract. doi: 10.1192/ bjp.bp.113.140343
- Papakostas GI, Fava M. Does the probability of receiving placebo influence clinical trial outcome? A meta-regression of double-blind, randomized clinical trials in MDD. Eur Neuropsychopharmacol (2009) 19:34–40. doi: 10.1016/j.euroneuro.2008.08.009
- Rutherford BR, Sneed JR, Roose SP. Does study design influence outcome? Psychother Psychosomatics (2009) 78(3):172–81. doi: 10.1159/000209348
- Rutherford BR, Wall MM, Brown PJ, Choo T-H, Wager TD, Peterson BS, et al. Patient expectancy as a mediator of placebo effects in antidepressant clinical trials. Am J Psychiatry (2017) 174:135–42. doi: 10.1176/appi. ajp.2016.16020225
- Sinyor M, Levitt AJ, Cheung AH, Schaffer A, Kiss A, Dowlati Y, et al. Does inclusion of a placebo arm influence response to active antidepressant treatment in randomized controlled trials? Results from pooled and meta- analyses. J Clin.Psychiatry (2010) 71:270–9. doi: 10.4088/JCP.08r04516blu
- Sneed JR, Rutherford BR, Rindskopf D, Lane DT, Sackeim HA, Roose SP. Design makes a difference: a meta-analysis of antidepressant response rates in placebo-controlled versus comparator trials in late-life depression. Am J Geriatr Psychiatry (2008) 16(1):65–73. doi: 10.1097/JGP.0b013e3181256b1d
- Rief W, Glombiewski JA. The hidden effects of blinded, placebo-controlled randomized trials: an experimental investigation. Pain (2012) 153(12):2473– 7. doi: 10.1016/j.pain.2012.09.007
- Rabkin JG, Markowitz JS, Stewart JW, McGrath PJ, Harrison W, Quitkin FM, et al. How blind is blind? Assessment of patient and doctor medication guesses in a placebo-controlled trial of imipramine and phenelzine. Psychiatry Res (1986) 19:75–86. doi: 10.1016/0165-1781(86)90094-6
- Chen JA, Papakostas GI, Youn S, Baer L, Clain AJ, Fava M, et al. Association between patient beliefs regarding assigned treatment and clinical response: reanalysis of data from the hypericum depression trial study group. J Clin Psychiatry (2011) 72(12):1669–76. doi: 10.4088/JCP.10m06453
- Chen JA, Vijapura S, Papakostas GI, Parkin SR, Kim DJH, Cusin C, et al. Association between physician beliefs regarding assigned treatment and clinical response: re-analysis of data from the hypericum depression trial study group. Asian J Psychiatry (2015) 13:23–9. Retrieved from http://www. sciencedirect.com/science/article/pii/S1876201814002810. doi: 10.1016/j. ajp.2014.12.002
- Hrobjartsson A, Emanuelsson F, Skou Thomsen AS, Hilden J, Brorson S. Bias due to lack of patient blinding in clinical trials. A systematic review of trials randomizing patients to blind and nonblind sub-studies. Int J Epidemiol (2014) 43:1272–83. doi: 10.1093/ije/dyu115
- Margraf J, Ehlers A, Roth WT, Clark DB, Sheikh J, Agras WS, et al. How blind are double-blind studies? J Consult Clin Psychol (1991) 59(1):184–7. doi: 10.1037//0022-006X.59.1.184
- Baethge C, Assall OP, Baldessarini RJ. Systematic review of blinding assessment in randomized controlled trials in schizophrenia and affective disorders 2000- 2010. Psychother Psychosomatics (2013) 82(3):152–60. doi: 10.1159/000346144
- Greenberg RP, Fisher S. Examining antidepressant effectiveness: findings, ambiguities, and some vexing puzzles. In: Fisher S, Greenberg RP, editors. The limits of biological treatments for psychological distress: comparisons with psychotherapy and placebo. Hillsdale, NJ: Lawrence Erlbaum (1989). p. 1–37.
- Oronowicz-Jaśkowiak W, Bąbel P. Twenty years after ‘listening to prozac but hearing placebo’. Do we hear placebo even louder? Health Psychol Rep (2019) 7(1):1–8. doi: 10.5114/hpr.2019.83383
- Philipp M, Kohnen R, Hiller KO. Hypericum extract versus imipramine or placebo in patients with moderate depression: randomised multicentre study of treatment for eight weeks. Br Med J (1999) 319:1534–9. doi: 10.1136/ bmj.319.7224.1534
- Ashar YK, Cohen ZD, Chang LJ, Wager TD, Dimidjian S (2015). Side effects or main effects? Side effects predict treatment response in ADM and placebo treatment of MDD. paper presented at the association for behavioral and cognitive therapy, chicagno.
- Barth M, Kriston L, Klostermann S, Barbui C, Cipriani A, Linde K. Efficacy of selective serotonin reuptake inhibitors and adverse events: meta-regression and mediation analysis of placebo-controlled trials. Br J Psychiatry (2016) 208(2):114–9. Retrieved from http://bjp.rcpsych.org/content/bjprcpsych/208/2/114.full.pdf. doi: 10.1192/bjp.bp.114.150136
- Greenberg RP, Bornstein RF, Zborowski MJ, Fisher S, Greenberg MD. A meta-analysis of fluoxetine outcome in the treatment of depression. J Nerv Ment Dis (1994) 182:547–51. doi: 10.1097/00005053-199410000-00003
- Laferton JAC, Vijapura S, Baer L, Clain AJ, Cooper A, Papakostas G, et al. Mechanisms of perceived treatment assignment and subsequent expectancy effects in a double blind placebo controlled RCT of major depression. Front Psychiatry (2018) 9:424. Retrieved from http://www.ncbi.nlm.nih.gov/pmc/ articles/PMC6137256/. doi: 10.3389/fpsyt.2018.00424
- Max MB, Schafer SC, Culnane M, Dubner R, Gracely RH. Association of pain relief with drug side effects in postherpetic neuralgia: a single-dose study of clonidine, codeine, ibuprofen, and placebo. Clin Pharmacol Ther (1988) 43(4):363–71. doi: 10.1038/clpt.1988.44
- Shah E, Triantafyllou K, Hana A, Pimentel M. Adverse events appear to unblind clinical trials in irritable bowel syndrome. Neurogastroenterol Motil (2014) 26(4):482–8. doi: 10.1111/nmo.12289
- Moncrieff J. The myth of the chemical cure. Basingstoke: Palgrave Macmillan (2008). doi: 10.1057/9780230589445
- Hunter AM, Cook I, Tartter M, Sharma S, Disse G, Leuchter A. Antidepressant treatment history and drug-placebo separation in a placebo-controlled trial in major depressive disorder. Psychopharmacology (2015) 232(20):3833–40. doi: 10.1007/s00213-015-4047-2
- Hunter AM, Cook IA, Leuchter AF. Impact of antidepressant treatment history on clinical outcomes in placebo and medication treatment of major depression. J Clin Psychopharmacol (2010) 30(6):748–51. doi: 10.1097/JCP. 0b013e3181faa474
- Andrews PW, Thomson JA, Amstadter A, Neale MC. Primum non nocere: an evolutionary analysis of whether antidepressants do more harm than good. Front Psychol (2012) 3. Retrieved from http://www.frontiersin.org/ Journal/Abstract.aspx?s=413&name=evolutionary_psychology&ART_ DOI=10.3389/fpsyg.2012.00117. doi: 10.3389/fpsyg.2012.00117
- Braun C, Bschor T, Franklin J, Baethge C. Suicides and suicide attempts during long-term treatment with antidepressants: a meta-analysis of 29 placebo-controlled studies including 6,934 patients with major depressive disorder. Psychother Psychosomatics (2016) 85(3):171–9. doi: 10.1159/000442293
- Coupland C, Dhiman P, Morriss R, Arthur A, Barton G, Hippisley-Cox J. Antidepressant use and risk of adverse outcomes in older people: population based cohort study. BMJ (2011) 343. doi: 10.1136/bmj.d4551
- Fava GA, Benasi G, Lucente M, Offidani E, Cosci F, Guidi J. Withdrawal symptoms after serotonin-noradrenaline reuptake inhibitor discontinuation: systematic review. Psychother Psychosomatics (2018) 87(4):195–203. doi: 10.1159/000491524
- Maslej MM, Bolker BM, Russell MJ, Eaton K, Durisko Z, Hollon SD, et al. The mortality and myocardial effects of antidepressants are moderated by preexisting cardiovascular disease: a meta-analysis. Psychother Psychosomatics (2017) 86(5):268–82. doi: 10.1159/000477940
- Molero Y, Lichtenstein P, Zetterqvist J, Gumpert CH, Fazel S. Selective serotonin reuptake inhibitors and violent crime: a cohort study. PLoS Med (2015) 12(9):e1001875. doi: 10.1371/journal.pmed.1001875
- Stone MB. In Search of a Pony. Med Care (2018) 56(5):375–81. doi: 10.1097/ MLR.0000000000000895
- Yuet WC, Derasari D, Sivoravong J, Mason D, Jann M. Selective serotonin reuptake inhibitor use and risk of gastrointestinal and intracranial bleeding. J Am Osteopathic Assoc (2019) 119(2):102–11. doi: 10.7556/jaoa.2019.016
- Charlesworth JE, Petkovic G, Kelley JM, Hunter M, Onakpoya I, Roberts N, et al. Effects of placebos without deception compared with no treatment: a systematic review and meta-analysis. J Evidence-Based Med (2017) 10(2):97– 107. doi: 10.1111/jebm.12251
- Locher C, Frey Nascimento A, Kirsch I, Kossowsky J, Meyer A, Gaab J. Is the rationale more important than deception? A randomized controlled trial of open-label placebo analgesia. Pain (2017) 158(12):2320–8. Retrieved from http://journals.lww.com/pain/Fulltext/2017/12000/Is_the_rationale_more_ important_than_deception A.7.aspx. doi: 10.1097/j.pain.0000000000001012
- Kelley JM, Kaptchuk TJ, Cusin C, Lipkin S, Fava M. Open-label placebo for major depressive disorder: a pilot randomized controlled trial. Psychother Psychosom (2012) 81:312–4.
- Appleton KM, Sallis HM, Perry R, Ness AR, Churchill R. Omega-3 fatty acids for depression in adults. Cochrane Database Syst Rev (2015) 11. doi: 10.1002/14651858.CD004692.pub4
- Khan A, Faucett J, Lichtenberg P, Kirsch I, Brown WA. A Systematic review of comparative efficacy of treatments and controls for depression. PLoS One (2012) 7(7):e41778. doi: 10.1371/journal.pone.0041778
- Macías-Cortés E, Llanes-González L, Aguilar-Faisal L, Asbun-Bojalil J. Individualized homeopathic treatment and fluoxetine for moderate to severe depression in peri-and postmenopausal women (HOMDEP-MENOP study): a randomized, double-dummy, double-blind, placebo-controlled trial. PLoS One (2015) 10(3):e0118440. doi: 10.1371/journal.pone.0118440
- Zou L, Yeung A, Li C, Wei G-X, Chen K, Kinser P, et al. Effects of meditative movements on major depressive disorder: a systematic review and meta- analysis of randomized controlled trials. J Clin Med (2018) 7(8):195. doi: 10.3390/jcm7080195
- Cuijpers P, Hollon SD, van Straten A, Bockting C, Berking M, Andersson G. Does cognitive behaviour therapy have an enduring effect that is superior to keeping patients on continuation pharmacotherapy? A meta-analysis. BMJ Open (2013) 3(4):e002542. Retrieved from http://bmjopen.bmj.com/ content/3/4/e002542.abstract. doi: 10.1136/bmjopen-2012-002542
- Shea MT, Elkin I, Imber SD, Sotsky SM, Watkins JT, Collins JF, et al. Course of depressive symptoms over follow-up: findings from the National Institute of Mental Health Treatment of Depression Collaborative Research Program. Arch Gen Psychiatry (1992) 49(10):782–7. doi: 10.1001/archpsyc.1992.018201 00026006
- Hollon SD, Cohen ZD, Singla DR, Andrews PW. Recent developments in the treatment of depression. Behavior Ther (2019) 50(2):257–69. Retrieved from http://www.sciencedirect.com/science/article/pii/S000578941930005X. doi: 10.1016/j.beth.2019.01.002
- Andrews PW, Kornstein S, Halberstadt L, Gardner C, Neale MC. Blue again: Perturbational effects of antidepressants suggest monoaminergic homeostasis in major depression. Front Psychol (2011) 2. Retrieved from http://www.frontiersin.org/Journal/Abstract.aspx?s=413&name=evolution arypsychology&ART_DOI=10.3389/fpsyg.2011.00159. doi: 10.3389/fpsyg. 2011.00159
- Barlow DH, Gorman JM, Shear MK, Woods SW. cognitive-behavioral therapy, imipramine, or their combination for panic disorder. JAMA (2000) 283:2529–36. doi: 10.1001/jama.283.19.2529
- Babyak MA, Blumenthal JA, Herman S, Khatri P, Doraiswamy PM, Moore KA, et al. Exercise treatment for major depression: maintenance of therapeutic benefit at 10 months. Psychosomatic Med (2000) 62:633–8. doi: 10.1097/00006842-200009000-00006
- Agar MR, Lawlor PG, Quinn S, Draper B, Caplan GA, Rowett D, et al. Efficacy of oral risperidone, haloperidol, or placebo for symptoms of delirium among patients in palliative care: a randomized clinical trial. JAMA Internal Med (2017) 177(1):34–42. doi: 10.1001/jamainternmed.2016.7491
- Tyrer P, Oliver-Africano PC, Ahmed Z, Bouras N, Cooray S, Deb S, et al. Risperidone, haloperidol, and placebo in the treatment of aggressive challenging behaviour in patients with intellectual disability: a randomised controlled trial. Lancet (2008) 371:57–63. doi: 10.1016/S0140-6736(08) 60072-0
- Roman-Blas JA, Castañeda S, Sánchez-Pernaute O, Largo R, Herrero- Beaumont G, Group C. G. C. T. S., et al. Combined treatment with chondroitin sulfate and glucosamine sulfate shows no superiority over placebo for reduction of joint pain and functional impairment in patients with knee osteoarthritis: a six-month multicenter, randomized, double-blind, placebo-controlled clinical trial. Arthritis Rheumatol (2017) 69(1):77–85. doi: 10.1002/art.39819
- Sarris J, Byrne GJ, Stough C, Bousman C, Mischoulon D, Murphy J, et al. Nutraceuticals for major depressive disorder- more is not merrier: an 8-week double-blind, randomised, controlled trial. J Affect Disord (2019) 245:1007–15. Retrieved from http://www.sciencedirect.com/science/article/ pii/S0165032718314113. doi: 10.1016/j.jad.2018.