Giovanni A. Fava
Pubblicato su Therapeutic Advances in Psychopharmacology 2020
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
Astratto
Negli ultimi anni c’è stato un ampio dibattito sui farmaci antidepressivi. Il trattamento farmacologico continuato con farmaci antidepressivi può stimolare processi che contrastano con gli effetti acuti iniziali di un farmaco. Il modello oppositivo di tolleranza può spiegare la perdita di efficacia del trattamento durante il trattamento di mantenimento e il fatto che alcuni effetti collaterali tendono a manifestarsi solo dopo un certo tempo. Questi processi possono anche indirizzare la malattia verso un decorso che non risponde al trattamento, comprese manifestazioni di disturbo bipolare o reazioni paradossali. Al termine del trattamento farmacologico, i processi oppositivi non incontrano più resistenza, con conseguente potenziale insorgenza di nuovi sintomi di astinenza, persistenti disturbi post-astinenza, ipomania e resistenza al trattamento se viene ripristinato. In tutti questi casi, i farmaci antidepressivi possono costituire una forma di comorbilità iatrogena, che aumenta la cronicità e la vulnerabilità agli episodi depressivi.
I farmaci antidepressivi sono farmaci essenziali per il trattamento degli episodi depressivi maggiori. Tuttavia, è meno probabile che forniscano protezione per la prevenzione delle ricadute. Le attuali pratiche di prescrizione devono essere riformulate alla luce della considerazione delle vulnerabilità e degli effetti negativi del trattamento. Il modello di tolleranza oppositivo fornisce un quadro concettuale per valutare tutti questi elementi nel singolo caso. Il modello non sembra applicarsi a tutti i pazienti sottoposti a trattamento con AD, ma solo ad una parte di essi. Lo studio delle variabili associate a tale evento in alcuni pazienti e non in altri sarebbe uno dei compiti più importanti dell’attuale ricerca terapeutica. Gli attuali sistemi diagnostici in psichiatria non considerano le componenti iatrogene della psicopatologia e possono essere applicati solo a pazienti che sono privi di droghe. Sono adatti per un paziente che non esiste più: la maggior parte dei casi che si osservano nella pratica clinica psichiatrica riceve farmaci psicotropi e tale trattamento è probabile che influisca sulla prognosi e sulle scelte terapeutiche.
Introduzione
Nel 1994, ho sollevato la questione se i farmaci antidepressivi (AD) potessero aumentare la cronicità nei disturbi dell’umore e d’ansia. 1 Successivamente è stata presentata una considerazione farmacodinamica dei fenomeni clinici legati ai farmaci antidepressivi. 2 Secondo il modello oppositivo di tolleranza, il trattamento farmacologico continuato può stimolare processi che contrastano gli effetti acuti iniziali di un farmaco. 2 È ampiamente riconosciuto che le risposte adattative, come i cambiamenti del recettore 5HT2A o il legame del recettore 5HT4, che sono diverse dalle risposte iniziali, mediano le azioni terapeutiche a 3-4 settimane. 3 – 6
È quindi anche concepibile che ulteriori cambiamenti adattativi possano verificarsi in un momento successivo e quando l’AD viene interrotto. Tali cambiamenti adattativi possono avvenire attraverso l’attività dell’autorecettore 5HT1A e/o essere associati alla modulazione allosterica della proteina trasportatrice della serotonina, che è stata recentemente rilevata con inibitori selettivi della ricaptazione della serotonina (SSRI) come paroxetina ed escitalopram. 7 Vari polimorfismi genetici nei recettori della serotonina, inclusi i sottotipi 5HT1A, 5HT1B e 5HT2, possono avere un ruolo nel determinare la misura in cui si verificano processi opposti e compensativi in risposta agli effetti iniziali dei farmaci. 8
Tuttavia, anche fattori come la durata e il tipo di trattamento, la storia precedente di esposizione all’AD e le manipolazioni farmacologiche come le strategie di aumento e cambio, possono comportare implicazioni molto profonde. 9 La durata di tali cambiamenti può essere variabile: se persistenti, i cambiamenti possono causare modificazioni sfavorevoli della traiettoria, delle caratteristiche e della reattività al successivo trattamento della malattia. 9
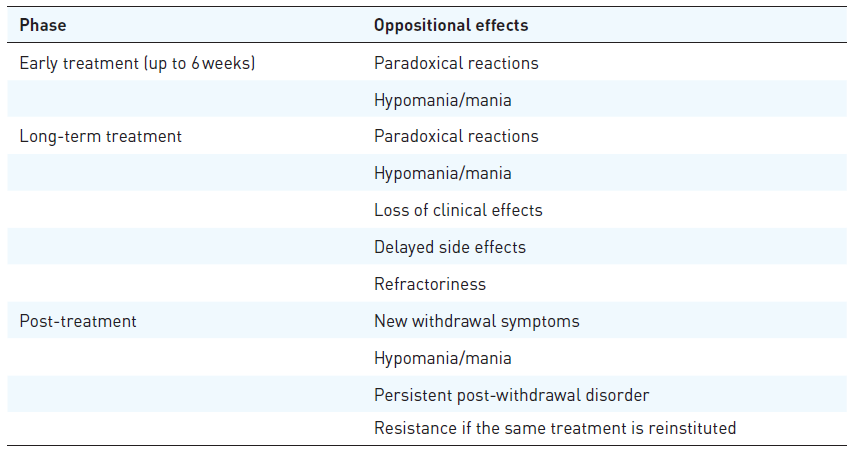
Il modello oppositivo di tolleranza 2 , 9 , 10 ha tre diverse fasi di applicazione: trattamento precoce, trattamento a lungo termine e fase successiva all’interruzione dell’antidepressivo ( Tabella 1 ).
Nella fase iniziale del trattamento (fino a 6 settimane) i processi oppositivi possono causare ipomania/mania o reazioni paradossali come l’approfondimento della depressione. Con la terapia a lungo termine, possono quindi comparire una perdita di efficacia del trattamento e alcuni effetti collaterali (come aumento dell’appetito e aumento di peso), che non si sono verificati inizialmente. 9 Questi meccanismi possono anche portare la malattia a un decorso che non risponde al trattamento. Al termine del trattamento farmacologico, i processi oppositivi non incontrano più resistenza, con conseguente potenziale insorgenza di nuova sintomatologia da astinenza, disturbi post-astinenza persistenti, ipomania, resistenza al trattamento se viene ripristinato.
A lungo termine, l’AD può aumentare la cronicità e la vulnerabilità ai disturbi depressivi, 2 , 9 , 10 costituendo una forma di comorbidità iatrogena. 9 Il modello è complesso e multifattoriale ed è influenzato dalla durata e dalla precedente esposizione al trattamento antidepressivo, nonché da fattori psicosociali e genetici. La durata del processo oppositivo al termine del trattamento farmacologico può essere variabile, da poche settimane a mesi o anche più a lungo. Il numero di studi clinici che affrontano problematiche legate al modello oppositivo di tolleranza è progressivamente aumentato nel corso degli anni. 9 , 10
Lo scopo di questo documento è quello di fornire una panoramica della tempestività e dell’adeguatezza clinica di questo quadro concettuale. Esaminerò criticamente le diverse espressioni di tolleranza che sono state riportate con l’uso di farmaci antidepressivi. Questa rassegna non intende essere esaustiva (si citeranno solo indagini illustrative), ma delineare le intuizioni cliniche che possono derivare da questo approccio.
I fondamenti clinici del modello di tolleranza oppositiva con trattamento antidepressivo
Sono stati documentati numerosi fenomeni clinici durante o dopo il trattamento antidepressivo (perdita di efficacia antidepressiva, resistenza, effetti paradossali, passaggio al decorso bipolare, reazioni da astinenza, refrattarietà).
Perdita di efficacia antidepressiva
Il ritorno dei sintomi depressivi durante il trattamento antidepressivo di mantenimento è stato oggetto di due recenti revisioni. 11 , 12 Il termine “tachifilassi” (la progressiva riduzione della risposta a una determinata dose di farmaco dopo somministrazione ripetuta di una sostanza farmacologicamente o fisiologicamente attiva) è stato utilizzato anche per caratterizzare la ricaduta durante il trattamento di mantenimento o il deterioramento clinico caratterizzato da sintomi come l’apatia e fatica. 11 – 13 L’uso di quest’ultimo termine è, tuttavia, discutibile, poiché la sua radice greca connota una veloce, rapida perdita di effetto; al contrario, il fenomeno aumenta con la durata del trattamento. In una meta-analisi di studi sul trattamento di mantenimento, il rischio di ricaduta è aumentato progressivamente dal 23% entro 1 anno al 34% in 2 anni e al 45% in 3 anni. 14 Di conseguenza, il termine “tachifilassi” dovrebbe essere evitato e sostituito da “perdita di effetti clinici” o “perdita di efficacia”.
Una potenziale spiegazione per la perdita di efficacia del trattamento potrebbe essere che l’AD è efficace per il trattamento dell’episodio acuto, ma non nel trattamento di mantenimento. Di conseguenza, non rappresenterebbe un’effettiva perdita degli effetti del trattamento, ma l’assenza di profilassi da AD. Questa possibilità va però contro il fatto che il fenomeno non è generalizzato, poiché coinvolge una fascia della popolazione trattata che cresce progressivamente nel tempo. 11 , 12 , 15
Una strategia clinicamente intuitiva per affrontare il problema consiste nell’aumentare il dosaggio dell’AD. In uno studio randomizzato controllato, 16 fluoxetina sono state somministrate a una dose di 20 mg al giorno o 90 mg a settimana. Circa un terzo dei pazienti ha avuto una ricaduta entro una media di 107 giorni dal trattamento di mantenimento. È stata valutata l’efficacia dell’aumento del farmaco in caso di recidiva: il 57% dei pazienti che hanno ricevuto la dose giornaliera e il 72% di quelli con la dose settimanale hanno mostrato una risposta all’aumento della dose. Un paziente su cinque che inizialmente ha risposto all’aumento della dose ha avuto una nuova ricaduta durante lo studio di 25 settimane. 16
È ipotizzabile che si sarebbero verificate più ricadute se il processo fosse continuato, come riportato nella depressione ricorrente. 17 I risultati in uno studio controllato con placebo sulla duloxetina erano abbastanza simili. 18 Tuttavia, in due indagini pilota controllate, 19 , 20 la psicoterapia (in un caso una forma modificata di terapia cognitivo-comportamentale e in un altro la terapia familiare) senza modificare il regime farmacologico è risultata significativamente più efficace dell’aumento della dose nel produrre una remissione persistente nei pazienti depressi che ha sperimentato una perdita dell’effetto clinico durante il trattamento con AD.
Resistenza ai farmaci antidepressivi
Il termine “resistenza” è generalmente applicato sia alla malattia depressiva (episodio che non risponde ai farmaci o alla psicoterapia) sia alla mancata risposta a un trattamento farmacologico precedentemente efficace quando lo stesso farmaco viene ripreso dopo un periodo di astinenza da farmaci. Il primo uso è il più comune, ma il secondo si verifica anche in un numero considerevole di casi. 21 In una recente revisione sistematica sulla mancanza di risposta alla ri-sfida, 22 la gamma dei fallimenti di risposta era ampia (tra il 4,9% e il 42,9% negli studi). In un ampio studio osservazionale, 23 in un quarto dei casi è stata riscontrata la mancata risposta allo stesso farmaco utilizzato in un episodio precedente.
È stato riscontrato che l’uso precedente dell’AD è correlato a una resistenza all’AD che differiva da quelle somministrate durante i primi studi. 24 , 25 In un’indagine su 122 pazienti che, dopo aver inizialmente risposto alla fluoxetina, erano stati assegnati al placebo, 26 è stata esaminata la resistenza. Circa la metà dei pazienti ha avuto una ricaduta. Dopo la ripresa della fluoxetina, il 38% dei pazienti depressi non ha risposto affatto o ha mostrato una risposta iniziale seguita da una ricaduta. 26
I dati disponibili indicano quindi che, quando il trattamento farmacologico viene ripristinato, il paziente potrebbe non rispondere allo stesso antidepressivo che inizialmente ha migliorato i sintomi depressivi. Nei pazienti che rispondono allo stesso AD utilizzato nell’episodio precedente, può quindi verificarsi una perdita dell’effetto terapeutico. 23 Ciò suggerisce che la perdita di efficacia e la resistenza al trattamento possono essere collegate e avere un meccanismo sottostante comune.
La mancanza di differenziazione tra un episodio di malattia che non risponde a un determinato trattamento e la mancanza di risposta a una terapia precedentemente efficace può generare confusione. Tale confusione è aumentata dal presupposto che il trattamento fosse giusto in primo luogo e la mancata risposta è attribuita alle caratteristiche dei pazienti. 21 “Resistenza al trattamento” richiede quindi il cambio e l’aumento di AD. Tuttavia, queste strategie terapeutiche possono innescare una “iatrogenesi a cascata”, invece di riconsiderare l’intero processo 21: il trattamento era appropriato in primo luogo?
L’esito clinico è il risultato di diverse variabili interagenti: condizioni di vita, caratteristiche del paziente, caratteristiche della malattia e precedenti esperienze terapeutiche, autogestione (il grado di collaborazione del paziente in termini di comportamento e stile di vita) e impostazione del trattamento (ad es. atteggiamento e attenzione del medico , comportamento di malattia). 21 Alcuni di questi fattori possono essere terapeutici, mentre altri fattori possono essere contro-terapeutici. In alcuni pazienti la combinazione interattiva di variabili terapeutiche può portare a un miglioramento clinico; negli altri casi, il risultato netto non produrrà alcun effetto; in un altro segmento della popolazione clinica, può causare un peggioramento della condizione.
Effetti paradossali
Nel 1968 Di Mascio et al. ha studiato gli effetti dell’imipramina su individui molto eterogenei per quanto riguarda i livelli di depressione, utilizzando una procedura in doppio cieco controllata con placebo. 27 L’imipramina ha indotto un aumento della depressione nei soggetti con i punteggi più bassi di depressione. Questo primo studio pilota ha suggerito la possibilità che, quando i sintomi depressivi sono minimi, i farmaci antidepressivi possano fare più male che bene. Di conseguenza, l’uso dell’AD può essere associato alla comparsa di nuovi sintomi e all’esacerbazione del quadro clinico di base (effetti paradossali). Il miglioramento può derivare dalla sospensione dell’antidepressivo. 10
Il verificarsi di effetti paradossali è stato riportato in indagini in doppio cieco controllate con placebo che riguardavano fluoxetina e sertralina. 28 , 29 In effetti, il concetto di disforia tardiva indotta da antidepressivi indica il fatto che la sintomatologia può essere invertita riducendo gradualmente o interrompendo l’AD. 30
Durante il trattamento del disturbo di panico con fluvoxamina, 31 è stata segnalata l’insorgenza di sintomi depressivi in 7 su 80 pazienti (9%). È di notevole interesse il fatto che questi pazienti non avessero una storia passata o attuale di depressione prima della terapia con fluvoxamina. I sintomi sono migliorati quando la fluvoxamina è stata interrotta e gli antidepressivi triciclici (TCA) o il clonazepam sono stati sostituiti come trattamento. I sintomi depressivi sono ricomparsi di nuovo quando è stata somministrata la fluoxetina. 28 Osservazioni simili sono state fatte con l’uso del TCA nei disturbi d’ansia. 32 Raja ha descritto nove pazienti che hanno avuto una buona risposta iniziale al trattamento con AD. 33 Tuttavia, tale risposta è stata seguita da perdita di efficacia, resistenza e peggioramento con il trattamento successivo. Queste manifestazioni oppositive sembravano essere strettamente connesse e parte della stessa sindrome.
Passaggio al disturbo bipolare
Il trattamento con AD è stato associato a mania o altre forme di attivazione comportamentale eccessiva. 34 Queste manifestazioni possono semplicemente rivelare un disturbo bipolare che non era stato riconosciuto o possono essere prevalentemente iatrogeni, poiché possono verificarsi anche in pazienti che non hanno alcuna storia precedente o predisposizione genetica alla malattia bipolare. All’inizio degli anni ’80, Koukopulos et al. osservato come il trattamento con AD può cambiare il decorso dalla malattia unipolare a quella bipolare. 35 Hanno suggerito che la mania indotta dagli antidepressivi potrebbe non essere semplicemente un fenomeno temporaneo e completamente reversibile quando il trattamento viene interrotto, ma che l’AD innesca complessi meccanismi biochimici di deterioramento permanente della malattia. Bader e Dunner hanno sottolineato l’associazione tra mania indotta da antidepressivi e depressione resistente al trattamento in pazienti che non avevano una storia familiare di disturbo bipolare. 36
Una revisione sistematica e una meta-analisi hanno esplorato l’ipomania, la mania e l’attivazione comportamentale di bambini e adolescenti durante il trattamento con AD. 37 Ha rivelato che i tassi di attivazione eccessiva dell’eccitazione con gli antidepressivi erano significativamente più alti sia nell’ansia (13,8%) che nella depressione (9,8%) rispetto ai placebo (5,2 contro 1,1%, rispettivamente). 37 Di conseguenza, l’attivazione comportamentale, l’ipomania e la mania sono un rischio consistente indipendentemente dalla storia individuale o familiare di malattia bipolare. Tale rischio è in contrasto con l’uso clinico diffuso di antidepressivi nei disturbi d’ansia, in particolare nei pazienti più giovani.
Nonostante la smentita iniziale, l’idea che l’AD possa peggiorare il decorso del disturbo bipolare ha ottenuto ampia diffusione. 34 AD, tuttavia, può indurre un’accelerazione dell’episodio anche nella depressione unipolare. Goodwin ha illustrato il suo potenziale meccanismo: “Se la sequenza naturale della malattia unipolare ricorrente va dalla depressione alla guarigione e poi eventualmente all’episodio successivo, i trattamenti che accelerano il recupero della depressione indice potrebbero anche accelerare l’insorgenza dell’episodio successivo” (p. 43). 38
Sintomi da astinenza
I sintomi di astinenza dopo l’interruzione del trattamento antidepressivo sono stati presto riconosciuti dopo l’introduzione di questi farmaci. 39 Sono stati descritti con qualsiasi tipo di AD, ma in particolare con SSRI, venlafaxina e duloxetina. 40 – 45 In passato sono state etichettate come “sindromi da sospensione”, con l’obiettivo di evitare qualsiasi accenno al potenziale di dipendenza degli SSRI che possa influenzare il marketing. Tuttavia, questa posizione non è più sostenibile alla luce delle attuali evidenze che indicano che i fenomeni clinici riguardano sindromi da astinenza e non differiscono da quelli che si verificano con altri farmaci psicotropi. 40 – 45 Hengartner et al.ha osservato che la prima revisione sistematica sugli SSRI è apparsa solo nel 2015, 40 , 46 e la prima sugli inibitori della ricaptazione della serotonina-noradrenalina (SNRI) nel 2018, 42 dopo quasi 200 meta-analisi sull’efficacia degli antidepressivi di nuova generazione.
La sindrome da astinenza comprende un’ampia gamma di sintomi somatici (ad es. mal di testa, vertigini, sintomi simil-influenzali, nausea). 40 – 45 Possono manifestarsi anche sintomi psicologici: agitazione, ansia, attacchi di panico, disforia, irritabilità, confusione e peggioramento dell’umore. 40 , 45 I sintomi in genere iniziano entro 3 giorni dall’interruzione del trattamento antidepressivo o dall’inizio della riduzione del farmaco. I sintomi non trattati possono essere lievi e risolversi spontaneamente in 1-3 settimane; in altri casi possono persistere per mesi o addirittura anni, 40 – 45 portando a quello che è stato definito come disturbo persistente post-astinenza. 41 , 45
L’interruzione dei farmaci antidepressivi può anche innescare ipomania o mania, nonostante il trattamento concomitante di stabilizzazione dell’umore. 47 La sindrome ha un decorso molto variabile: può essere autolimitante, o può attenuarsi alla ripresa dell’AD, oppure può richiedere un trattamento antimaniacale specifico. L’aumento dell’umore può verificarsi anche con la riduzione della dose di antidepressivi, 48 e i pazienti che non hanno risposto agli stabilizzatori dell’umore in combinazione con gli antidepressivi possono migliorare con l’interruzione degli antidepressivi. 49
È probabile che i sintomi da astinenza vengano fraintesi come indicazioni di ricaduta e possono portare a ricominciare il trattamento con l’AD, perpetuando il problema. 50
Refrettrietà
Il Sequenced Treatment Alternatives to Relieve Depression Study (STAR*D) ha fornito un’importante conferma del modello oppositivo di tolleranza. 51 Lo scopo originario della sperimentazione era di testare le migliori strategie farmacologiche per ottenere la remissione nella depressione maggiore. I pazienti sono entrati in un primo studio aperto di farmaci (citalopram), con un dosaggio aggressivo e una durata prolungata del trattamento. Solo il 37% dei pazienti ha raggiunto la remissione e la percentuale che ha risposto e si è mantenuta bene per un anno è stata del 15%. 51 , 52 I pazienti che non si sono ripresi dopo la prima prova del farmaco sono stati sottoposti a tre fasi sequenziali che prevedevano il cambio, l’aumento o le strategie di combinazione, sulla base delle prove esistenti.
Il tasso di remissione cumulativa dopo tutti e quattro i passaggi sequenziali era del 67%; tuttavia, quando è stata considerata la guarigione persistente (includendo anche i tassi di recidiva durante il trattamento), il tasso cumulativo era del 43%. Gli sforzi terapeutici dopo la fase uno (trattamento aperto con citalopram) hanno prodotto solo un ulteriore 6% di recupero prolungato. I tassi di remissione sono diminuiti dopo ogni fase del trattamento, nonostante il fatto che ogni fase dello studio sia stata attentamente concepita per aumentare la probabilità di risposta nei pazienti che non si erano rimessi. 51In ogni fase del trattamento sequenziale, i tassi di recidiva (mentre erano ancora in terapia) sono aumentati nei pazienti che hanno ottenuto la remissione. Inoltre, dopo ogni fase del trattamento l’intolleranza al trattamento è aumentata (come evidenziato da abbandoni per qualsiasi motivo durante le prime 4 settimane o effetti collaterali successivi).
Se interpretiamo i risultati di STAR*D alla luce del modello di tolleranza oppositiva 2 , 10 , 15 : le manipolazioni farmacologiche, sia per cambio che per aumento, possono spingere la malattia depressiva in una fase più refrattaria, caratterizzata da tassi più elevati di ricaduta durante il trattamento, inferiori remissione ai trattamenti successivi, nonché maggiore intolleranza a ulteriori trattamenti (passaggi 3 e 4). Tali tendenze sono state confermate da un altro studio: 53 maggiore era il numero di precedenti trattamenti antidepressivi, maggiore era la probabilità di una ricaduta depressiva.
È stato suggerito che la bipolarità non diagnosticata nei pazienti depressi possa essere una spiegazione della resistenza e della refrattarietà al trattamento e gli attuali sistemi diagnostici che differenziano la depressione unipolare e bipolare non riescono a riconoscere le aree intermedie. 54 , 55 Tuttavia, la bipolarità non diagnosticata può spiegare solo una parte dello spettro dei fenomeni clinici e, inavvertitamente, sposta la colpa su una diagnosi errata e su un uso scorretto dell’AD. Interruzioni ipomaniacali e maniacali del trattamento antidepressivo possono verificarsi anche con una valutazione corretta e accurata e sono solo una delle numerose manifestazioni di tolleranza. Non sorprende che tendano a raggrupparsi con altre manifestazioni (Tabella 1).
Il modello oppositivo come quadro clinico concettuale
Gli eventi clinici che sono stati delineati nelle sezioni precedenti possono essere eventi sparsi che sono gli inevitabili inconvenienti delle terapie. In alternativa, possono essere concettualizzati sotto l’ombrello unificante del modello di tolleranza di opposizione. 2 , 10 , 15 In effetti, vi è una chiara tendenza al raggruppamento e alle sovrapposizioni nei singoli casi (p. es., insorgenza di sindromi da astinenza dopo la sospensione degli antidepressivi seguita da switch ipomaniacale; perdita dell’effetto clinico durante la terapia che si trasforma in refrattarietà al trattamento). Le decisioni cliniche relative all’applicazione delle conoscenze al singolo paziente devono essere collocate nel quadro dei potenziali benefici (la probabilità di scarsi risultati da un disturbo dell’indice se il trattamento non viene avviato), la vulnerabilità agli effetti avversi del trattamento e la reattività attesa all’opzione di trattamento. 9 Verrà illustrato come il quadro concettuale del modello oppositivo di tolleranza possa influenzare le pratiche di prescrizione nei disturbi dell’umore e d’ansia.
Trattamento dell’episodio depressivo maggiore
L’efficacia dei farmaci antidepressivi nel trattamento della depressione è stata gonfiata dalla segnalazione selettiva di studi positivi. 56 Sembrerebbe che se un paziente soffre di una grave depressione, non ci sono dubbi sul fatto che l’AD possa trarre un beneficio sostanziale dall’impiego della farmacoterapia, sebbene, ovviamente, vi sia una notevole variabilità nella risposta da paziente a paziente e recenti meta-analisi i dati hanno messo in discussione l’idea che l’entità del beneficio rispetto al placebo aumenta con la gravità della depressione. 57 Tuttavia, se sono presenti sintomi di intensità lieve o moderata, gli studi clinici indicano che i benefici possono essere minimi o non superiori al placebo, 58 mentre è probabile che i pazienti malinconici rispondano relativamente bene alla farmacoterapia. 52
La trascuratezza dei fenomeni clinici legati alla tolleranza (vulnerabilità) può indurre il clinico a sottoporre a sintomi depressivi lievi una sperimentazione con AD. Anche quando la depressione è grave, la soglia clinica fornita dai criteri diagnostici può essere abbassata dalla presenza di disturbi d’ansia; la depressione ansiosa ha meno probabilità di rispondere all’AD rispetto alla depressione non ansiosa. 59 Quando è prevedibile una scarsa reattività, i potenziali benefici che il trattamento antidepressivo può comportare sono superati dalla probabilità di vulnerabilità, che dovrebbero essere valutate caso per caso.
Devono essere considerate alternative non farmacologiche, come la terapia cognitivo-comportamentale. 60 Un’altra opzione è quella di posticipare la prescrizione di un farmaco antidepressivo e di rivedere il paziente dopo un paio di settimane se la depressione non è grave e con idee suicide. Questo può essere particolarmente importante nel contesto di una malattia medica, quando la depressione può migliorare se le condizioni mediche migliorano e/o il paziente viene dimesso dall’ospedale. 61
Trattamento a lungo termine per la prevenzione delle ricadute
Vi è un’elevata variabilità interindividuale del tempo necessario per riprendersi da un episodio depressivo. Almeno 6 mesi di trattamento farmacologico sembrano essere necessari affinché la maggior parte dei pazienti raggiunga un livello soddisfacente di remissione. 62 Questo tempo può essere ridotto a 3 mesi prima della riduzione graduale se viene impiegata la combinazione sequenziale di farmacoterapia e psicoterapia. 63 Il disegno sequenziale è un approccio intensivo in due fasi, in cui un tipo di trattamento (psicoterapia) viene impiegato per migliorare i sintomi che un altro tipo di trattamento (farmacoterapia) non è stato in grado di influenzare. Questo approccio cerca di utilizzare le strategie psicoterapeutiche in un modo che è più probabile ottenere un recupero più pervasivo affrontando la sintomatologia residua e dare un contributo specifico e sostanziale al benessere del paziente. I benefici dell’applicazione di strategie psicoterapeutiche dopo che la farmacoterapia ha prodotto i suoi effetti diventano massimi quando si ottiene l’interruzione del farmaco mediante una lenta riduzione graduale. 63
L’assunto di base del modello sequenziale è lavorare con il paziente per riconoscere e modificare le impostazioni di vita e gli atteggiamenti che favoriscono lo sviluppo della depressione. 63 Quando il modello sequenziale prevede la riduzione e l’interruzione dell’AD, presenta il vantaggio di limitare l’esposizione all’AD. 63
Il prolungamento dei trattamenti farmacologici per mantenere le risposte cliniche ottenute a breve termine è raccomandato per la prevenzione delle ricadute nella depressione. 64 L’assunto di base è che il prolungamento del trattamento che ha prodotto la remissione sia la migliore strategia per prevenire le ricadute della depressione. L’evidenza a sostegno di questa strategia, tuttavia, si basa principalmente su studi clinici in cui i pazienti rimessi sono stati randomizzati alla continuazione del farmaco o al placebo, senza alcuna differenziazione tra astinenza e recidiva. Tale ipotesi è stata recentemente contestata 65 – 68: non abbiamo modo di sapere quante delle ricadute siano state effettivamente sindromi da astinenza e post-astinenza nel gruppo che ha subito il tapering e la sospensione del farmaco. Inoltre, i pazienti con episodi depressivi multipli sperimentano un beneficio significativamente inferiore nella prevenzione delle ricadute durante la fase di mantenimento degli antidepressivi rispetto a quelli con un singolo episodio. 69
Negli studi naturalistici su pazienti trattati con SSRI, 70 , 71 più lunga era la durata del trattamento antidepressivo, maggiore era la probabilità che i pazienti si ripresentassero. In altri studi longitudinali naturalistici che hanno coinvolto tutti i tipi di AD, è stata riscontrata una maggiore incidenza e una maggiore durata di episodi di depressione maggiore in coloro che hanno utilizzato l’AD rispetto a coloro che non assumevano quei farmaci. 72 Anche se i risultati potrebbero essere stati confusi dalla possibilità che l’AD fosse prescritto ai casi più gravi e ricorrenti, l’impatto dell’AD sulla popolazione generale non è apparso favorevole. 72 Un altro inconveniente del trattamento antidepressivo a lungo termine riguarda i gravi e fastidiosi effetti collaterali che possono derivare da SSRI e SNRI, come alti tassi di disfunzione sessuale, sanguinamento (in particolare gastrointestinale), aumento di peso, rischio di frattura e osteoporosi e iponatriemia. 73
Farmaci antidepressivi nei disturbi d’ansia
Nell’ultimo decennio è stato osservato un progressivo cambiamento nel modello di prescrizione dalle benzodiazepine agli antidepressivi di seconda generazione nei disturbi d’ansia. 74 Tale cambiamento è avvenuto senza alcuna prova a sostegno. 75 In una revisione sistematica, le benzodiazepine sono state associate a un minor numero di ritiri ed eventi avversi rispetto all’AD nei disturbi d’ansia. 75 Nel disturbo di panico, accompagnato o meno da agorafobia, il trattamento con benzodiazepine è stato più efficace nel ridurre il numero di attacchi di panico rispetto ai farmaci antidepressivi. 75
Un importante stimolo nel passaggio dalle benzodiazepine agli antidepressivi nei disturbi d’ansia è stato il rischio di dipendenza dalle benzodiazepine. Tuttavia, a tempo debito dopo la loro introduzione, si sono verificati problemi più pronunciati con la maggior parte dei nuovi antidepressivi. 40 – 46 Sembrerebbe che, con entrambi i tipi di farmaci, possano derivare reazioni da astinenza e sindromi post-astinenza, nonostante il lento tapering. Tuttavia, anche se la perdita dell’effetto clinico e le reazioni paradossali possono verificarsi anche con il trattamento a lungo termine con le benzodiazepine, è improbabile che si verifichino altre vulnerabilità che sono state descritte con l’AD (resistenza, passaggio a mania o ipomania, refrattarietà) con le benzodiazepine. 45 , 76 L’uso di farmaci antidepressivi può essere giustificato quando un episodio depressivo maggiore è associato a un disturbo d’ansia. In tutti gli altri casi, il trattamento con antidepressivi dovrebbe essere attentamente considerato e dovrebbe essere limitato ai casi in cui le strategie psicoterapeutiche non sono disponibili o efficaci o le benzodiazepine non hanno fornito un sollievo adeguato. Va anche ricordato che le benzodiazepine sono risultate efficaci nella depressione ansiosa e lieve. 77
Conclusione
A 26 anni dalla formulazione di un’ipotesi ampiamente speculativa riguardante gli effetti iatrogeni dell’AD, 1 le prove che ho esaminato indicano che l’uso di questi farmaci può avere il potenziale per peggiorare l’esito a lungo termine dei disturbi dell’umore e d’ansia in singoli casi. Meccanismi simili, inclusi nel concetto di psicosi da supersensibilità, possono applicarsi all’uso di antipsicotici nella schizofrenia e nei disturbi dell’umore. 78 , 79 Il modello oppositivo di tolleranza è anche coerente con l’uso di farmaci psicotropi come droghe ricreative. 80
Se prendiamo in considerazione i potenziali benefici, la probabilità di reattività e i potenziali eventi avversi e vulnerabilità implicati dai meccanismi di opposizione, saremmo propensi a indirizzare l’applicazione dell’AD solo ai casi più gravi e persistenti di depressione per il più breve tempo possibile ed evitarne l’utilizzo nei disturbi d’ansia (a meno che non sia presente un disturbo depressivo maggiore o che altri trattamenti siano stati inefficaci). 81
L’AD si è rivelato efficace nel trattamento della depressione grave, ma la migliore tollerabilità dell’AD più recente ha ampliato le loro indicazioni originali. Il loro uso è stato prolungato per il mantenimento e la prevenzione delle ricadute della depressione ed è stato esteso al trattamento a lungo termine dei disturbi d’ansia. 81 Tuttavia, se il trattamento si prolunga oltre i 6 mesi, possono verificarsi fenomeni quali tolleranza, accelerazione degli episodi, sensibilizzazione ed effetti paradossali. I costi nascosti dell’utilizzo dell’AD possono quindi superare i loro guadagni apparenti, in particolare quando la probabilità di reattività è bassa. 81
Le strategie terapeutiche che si rivelano efficaci a breve termine non sono necessariamente le più adatte per il trattamento a lungo termine. Purtroppo, un presupposto in gran parte non testato (ciò che fa stare meglio il paziente è il migliore per mantenerlo in salute) ha ostacolato il progresso della ricerca farmacologica sulla depressione, trascurando i farmaci che possono essere efficaci per il trattamento di mantenimento e non per il trattamento dell’episodio acuto 82
I farmaci antidepressivi sono farmaci essenziali se vengono approvate le indicazioni appropriate. Tuttavia, attualmente, le prescrizioni sono guidate da una considerazione sopravvalutata dei potenziali benefici, poca attenzione alla probabilità di risposta e trascuratezza delle potenziali vulnerabilità agli effetti avversi del trattamento. 81 Il modello oppositivo di tolleranza attende ancora adeguati test preclinici e di ricerca clinica. Tuttavia, fornisce un quadro concettuale per unificare i fenomeni clinici avversi che possono verificarsi nei pazienti e per valutare i benefici e i danni quando si utilizza l’AD.
Il modello non sembra applicarsi a tutti i pazienti sottoposti a trattamento con AD, ma solo a una frazione di essi. Lo studio delle variabili associate a tale evento in alcuni pazienti e non in altri sarebbe uno dei compiti più importanti dell’attuale ricerca terapeutica. Gli attuali sistemi diagnostici in psichiatria non considerano le componenti iatrogene della psicopatologia e possono essere applicati solo a pazienti che sono privi di droghe. Sono adatti per un paziente che non esiste più: la maggior parte dei casi che si osservano nella pratica clinica psichiatrica riceve farmaci psicotropi e tale trattamento è probabile che influisca sulla prognosi e sulle scelte terapeutiche.
Dichiarazione di conflitto di interessi
L’autore dichiara che non vi è alcun conflitto di interessi.
Finanziamento
L’autore non ha ricevuto alcun sostegno finanziario per la ricerca, la paternità e/o la pubblicazione di questo articolo.
Bibliografia
Vedi l’articolo originale disponibile a questo link