Peter R. Breggin, MD
Ithaca, NY
Pubblicato su Ethical Human Psychology and Psychiatry, Volume 8, Number 1, Spring 2006
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
Alla fine del 1999 l’avvocato Don Farber mi chiese di essere l’esperto medico in una causa di responsabilità del prodotto intentata dalla famiglia di Reynaldo Lacuzong contro la società farmaceutica Glaxo SmithKline (GSK) in California. Il signor Lacuzong era un operatore di macchinari senza precedenti di gravi malattie mentali, violenza o suicidalità prima che gli fosse prescritta una dose relativamente piccola di 10 mg di Paxil (paroxetina). Quasi immediatamente dopo aver iniziato l’antidepressivo inibitore selettivo della ricaptazione della serotonina (SSRI) simile al Prozac, ha sviluppato acatisia – un’agitazione interiore accompagnata da un’iperattività compulsiva – così come altri segni maniacali di irritabilità e ansia.
L’acatisia indotta dagli antidepressivi è nota per essere associata a violenza, suicidio, psicosi e deterioramento mentale generale (American Psychiatric Association, 2000, pp. 800-802). La depressione con agitazione indotta da farmaci può produrre risultati simili. Il terzo giorno di assunzione del Paxil, il signor Lacuzong ha annegato se stesso e i suoi due figli piccoli in una vasca da bagno.
Come esperto medico, sono stato autorizzato dal tribunale a esaminare centinaia di scatole di documenti della casa farmaceutica contenuti nella stanza dei registri sigillata della GSK. Questi documenti includevano la corrispondenza della Food and Drug Administration (FDA) e tutti gli studi clinici mondiali dell’azienda e i rapporti sugli effetti avversi del Paxil.
Il 21 luglio 2001, il mio rapporto sotto forma di affidavit è stato inviato all’arbitro giudiziario del caso. La relazione riguardava le pratiche della GSK nello sviluppo e nella commercializzazione del Paxil, e in particolare il suo presunto occultamento o manipolazione delle informazioni sulla pericolosità del farmaco. Basato sui file di proprietà della GSK che fino ad oggi non sono mai stati resi pubblici, il mio rapporto ha esaminato molti fattori, tra cui (a) quanto velocemente dopo la prima dose il Paxil può causare gravi reazioni avverse; (b) i tassi effettivi di acatisia; (c) il rischio effettivo di sovrastimolazione che causa agitazione, irritabilità e sintomi simili alla mania; (d) i tassi effettivi di suicidalità negli adulti; e (e) le dichiarazioni promozionali fatte per il farmaco.
La causa contro la GSK è stata infine “risolta” con la soddisfazione della GSK e della famiglia Lacuzong. La GSK ha negato e continua a negare tutte le accuse di negligenza nello sviluppo e nella commercializzazione del Paxil. La mia impressione è che una notevole quantità di denaro sia stata coinvolta nella risoluzione del caso, anche se l’importo non è stato rivelato. GSK all’epoca si rifiutò di svelare i suoi documenti o di permettermi di rendere pubbliche le mie scoperte, indipendentemente dalla loro importanza per la FDA, la professione medica e la salute pubblica.
Il 23 giugno 2005, il mio rapporto sul caso Lacuzong è stato depositato come parte di una mozione in un altro caso Paxil, Moffett contro Glaxo SmithKline, nel tribunale distrettuale degli Stati Uniti per il distretto meridionale del Mississippi. Poiché è stato depositato nei registri pubblici, il mio rapporto è ora disponibile al pubblico e sono in grado di commentare i dettagli. La versione completa è disponibile sul mio sito web www.breggin.com. Il rapporto dovrebbe risultare utile alla FDA, agli operatori sanitari, agli scienziati, ai ricercatori, agli avvocati, ai consumatori e a chiunque sia preoccupato di come funzionano le aziende farmaceutiche nello sviluppo e nella commercializzazione dei loro prodotti.
Nel frattempo, la FDA ha recentemente riconosciuto molte delle mie osservazioni originali sugli effetti stimolanti di tutti gli SSRI come Paxil e Prozac, così come di altri nuovi antidepressivi come Effexor. Ho messo in guardia per la prima volta su questi effetti in Toxic Psychiatry (Breggin, 1991) e poi in successivi articoli e libri sottoposti a peer-review (vedi per esempio Breggin, 1997, 2001, 2003).
A partire dal 2005, la FDA ora richiede ai produttori di farmaci di mettere sulle loro etichette elaborate avvertenze riguardanti il potenziale di questi farmaci di causare effetti stimolanti, tra cui agitazione, ansia, irritabilità, labilità emotiva, aggressività, ostilità e mania. Le etichette devono anche includere un avvertimento sull’aumento della suicidalità nei bambini. Senza giungere a una conclusione scientifica, la FDA ha anche messo in guardia e iniziato a indagare sul problema della suicidalità degli antidepressivi negli adulti. Tra le altre cose, il mio rapporto su Lacuzong tratta in dettaglio la suicidalità indotta dagli antidepressivi negli adulti e come la compagnia farmaceutica ha gestito questi dati.
I seguenti estratti includono le sezioni XI-XIV del rapporto che può essere trovato nella sua interezza su www.breggin.com. Queste sezioni estratte si concentrano sulla suicidalità indotta dal Paxil negli adulti, oggetto di un’indagine in corso della FDA. Altre sezioni trattano numerose questioni tra cui la corrispondenza della FDA che critica l’azienda, la pubblicità e la promozione, l’etichetta del farmaco, i tassi di effetti psichiatrici avversi dopo solo poche dosi, l’acatisia, e il continuum stimolante o di attivazione. Un lungo e dettagliato riassunto e una conclusione possono essere trovati nel rapporto completo.
ESTRATTI DALLA RELAZIONE E DALL’AFFIDAVIT DI PETER R. BREGGIN, MD, NELLA CAUSA LACUZONG CONTRO GLAXO SMITHKLINE
XI. Valutazione degli errori nella compilazione dei dati sul suicidio
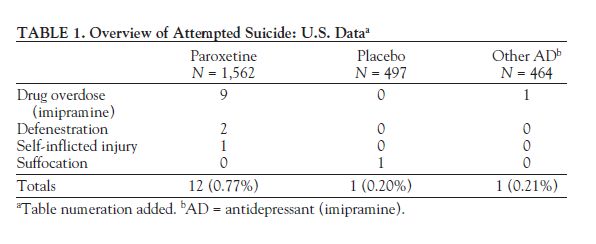
1. Tentativi di suicidio: Studi clinici statunitensi. Un totale di 14 tentativi di suicidio sono stati riportati negli studi clinici statunitensi. Nessuno era un suicidio completato. Una panoramica è presentata nella tabella 1 (PAR Safety Summary 20-Nov-1989, p. 203, stampata p. 297).
Si noti che il tasso di tentativi di suicidio con la paroxetina si avvicina all’1%, che la FDA considera “frequente”. Si noti anche che il tasso di tentativi di suicidio con la paroxetina è 3,8 volte superiore a quello del placebo e 3,6 volte superiore a quello degli antidepressivi di confronto (triciclici). Inoltre, il tentativo di suicidio su imipramina è elencato come un “possibile suicidio” (p. 211, timbro 306).
Per quanto riguarda l’insorgenza di tentativi di suicidio, un paziente (117A-004, pag. 200, timbro 291) si è tagliato il terzo giorno di Paxil: “Il terzo giorno questo paziente ha tentato di tagliarsi i polsi e l’addome ed è stato ritirato dallo studio”. Si noti anche che il caso 647 002 (sopra) ha fatto dei tentativi nei giorni 1, 8 e 15.
Questi dati importanti degli Stati Uniti non sono presentati nel testo del rapporto della SKB (ora Glaxo SmithKline o GSK) del 29 aprile 1991 per la FDA, “Suicidal Ideation and Behavior: Analysis of the Paroxetine Worldwide Clinical Database”. Nascondere i dati statunitensi nei dati mondiali era estremamente fuorviante.
2. Tralasciando due tentativi di suicidio non statunitensi. Ci sono prove che alcuni tentativi di suicidio sono stati omessi dai calcoli inviati alla FDA. Nel rapporto “Adverse experiences which occurred during active treatment. Non-US Phase II-III studies” (Appendice V.1), ho individuato due pazienti che sembrano essere stati omessi dai riassunti dei tentativi di suicidio non statunitensi. Il caso 647 002 (Volume 420, pag. 157) ha fatto tre tentativi di suicidio nei giorni 1, 8, e infine il giorno 15, quando il farmaco è stato interrotto. I primi due furono considerati “collegati” e il terzo “possibilmente collegato”. Inoltre, il caso 1 113 120 (Volume 420, pag. 157) fu considerato “sicuramente collegato al farmaco”. Questi due tentativi di suicidio non appaiono nella lista completa di 40 nel rapporto sui suicidi del 29 aprile 1991 (pp. 17-18), o in qualsiasi altra fonte che abbiamo trovato. Questo porta il totale dei tentativi di suicidio non statunitensi a 32.
3. Tralasciando due suicidi non statunitensi completati con Paxil. Due suicidi non statunitensi completati sembrano essere stati lasciati fuori da tutti i rapporti ufficiali, incluso il rapporto sui suicidi del 29 aprile 1991. I due mancanti si trovano nell’appendice 5.4.2-Summary of Deaths Occurring in Paroxetine-Treated Patients (pagina non numerata, SB 0000044). Vedere la Tabella 2 per i sette casi con le loro descrizioni complete sotto il titolo “Causa della morte e commenti”.
Poiché solo cinque suicidi non statunitensi sono elencati in qualsiasi tabella o rapporto, è evidente che ne mancano due. Altri due dovrebbero essere aggiunti al conteggio dei suicidi completati (vedi sotto). Ho controllato questi numeri e ho trovato che cinque sono inclusi (vedi singolo asterisco [*]) nelle liste ufficiali dei suicidi. Dobbiamo ottenere i due casi mancanti (vedi doppio asterisco [**]).
L’appendice 5.4.2 sembra essere basata sui dati del Summary Basis of Approval (SBA), che attinge dalla NDA. Faceva parte di un elenco di 15 decessi descritti in un memo del 25 agosto 1992 intitolato “Miscellaneous Requests” da Thomas P. Laughren, MD, della FDA a Thomas Donnelly, Jr, PhD, della SKB. Egli nota che ne sta aggiungendo uno, 083.003.1090, dall’aggiornamento sulla sicurezza, che fa anche parte della NDA originale.
Dobbiamo informarci su qualsiasi ulteriore corrispondenza o correzione riguardante questa lista.
4. Aggiunta di due suicidi completati con placebo agli studi non statunitensi. Nel rapporto suicidi sono elencati i seguenti due casi di suicidio: 7119.062 e 7119.009. Tuttavia, entrambi si sono verificati durante la fase di rodaggio del placebo (chiamata anche placebo wash-out). I casi possono essere trovati riassunti nel PAR Safety Summary del 20 novembre 1989 (7119.062 a pag. 202c, timbrato a pag. 296, SB 0000544; 7119.009 a pag. 202b, timbrato a pag. 295, SB 0000543).
Non c’è dubbio che placebo run-in sia un eufemismo per placebo wash-out. Nel rapporto sui suicidi del 29 aprile 1991, una nota a piè di pagina afferma: “I suicidi sono stati commessi durante la fase di eliminazione del placebo di uno studio di controllo attivo. Questi due atti sono stati commessi 2 giorni e 7 giorni prima della valutazione di base, cioè -2 e -7 giorni”.
Gli effetti avversi dei farmaci non sono mai riportati dalla fase di wash-out del placebo. Infatti, il suicidio e i tentativi di suicidio sono probabilmente gli unici presunti effetti avversi al farmaco riportati dal placebo wash-out. Il periodo di wash-out del placebo non fa parte degli studi clinici controllati. Si verifica prima della randomizzazione. Tutti i pazienti vi sono raggruppati. Inoltre, molti dei pazienti soffrono molto probabilmente di astinenza da altri farmaci che stavano precedentemente prendendo per la depressione.
L’inclusione di questi suicidi nel gruppo di confronto del placebo è stata fuorviante all’estremo. Devono essere rimossi dai calcoli relativi al confronto tra i suicidi su Paxil e quelli su placebo.
5. Inclusi due tentativi di suicidio placebo run-in in studi non statunitensi. I dati mondiali per i tentativi di suicidio includono anche i dati del placebo run-in. Questo è confermato nella Tabella XI.21, Tentativi di suicidio e overdose – Dati mondiali (PAR Safety Summary 10- Nov-1989, p. 206, pagina stampata 300, SB 0000548). Esattamente come nel caso dell’inclusione dei suicidi completati dalla fase di wash-out del placebo, l’inclusione di due pazienti run-in con placebo nella categoria dei tentativi di suicidio non statunitensi è fuorviante e fraudolenta. I due pazienti del placebo devono essere esclusi dai dati non statunitensi e mondiali.
XI. Ri-analisi dei dati sul suicidio
1. Rivalutare i suicidi completati non statunitensi. Vari documenti della SKB, incluso il rapporto sui suicidi del 29 aprile 1991, elencano solo cinque suicidi completati. Come descritto sopra, abbiamo trovato altri due per un totale di sette. Pertanto il tasso di suicidio completato per il Paxil è di sette in una popolazione di 1.401 pazienti per un tasso dello 0,499%. Come descritto anche sopra, abbiamo trovato che due suicidi completati per il placebo sono stati erroneamente contati nel tasso di suicidio per il placebo. La vera occorrenza dei suicidi completati nel gruppo placebo è 1 su 544 per un tasso dello 0,180%. Il tasso di suicidio su Paxil è quindi 2,7 volte quello su placebo.
2. Creazione di una nuova categoria di comportamento suicida o suicidi, tentati e compiuti. I 5 suicidi di Paxil completati (riconosciuti dalla SKB) devono essere aggiunti ai 42 (dalla tabella XI.21) tentati suicidi per creare la categoria di Comportamento suicida o suicidi, tentati e completati. La categoria contiene, come minimo, 47 casi di comportamento suicida (42 + 5 = 47). L’analisi della SKB oscura e nasconde il tasso reale di comportamento suicida valutando i suicidi tentati e completati come entità separate. Abbiamo anche bisogno di conoscere il tasso complessivo di comportamento suicida.
Sulla base di questa analisi, il tasso di comportamento suicida è 47 su 2.963 per un tasso dell’1,58%. Se aggiungiamo gli ulteriori due suicidi completati che sembrano essere stati lasciati fuori dai dati, abbiamo ora 49 (47 + 2 = 49) comportamenti suicidi su 2.963 per un tasso dell’1,65%. Sia che usiamo la cifra dell’1,58% o quella dell’1,65%, questa categoria combinata di comportamento suicida è molto più significativa delle categorie separate di tentativi di suicidio e suicidi completati. È stato grossolanamente fuorviante non creare una categoria combinata.
I calcoli di cui sopra erano basati sul presupposto che ci fossero 42 tentativi di suicidio come indicato nella NDA originale. Se aggiungiamo i due tentativi di suicidio che sembrano essere stati lasciati fuori dai dati, ci sono almeno 44 tentativi di suicidio totali. Il totale corretto per il comportamento suicida combinato su Paxil diventa quindi 51 (44 tentativi di suicidio + 7 suicidi = 51). Cinquantuno su 2.963 produce un tasso dell’1,72% per il comportamento suicida su Paxil.
3 Ri-analisi dei confronti mondiali per i tentativi di suicidio. Abbiamo già trovato che due tentati suicidi con il Paxil apparentemente non sono stati inclusi nei calcoli mondiali. Come descritto sopra, questo porta la cifra originale della NDA da 42 a 44 per i suicidi tentati su 2.963 casi, per un tasso dell’1,48%. Oltre a sottocontare i tentativi di suicidio con il Paxil, la SKB ha sovradichiarato i tentativi di suicidio legati al placebo. Per il placebo, sono elencati tre tentativi di suicidio. Ma come abbiamo documentato, il numero corretto per i suicidi da placebo è solo uno per il gruppo mondiale. Gli altri due tentativi di suicidio erano casi di wash-out da placebo. Questo rende il tasso di tentativi di suicidio da placebo solo 1 su 554 per un tasso dello 0,18%. Così il confronto corretto indica un tasso dell’1,48% di tentativi di suicidio su Paxil rispetto ad un tasso dello 0,18% di tentativi di suicidio su placebo in tutto il mondo. Così il suicidio su Paxil era 8,2 volte superiore al tasso del placebo.
4. Nascondere la frequenza dei suicidi nel mondo nel rapporto sui suicidi del 29 aprile 1991. Nella “Discussione e Conclusioni” del rapporto del 29 aprile 1991 (SB 0000819, report pp. 12-13) si afferma la seguente conclusione: L’incidenza dei tentativi di suicidio non differisce sostanzialmente tra i tre gruppi di trattamento (paroxetina, placebo, controlli attivi). Tuttavia, il rapporto non tratta mai gli studi clinici statunitensi come un’entità separata. Essi mostrano un tasso di tentativi di suicidio significativamente più alto per il Paxil che per gli altri antidepressivi o il placebo. Inoltre, non c’è una categoria generale di comportamento suicida o di suicidi, tentati e completati. Pertanto, quando si contano i tentativi di suicidio, i suicidi completati sono esclusi, travisando malamente i dati.
Inoltre, sembra che ci siano due tentativi di suicidio non segnalati e sei suicidi completati non segnalati in tutto il mondo. Infine, come già notato, la cifra mondiale è distorta da conteggi errati in entrambe le categorie Paxil e placebo. Il rapporto sui suicidi del 29 aprile 1991 contiene anche numeri diversi dalla NDA. Troviamo che il numero totale di tentativi di suicidio con la paroxetina è stato inspiegabilmente ridotto da 42 nella NDA a 40 due anni dopo, mentre il numero totale di tentativi di suicidio con il placebo è stato inspiegabilmente aumentato da 3 a 6. Queste manipolazioni favoriscono ovviamente l’interesse della casa farmaceutica. Il rapporto del 29 aprile 1991 dichiara infatti di essersi basato sui dati originali della NDA, cioè “utilizzando i dati che erano stati presentati all’epoca della New Drug Application per la paroxetina” (p. 1, SB 0000003). Ma i dati NDA differiscono a svantaggio di SKB.
XIII. Follow-Up dei casi di tentativi di suicidio negli Stati Uniti
Sono stato in grado di rintracciare molti ma non tutti i numeri dei casi individuali elencati nella compilazione dei tentativi di suicidio (Tabella XI.19 dal PAR Safety Summary 20-Nov-1989, pag. 203, timbrata pag. 297). I casi sono stati trovati separatamente in un documento, “Narrative of US Patients with Potentially Clinically Significant Events” (Appendice I.1 di NDA 20031, 409, novembre 1989). Essi indicano che i tentativi di suicidio spesso si verificano in un contesto di varie altre reazioni avverse al farmaco angoscianti, ma a volte si verificano senza alcun altro effetto avverso serio. Questo contrasta con i dati non statunitensi sui suicidi completati che indicano che i cinque che abbiamo potuto rintracciare erano tutti legati a reazioni avverse al sistema nervoso centrale, tra cui acatisia e stimolazione.
(1) 02-04-089 (p. 37). Questo paziente aveva preso Paxil 20 mg per 40 giorni. “Le esperienze cliniche avverse . . erano moderati capogiri e mancanza di energia (probabilmente legati al farmaco), e moderati mal di testa (possibilmente legati al farmaco)”.
(2) 04-01-009 (pag. 192; SB 0000571). Questo paziente ha scelto di passare da un triciclico al Paxil. Dopo 193 giorni il paziente prendeva 50 mg e sperimentava le seguenti reazioni ad- verse: “stringere i denti”, bocca secca, diminuzione della libido, incapacità di raggiungere l’orgasmo, nausea, diarrea, ritenzione urinaria, “debolezza nelle gambe”, “contrazione della guancia sinistra”, vertigini, ansia, “sensazione di velocità”, vertigini, “formicolio”, letargia, mal di testa e diminuzione della concentrazione.
(3) 04-02-056 (Volume 409, pag. 260). Questo paziente stava prendendo Paxil 40 mg e a 19-20 giorni si è fatto dei graffi autoinflitti. Al paziente è stato dato l’ECT [quindi probabilmente ha sperimentato un peggioramento della depressione]. A parte la secchezza delle fauci, non sono stati riportati altri ADR.
(4) 04-06-96. Questo paziente era sotto 30 mg di Paxil per 116 giorni. Il paziente non poteva essere localizzato nel “Narrative of US Patients with Potentially Clinically Significant Events”.
(5) 05-01A-030 (Volume 410, p. 65). Questo paziente di 23 anni stava prendendo Paxil 50 mg e ha tentato il suicidio due volte. I due tentativi sono stati contati solo una volta. “Il paziente ha richiesto l’ospedalizzazione a causa dell’uso eccessivo di etanolo con un comportamento violento e imprevedibile. Ha fatto un’overdose intenzionale.
(6) 05-01A-075. Questa paziente era una donna di 37 anni che prendeva Paxil 40 mg da più di tre anni. Non è stata trovata nel “Narrative of US Patients with Potentially Clinically Significant Events”.
(7) 05-02B-019 (Volume 410, pag. 124). Questa paziente stava prendendo Paxil 50 mg per 57 giorni quando si è verificata l’overdose. “Le esperienze avverse riportate durante lo studio sono state lieve eruzione cutanea, diarrea, ‘tremore’ (possibilmente legato al farmaco), e un’overdose”. Ha preso 20-50 pillole sconosciute ed è stata ricoverata in ospedale.
(8) 05-02F-002 (Volume 410, pag. 151). Questa paziente ha preso Paxil 40 mg per 38 giorni e ha tentato il suicidio. Non sono stati riportati altri ADR.
(9) 07-01A-001. Questa persona stava prendendo Paxil 40 mg per 20 giorni. Il caso non poteva essere lo- cato nel “Narrative of US Patients with Potentially Clinically Significant Events”.
(10) 09-01A-005 (Volume 410, pag. 196). Questa paziente stava prendendo Paxil 40 mg ed è andata in overdose a 7 giorni. Stava sperimentando “sonnolenza moderata, tremore, nausea grave (probabilmente legata al farmaco), e overdose”. E’ andata in overdose una seconda volta 7-8 giorni dopo. Ci sono state quindi due overdose, una durante l’esposizione al farmaco, e una apparentemente entro una settimana dopo l’astinenza.
(11) 09-01E-260. Questo paziente stava prendendo Paxil 10 mg per 60 giorni. Il paziente non poteva essere localizzato nel “Narrative of US Patients with Potentially Clinically Significant Events”.
(12) 09-01J-573 (Volume 410, pag. 279). Questo paziente prendeva Paxil 10 mg secondo il riassunto (p. 298) ma assumeva 20 mg secondo questo rapporto di caso. L’esposizione al farmaco è stata elencata come 26 giorni ma sembra essere stata di 30 giorni. Il paziente “saltò dalla finestra del secondo piano” e “ricevette fratture multiple”.
Oltre a questi 12 pazienti con Paxil che hanno tentato il suicidio (per un totale di 14 tentativi), c’è stato un tentativo di suicidio su imipramina e uno su placebo. Seguono:
(13) 04-06-088 (Volume 410, p. 50). Questo paziente stava prendendo imipramina 225 mg per 61 giorni. Il paziente è stato elencato come “possibile tentativo di suicidio”. “Secondo quanto riferito, aveva preso una quantità sconosciuta di ‘pillole’ ed era intossicato”. In effetti, questo probabilmente non è un tentativo di suicidio.
Se questo caso viene scartato, non ci sono altri casi di tentativo di suicidio sul farmaco di confronto e il rapporto diventa 12-14 a 0. Sembra che la casa farmaceutica abbia tentato di coprire il più alto tasso di tentativi di suicidio sul Paxil includendo questo improbabile caso di tentativo di suicidio.
(14) 02-01-009 (volume 410, p. 5). Questo paziente è stato sotto placebo per 6 giorni. Il caso è descritto come “un gesto di suicidio per soffocamento. Il marito ha impedito il suo suicidio”. Non si noti che questo caso è un “gesto”. Non ho trovato nessun “gesto” nel gruppo Paxil.
Se questo caso viene scartato, così come l’unico caso di imipramina, allora ci sono stati 12-14 tentativi di suicidio tra 12 pazienti su Paxil e nessuno su placebo o su imipramina.
XIV. Prove crescenti di suicidalità con il Paxil
Il 1.14.00 la FDA ha scritto una lettera di 3 pagine a Thomas Kline della SKB suggerendo un cambiamento di etichetta. La FDA raccomanda un cambiamento dell’etichetta sotto “Sovradosaggio/Esperienza umana”. Dall’introduzione negli Stati Uniti, 342 casi spontanei di sovradosaggio deliberato o accidentale con la paroxetina sono stati riportati in tutto il mondo (circa 1999). Diciassette hanno coinvolto Paxil da solo. Ci sono stati 48 decessi. Questo problema è ancora più grave di quanto indicato dalla FDA, dato che c’è ovviamente un gran numero di tentativi di suicidio in questo gruppo.
Bibliografia
- American Psychiatric Association. (2000). Diagnostic and statistical manual of mental disorders (4th ed., text revision) (DSM-IV-TR). Washington, DC: Author
- Breggin, P. (1991). Toxic psychiatry. New York: St. Martin’s Press.
- Breggin, P. (1997). Brain-disabling treatments in psychiatry. New York: Springer Publishing Company. Breggin, P. (2001). The antidepressant fact book. Cambridge, MA: Perseus Books.
- Breggin, P. R. (2003). Suicidality, violence, and mania caused by selective serotonin reuptake in- hibitors: A review and analysis. Ethical Human Sciences and Services, 5, 225–246.