Fava GA a, b · Gatti A. a · Belaise C. a · Guidi J. a · Offidani E. c
Pubblicato su Psychotherapy and Psychosomatics 2015;84:72-81
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
a Affective Disorders Program, Department of Psychology, University of Bologna, Bologna, Italy;
b Department of Psychiatry, State University of New York at Buffalo, Buffalo, N.Y., and
c Center for Complementary and Integrative Medicine, Weill Cornell Medical College, New York, N.Y., USA
Introduzione
Negli anni ’90, case report [1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16] hanno iniziato a documentare le reazioni di astinenza in seguito all’interruzione della ricaptazione selettiva della serotonina inibitori (SSRI). Con l’aumentare del volume della letteratura, una delle prime recensioni [17] ha suggerito che potrebbe effettivamente verificarsi una sindrome da sospensione consistente in un gruppo di sintomi somatici e psicologici.
I dati clinici hanno suggerito che la sindrome potrebbe durare fino a 3 settimane e potrebbe essere migliorata riavviando lo stesso o un farmaco antidepressivo (AD) simile. Anche se i sintomi da sospensione sono stati per lo più riportati dopo una sospensione improvvisa, si è riscontrato che si manifestavano anche dopo una graduale riduzione [17, 18, 19] e differivano nella prevalenza in base al profilo farmacologico dell’SSRI [20, 21].
Nel 1998 è stato sviluppato un indice specifico per la sintomatologia da astinenza, la checklist dei segni e sintomi emergenti da sospensione (DESS) [22] . Criteri diagnostici, come quelli sviluppati da Black et al. [23], sono stati proposti. Tali criteri comprendevano sia sintomi somatici (vertigini, stordimento, sensazioni di shock, parestesie, affaticamento, mal di testa, nausea, tremore, diarrea e disturbi visivi) che psicologici (ansia, insonnia e irritabilità) e richiedevano un disagio significativo essere associato a loro [23].
Il termine “sindrome da sospensione” ha progressivamente sostituito “sindrome da astinenza” o “reazioni” [24]. Nell’ultimo decennio, pochi studi hanno valutato la presenza di sintomi da sospensione e l’argomento ha attirato un’attenzione limitata anche per quanto riguarda le revisioni della letteratura [25, 26, 27, 28]. Per quanto ne sappiamo, in lingua inglese non è stata effettuata una revisione sistematica degli aspetti clinici dell’interruzione del trattamento con SSRI secondo criteri stabiliti [29]. Tuttavia, tale conoscenza è importante a causa dell’uso diffuso degli SSRI nella pratica medica.
Metodi
Origine dei dati
Le linee guida PRISMA sono state seguite per condurre una revisione sistematica della letteratura, esaminando la presenza di sintomi di astinenza/interruzione di SSRI [29]. I titoli, gli abstract e gli argomenti sono stati ricercati utilizzando i seguenti termini: “sintomi da astinenza” OPPURE “sindrome da astinenza” OPPURE “sindrome da sospensione” OPPURE “sintomi da sospensione” E “SSRI” OPPURE “serotonina” OPPURE “antidepressivo” OPPURE “paroxetina” OPPURE “fluoxetina” O “sertralina” O “fluvoxamina” O “citalopram” O “escitalopram”. I database della letteratura di ricerca elettronica includevano CINAHL, Cochrane Library, PubMed e Web-of-Science dall’inizio di ciascun database fino a luglio 2014. Sono stati fissati limiti alla popolazione adulta, agli esseri umani e alla lingua inglese. Sono stati inoltre esaminati elenchi di riferimento e citazioni di relazioni inizialmente individuate. Ulteriori studi clinici sono stati cercati manualmente.
La ricerca è stata condotta in modo indipendente da due investigatori (AG e CB); i disaccordi sono stati risolti per consenso tra questi valutatori primari e gli altri ricercatori (GAF, JG ed EO). Gli articoli sono stati considerati idonei se hanno segnalato almeno un caso di sindrome da astinenza dopo l’interruzione del trattamento con SSRI. Abbiamo limitato la nostra ricerca ai farmaci SSRI. A causa dell’importanza delle osservazioni fortuite, abbiamo incluso studi di vari disegni: studi randomizzati e controllati (RCT), indagini aperte, studi retrospettivi e singoli casi clinici. Sono stati esclusi gli studi se sono stati condotti in campioni e contesti non clinici e/o si sono basati sull’esplorazione dei siti Web dei pazienti [30].
I dati sono stati estratti indipendentemente da entrambi i revisori con l’uso di un modulo precodificato. I seguenti dati sono stati estratti da studi che soddisfano i criteri per l’inclusione nella revisione sistematica: età, distribuzione di genere, disegno dello studio, tipo di SSRI, numero di pazienti, confronti di gruppo, durata del trattamento e tempi di valutazione e metodi utilizzati per valutare i sintomi di astinenza. I termini “ricaduta/recidiva”, “rimbalzo” e “ritiro” sono stati utilizzati secondo le definizioni di Chouinard [31]: i sintomi ricorrenti sono un graduale ritorno dei sintomi originari del paziente con la stessa intensità di prima del trattamento; i sintomi di rebound sono un rapido ritorno dei sintomi originali ma peggiori rispetto a prima del trattamento e i sintomi di astinenza sono nuovi sintomi che non facevano parte della malattia del paziente prima del trattamento e sono associati a classi specifiche di farmaci psicotropi. I termini “sindromi da astinenza” e “sindromi da sospensione” sono stati considerati equivalenti. In particolare nei case report, è stata verificata l’aderenza alla descrizione prototipo delle sindromi da sospensione degli SSRI [23] ma non è stata considerata un requisito.
In considerazione delle popolazioni di pazienti altamente eterogenee e delle differenze nel disegno dell’RCT, una meta-analisi non è stata ritenuta appropriata.
Risultati
Caratteristiche degli studi inclusi
La ricerca in letteratura ha identificato 437 documenti potenzialmente rilevanti sulla sindrome da astinenza/interruzione di SSRI; 275 sono stati lasciati dopo la rimozione dei duplicati. Dai titoli e dagli abstract, 31 studi sono stati esclusi poiché riguardavano farmaci psicotropi diversi dagli SSRI. Un’ulteriore esclusione ha coinvolto 128 pubblicazioni per mancanza di pertinenza alle reazioni di ritiro e altre 55 per essere recensioni o commenti. Un totale di 61 indagini ha soddisfatto i criteri per l’inclusione nello studio (suppl. online fig. 1, per tutto il materiale suppl. online, vedere www.karger.com/doi/10.1159/000370338). Ci sono stati 15 studi randomizzati che hanno confrontato fluoxetina, sertralina, paroxetina, citalopram, escitalopram e placebo o altri AD (suppl. online, tabella 1). Altri studi includevano 4 studi aperti e 4 indagini retrospettive (suppl. online, tabella 2). Sono stati inoltre esaminati in totale 38 referti clinici (suppl. online, tabella 3). Questi studi sono stati riassunti e rivisti criticamente in base alle caratteristiche del disegno di ricerca.
Confronti di farmaci singoli e placebo
Il primo RCT per valutare la presenza di sintomi da sospensione dopo la sospensione di SSRI è stato condotto su 120 pazienti affetti da disturbo di panico e che sono stati trattati con terapia cognitiva e paroxetina (20, 40, 60 mg/die) per 12 settimane [32]. Dopo la brusca interruzione, i sintomi di astinenza (principalmente capogiri) si sono verificati in una percentuale significativamente maggiore di individui che assumevano paroxetina (34,5%) rispetto ai soggetti trattati con placebo (13,5%) [32]. Nel 1998, Zajecka et al. [17] ha trattato 395 pazienti che soddisfacevano i criteri del DSM-III-R per la depressione maggiore con 12 settimane di fluoxetina.
I pazienti che hanno risposto sono stati assegnati in modo casuale al placebo (interruzione improvvisa) o alla continuazione per 6 settimane. I sintomi da sospensione sono stati valutati da segnalazioni spontanee e domande a risposta aperta. Dopo 2 settimane, la sonnolenza è risultata significativamente più frequente nei pazienti che hanno interrotto bruscamente il farmaco (4%) rispetto a quelli che hanno continuato a ricevere fluoxetina (0%, p <0,01). Alle settimane 4 e 6, i soggetti nel gruppo placebo hanno riportato capogiri più frequentemente rispetto ai pazienti nel gruppo di continuazione (7 vs 4%, p <0,05 e 5 vs 1%, p <0,05, rispettivamente).
Nel 2000, Markowitz et al. [33] hanno riesaminato i dati di uno studio controllato con placebo condotto in precedenza [34] che ha valutato l’efficacia del citalopram nei pazienti con depressione.
Dopo 8 settimane di trattamento, i pazienti sono stati randomizzati a ricevere placebo (condizione da sospensione) o a continuare con il farmaco attivo per altre 24 settimane. I sintomi da sospensione sono stati valutati dopo 2 settimane utilizzando la scala degli effetti collaterali indesiderati (UKU) [35]. I risultati, ottenuti in base allo stato di recidiva dei pazienti, non hanno mostrato differenze nei sintomi neurologici e psichiatrici tra gli individui passati al placebo e quelli che hanno continuato con il trattamento attivo. Tuttavia, la durata del trattamento è stata breve e i metodi di valutazione non erano mirati a rilevare i sintomi di astinenza.
Montgomery et al. [36], dopo un trattamento in aperto di 12 settimane con escitalopram, ha randomizzato 371 pazienti affetti da disturbo d’ansia sociale (SAD) in uno studio controllato in doppio cieco che ha confrontato escitalopram (da 10 a 20 mg/die; n = 190) e placebo (n = 181). I risultati hanno mostrato che, 1 e 2 settimane dopo la randomizzazione, il punteggio DESS totale era significativamente più alto in coloro che avevano interrotto escitalopram rispetto al gruppo di continuazione (p <0,01).
Confronti multipli di farmaci
Diversi studi che hanno confrontato diversi SSRI hanno studiato l’insorgenza dei sintomi da sospensione. Nel 1998, Rosenbaum et al. [22] ha condotto uno studio randomizzato in doppio cieco di sostituzione con placebo della durata di 1 settimana per valutare l’insorgenza di sintomi da sospensione in 231 pazienti con disturbo depressivo maggiore (MDD) trattati con paroxetina, sertralina o fluoxetina. Dopo l’interruzione del trattamento, i sintomi da sospensione, misurati attraverso il DESS, sono stati riportati più frequentemente dai pazienti trattati con paroxetina (p <0,001) e sertralina (p <0,001) rispetto a quelli trattati con fluoxetina.
Quando i trattamenti sono stati confrontati, gli individui trattati con paroxetina hanno riportato il maggior numero di sintomi DESS rispetto a quelli trattati con sertralina (p <0,05) e fluoxetina (p <0,001). Inoltre, durante l’interruzione, ansia, depressione, sintomi somatici e ostilità erano significativamente maggiori nei gruppi paroxetina e sertralina (p < 0. In uno studio successivo, Michelson et al. [37] ha reclutato pazienti con una storia di depressione, trattati con successo con fluoxetina, sertralina o paroxetina. All’ingresso, i pazienti stavano assumendo farmaci in modo continuativo per almeno 4 mesi ma non più di 3 anni e non avevano avuto modifiche della dose nei 2 mesi precedenti l’ingresso nello studio
In condizioni randomizzate in doppio cieco, tutti i soggetti sono stati sottoposti a sostituzione del placebo per un periodo di 5 giorni e hanno continuato il trattamento con il loro SSRI abituale durante il periodo di 5 giorni successivo. I soggetti hanno continuato il trattamento con l’SSRI in tutti gli altri momenti. Lo studio ha mostrato che la sostituzione con placebo, ma non la continuazione del trattamento attivo, era associata ad aumenti statisticamente significativi del numero totale di eventi avversi sollecitati per i pazienti trattati con paroxetina entro la fine del quarto giorno (p <0,001).37].
Giudice et al. [38] hanno raggiunto risultati simili confrontando paroxetina e fluoxetina durante una sostituzione randomizzata del placebo da 5 a 8 giorni. Circa il 16% dei pazienti che assumevano paroxetina rispetto al 6% di quelli che assumevano fluoxetina hanno riportato sintomi da sospensione (p < 0,05). Durante l’interruzione, il gruppo di trattamento con paroxetina ha anche riportato aumenti significativi dei sintomi depressivi e dei punteggi di gravità clinica globale, nonché difficoltà nel funzionamento sociale. La paroxetina ha anche ottenuto punteggi significativamente più alti sul DESS rispetto all’agomelatina in 192 pazienti con MDD [39].
I tassi di sintomi da astinenza erano significativamente maggiori nei pazienti che avevano interrotto la paroxetina rispetto a quelli che continuavano il trattamento (p < 0,001), mentre non sono state riscontrate differenze significative nel gruppo di pazienti con agomelatina (3,0 ± 4,2 e 4,4 ± 5,7).
Risultati simili sono emersi anche quando la paroxetina è stata confrontata direttamente con altri SSRI. In particolare, Hindmarch et al. [40], in 87 pazienti affetti da depressione che avevano interrotto la terapia di mantenimento con paroxetina, fluoxetina, sertralina e citalopram per 4-7 giorni, hanno riferito che, sebbene i punteggi DESS fossero aumentati in tutti i gruppi di trattamento, la paroxetina ha causato sintomi da interruzione significativamente maggiori rispetto a altri SSRI hanno fatto (p <0,05).
Due RCT hanno esaminato l’insorgenza dei sintomi di astinenza dopo il trattamento con escitalopram [41] o sertralina [42]. Quando escitalopram è stato confrontato con venlafaxina XR in pazienti con MDD, significativamente più pazienti trattati con venlafaxina rispetto a quelli trattati con escitalopram hanno riportato un punteggio DESS >4 in un periodo di runout di 1 settimana (p <0,01) [41]. Aumento dei sogni, disturbi del sonno, nervosismo o ansia, irritabilità e improvviso peggioramento dell’umore si sono verificati con un’incidenza >10% nel gruppo escitalopram. Sir et al. [42] ha valutato sistematicamente la presenza di reazioni da astinenza utilizzando la scala di interruzione dell’antidepressivo (ADDS) [42] in uno studio randomizzato multicentrico di 8 settimane che ha confrontato sertralina e venlafaxina XR in 163 pazienti con MDD.
Dopo un’interruzione graduale, il 34,3% dei pazienti trattati con sertralina ha manifestato una sindrome da sospensione da moderata a grave; Il 23,9% di loro ha manifestato una lieve reazione da interruzione, mentre il 23,9% ne ha segnalata una minima. I soggetti che assumevano venlafaxina XR hanno anche riportato sintomi da sospensione da minimi a molto gravi (minimo = 17,7%; lieve = 27,4%; moderato = 38,7%; grave = 3,2%; molto grave = 1,6%). Gli autori hanno riportato solo sintomi di ADDS che si sono verificati in più del 10% dei pazienti, senza mostrare differenze tra coloro che hanno ricevuto sertralina rispetto a venlafaxina XR. Vertigini (33,3%), sogni vividi (26,4%), affaticamento (22,2%), vertigini (5,6%), umore in rapido cambiamento (6,9%) e tachicardia (4.2 %] eran0o i sintomi più frequentemente riportati [42].
È stato osservato che la paroxetina causa sintomi da sospensione anche in pazienti con disturbi d’ansia. Nei pazienti con SAD, il 28,4% di coloro che erano stati trattati con paroxetina aveva un punteggio DESS totale ≥4, rispetto a 15,1, 17,1 e 21,7% dei pazienti trattati con escitalopram (5, 10 e 15 mg, rispettivamente) e l’1,9% di pazienti assegnati al placebo (p < 0,001 vs. placebo) [43]. Risultati simili sono emersi in pazienti affetti da disturbo d’ansia generalizzato. Dopo uno studio randomizzato controllato con placebo di 12 settimane di escitalopram (5, 10 o 20 mg, rispettivamente) e paroxetina, i pazienti con disturbo d’ansia generalizzato sono stati sottoposti a un periodo di washout di 2 settimane [44].
Alla sospensione, mentre i pazienti trattati con escitalopram non differivano in termini di eventi avversi dai controlli con placebo, quelli che hanno interrotto la paroxetina hanno mostrato un punteggio DESS medio significativamente più alto rispetto ai controlli (p <0,001). Per quanto riguarda i farmaci attivi, la paroxetina ha prodotto significativamente più sintomi da sospensione rispetto a escitalopram (5 o 10 mg, p < 0,001) [44].
Baldwin et al. [45] hanno valutato la differenza tra interruzione improvvisa e graduale quando si utilizzava paroxetina o escitalopram in pazienti con MDD. Gli effetti emergenti dall’interruzione sono stati valutati in due periodi separati in doppio cieco. In primo luogo, i pazienti sono stati randomizzati a uno dei due periodi di interruzione del trattamento (sostituzione con placebo per 3-5 giorni), quindi sono stati randomizzati a un periodo di sospensione graduale da 1 a 2 settimane. Durante la breve sostituzione con placebo, non ci sono state differenze significative.
Nella condizione ridotta, i risultati hanno mostrato che le variazioni del punteggio DESS totale erano significativamente maggiori per paroxetina rispetto a escitalopram dopo 1 settimana di somministrazione a giorni alterni (p < 0,01) e una settimana successiva (post trattamento) con placebo (p < 0,01). Per esaminare due diverse strategie di tapering, Tint et al. [46] hanno randomizzato 28 pazienti trattati con diversi SSRI o venlafaxina a una riduzione graduale (3 giorni) o lunga (14 giorni). I risultati hanno mostrato che il 46% dei soggetti ha riportato sintomi da interruzione e che l’incidenza era simile in entrambe le condizioni (47 contro 46% nei gruppi corto vs. lungo).
In conclusione, tra i pazienti con MDD, il punteggio medio DESS medio era 5,7 (DS = 7,36) per coloro che hanno interrotto il trattamento con paroxetina [22, 38, 39, 45], mentre per escitalopram [41, 45] variava da 2,4 a 3.2, e in entrambi gli studi che hanno esaminato l’interruzione del trattamento con fluoxetina [22, 38], era 0,2 (DS = 3,86). Nei pazienti con SAD, i tassi di interruzione dei sintomi dopo il trattamento con escitalopram (10-20 mg/die) variavano dal 17 al 27% [36, 43]. Tuttavia, solo pochi studi hanno utilizzato una definizione di reazione da astinenza basata su criteri specifici [23,47] o un punteggio limite del DESS [36, 40, 43, 46] per determinare l’insorgenza dei sintomi di astinenza.
Sintomi di astinenza nelle prove aperte
Due studi aperti sulla fluvoxamina che hanno coinvolto rispettivamente 17 pazienti con disturbo ossessivo-compulsivo [48] e 14 con disturbo di panico [3] hanno riportato sistematicamente l’insorgenza di sindromi da astinenza. In entrambi i report, i pazienti hanno manifestato reazioni da astinenza valutate utilizzando la Hopkins Symptom Checklist (HSCI-90) di 90 voci [48] o basandosi su segnalazioni spontanee [3].
Il 23% dei pazienti con disturbo ossessivo-compulsivo [48] e l’85,7% dei pazienti con PD [3] hanno manifestato vertigini, nausea, mal di testa, confusione, bassa energia e debolezza che sono diminuite in circa 2-3 settimane. Bogetto et al. [49] hanno esaminato la sindrome da sospensione in 97 pazienti con disturbo distimico trattati con paroxetina (n = 52) o fluoxetina (n = 45). Circa il 27% del campione totale ha riportato sintomi di astinenza dopo aver interrotto la terapia secondo le istruzioni del proprio psichiatra. Di questi, l’84,6% è stato trattato con paroxetina. Inoltre, i pazienti con un esordio precoce del disturbo distimico avevano maggiori probabilità di riportare sintomi di astinenza.
Un’indagine di Fava et al. [50] hanno esplorato la prevalenza e le caratteristiche delle sindromi da sospensione conseguenti alla riduzione graduale degli SSRI in pazienti con disturbo di panico e agorafobia che si erano rimessi in seguito al trattamento comportamentale. Nove su 20 pazienti (45%) hanno manifestato una sindrome da sospensione secondo criteri specifici basati sul DESS. Le sindromi da sospensione si sono attenuate entro un mese in tutti i pazienti tranne 3 (27%). Questi 3 pazienti hanno tutti ricevuto paroxetina e hanno mostrato un’alternanza di peggioramento dell’umore, affaticamento e instabilità emotiva con disturbi del sonno, irritabilità e iperattività, soddisfacendo i criteri del DSM-IV [51] per il disturbo ciclotimico tranne che per la durata.
Sintomi di astinenza in studi retrospettivi
Coupland et al. [52] hanno utilizzato grafici retrospettivi per riportare l’incidenza dei sintomi da astinenza in 171 pazienti che hanno interrotto il trattamento con clomipramina e diversi SSRI (fluoxetina, fluvoxamina, paroxetina e sertralina). I sintomi si sono verificati significativamente più frequentemente nei pazienti trattati con uno degli SSRI a emivita più breve, fluvoxamina o paroxetina (17,2%) o con clomipramina (30,8%) rispetto ai pazienti che assumevano SSRI con metaboliti a emivita più lunga come la sertralina o fluoxetina (1,5%). In uno studio simile [53], il database del Regno Unito per le segnalazioni spontanee di sospette reazioni avverse al farmaco è stato utilizzato per descrivere le reazioni associate all’interruzione di diversi SSRI. Gli autori hanno sottolineato che le reazioni di astinenza con la paroxetina costituivano una percentuale maggiore delle segnalazioni rispetto agli altri SSRI. La sindrome da sospensione era anche più comune nei pazienti giovani rispetto agli anziani.
Himei e Okamura [54] hanno studiato l’insorgenza di sintomi da sospensione utilizzando le cartelle cliniche di 385 pazienti ambulatoriali a cui era stato diagnosticato un singolo episodio di MDD ed erano stati sottoposti a monoterapia con paroxetina nei 5 anni precedenti. I risultati hanno mostrato che il 10% dei pazienti ha manifestato sintomi da sospensione. Inoltre, era più probabile che si verificassero sintomi di astinenza nei pazienti che hanno interrotto bruscamente la paroxetina rispetto a quelli che hanno ridotto gradualmente il farmaco.
È interessante notare che è emersa un’associazione tra l’insorgenza della sindrome da sospensione e l’età, sebbene tale associazione sembrava essere moderata dal fatto che i pazienti più giovani erano più inclini a interrompere bruscamente il farmaco. Van Geffen et al. [55] hanno studiato diverse strategie di tapering valutando retrospettivamente le caratteristiche dell’interruzione nei pazienti che avevano precedentemente interrotto il loro SSRI. È emersa una differenza significativa a favore di un’interruzione graduale. In particolare, i pazienti che hanno interrotto bruscamente il trattamento hanno riportato un numero significativamente maggiore di eventi avversi rispetto a quelli che hanno ridotto gradualmente il farmaco (p <0,01).
Sintomi di astinenza nei rapporti sui casi
Fluoxetina
Sono stati recuperati sei casi clinici di reazioni da astinenza da fluoxetina [1, 5, 10, 56, 57, 58]. In tutti i casi, i soggetti hanno interrotto bruscamente i loro farmaci e i sintomi di astinenza sono comparsi per lo più entro 2 giorni, ad eccezione di 1 paziente che ha riportato sintomi 2 settimane dopo l’interruzione. I sintomi più comuni erano vertigini, stordimento e disturbi del sonno. Anche due soggetti hanno sperimentato delirio [10, 58]. Un paziente si è lamentato di reazioni distoniche [1] e 1 ha avuto una cataplessia di rimbalzo prolungata [57]. Gli autori non hanno riportato informazioni sulla durata delle sindromi da astinenza, probabilmente perché i sintomi sono stati trattati reintroducendo la fluoxetina [10, 57, 58] o somministrando altri farmaci [1, 5].
Paroxetina
Abbiamo identificato 18 casi clinici di sintomi da astinenza in pazienti adulti (di età compresa tra 22 e 73 anni) che assumevano paroxetina. I sintomi di interruzione sono stati riportati indipendentemente dalla durata del trattamento (da poche settimane ad anni) e dal tipo di interruzione (improvvisa vs. graduale). I sintomi di solito sono comparsi 1 settimana dopo l’interruzione, ad eccezione di 1 paziente che ha manifestato sintomi dopo 1 mese [59]. I sintomi più comunemente riportati sono stati vertigini, stordimento, affaticamento, disturbi del sonno e disturbi gastrointestinali [7, 11, 60]. Reazioni meno comuni sono state sensazione di “shock elettrico” [9, 59, 61, 62], allucinazioni visive e uditive [9, 59, 61, 62], allucinazioni visive e uditive [63], enuresi notturna [64], prurito [65] ed emesi [6]. Nella maggior parte dei rapporti, i sintomi sono durati fino alla reintroduzione della paroxetina o al passaggio ad altri farmaci e/o terapia cognitivo-comportamentale [12, 13, 15, 59, 62, 66]. Solo in pochi casi i sintomi si sono risolti spontaneamente in circa 2 settimane [4, 8, 63, 67].
Sertralina
Otto case report hanno evidenziato la presenza di reazioni da astinenza nei soggetti che hanno interrotto la sertralina. In tutte le segnalazioni, le reazioni da sospensione sono apparse entro 1-5 giorni dopo l’interruzione improvvisa [68, 69] o graduale [9, 14, 13, 16, 70, 71] e sono durate da 1-2 settimane [13, 14, 69, 70] a 6 settimane [16] o anche più a lungo (13-14 settimane) [9, 68]. Nella maggior parte dei casi, i sintomi sono scomparsi spontaneamente, ad eccezione di 2 segnalazioni in cui è stata reintrodotta la sertralina 25-50 mg/die [68, 71] e altre 2 in cui è stata prescritta una combinazione di farmaci psicotropi [69, 70]. Stanchezza, instabilità, vertigini e sintomi simil-influenzali sono state le reazioni avverse riportate più frequentemente. Sono stati riportati anche sintomi extrapiramidali e sensazioni di shock elettrico [9, 70]. Inoltre, 1 paziente ha manifestato ipotensione ortostatica [71].
Fluvoxamina
Sono stati inoltre pubblicati tre casi clinici di sindrome da sospensione della fluvoxamina [2, 72, 73]. Anche se un paziente ha interrotto gradualmente la fluvoxamina [72] e un altro ha saltato solo poche dosi [73], entrambi hanno manifestato sintomi di astinenza come vertigini, nausea, parestesie, perdita di concentrazione, sentimenti irrequieti e agitazione. I sintomi sono stati gestiti con la ripresa della fluvoxamina [2, 73] o trattati con clonazepam [72].
Citalopram
Sono stati riscontrati anche tre casi clinici che riportavano reazioni da astinenza in pazienti trattati con citalopram [74, 75, 76]. Tutti i soggetti che mostravano sindromi da astinenza hanno gradualmente interrotto il trattamento con citalopram. I sintomi sono comparsi entro 1-5 giorni dopo l’ultima dose e sono durati da 1 settimana [74] a 2 mesi [76]. I sintomi più comuni erano vertigini, ansia e irritabilità. Un soggetto ha anche sperimentato ipersensibilità dei genitali ed eiaculazione precoce [76].
Escitalopram
Casi clinici di sindrome da sospensione di escitalopram hanno coinvolto 2 pazienti [77, 78]. Un soggetto ha gradualmente ridotto l’escitalopram (in 3 settimane) [77], mentre l’altro ha prima saltato alcune dosi e poi ha ridotto il farmaco molto gradualmente (in 9 mesi) [78]. Entrambi hanno sperimentato sensazioni di shock elettrico pochi giorni dopo l’interruzione del farmaco, che sono durate da 5 giorni [77] a 4 settimane [78].
Discussione
Nonostante la letteratura limitata disponibile, i risultati di questa revisione sistematica indicano che i sintomi di astinenza possono verificarsi con qualsiasi tipo di SSRI (citalopram, escitalopram, fluoxetina, fluvoxamina, paroxetina e sertralina), anche se sono estremamente più frequenti con paroxetina. I sintomi quando la paroxetina è stata interrotta sono stati significativamente superiori al placebo nella maggior parte degli RCT che sono stati eseguiti [22, 32, 37, 38, 39, 40, 43, 44, 45].
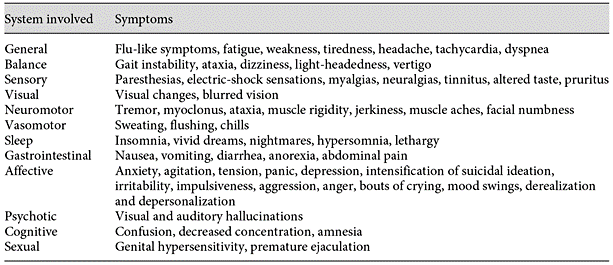
La durata del trattamento potrebbe essere di appena 2 mesi [33, 39, 42]. La prevalenza della sindrome era variabile e la sua stima era ostacolata dalla mancanza di identificazione del caso in molti studi. Il graduale scalaggio non elimina il rischio di reazioni da astinenza. In effetti, non è emerso un vantaggio significativo della riduzione graduale rispetto all’interruzione improvvisa [45, 46]. Può derivarne un’ampia gamma di manifestazioni cliniche che comprendono sintomi sia fisici che psicologici (riassunti nella tabella 1). Tali sintomi richiedono metodi di rilevamento adeguati (come DESS) e domande specifiche.
Ci sono molte somiglianze con i fenomeni di astinenza che caratterizzano gli antidepressivi di seconda generazione come la venlafaxina e la duloxetina [79, 80] e le benzodiazepine [27] ma si sovrappongono in modo più limitato a quelli che si verificano con gli antidepressivi triciclici [81].
La sindrome da astinenza si verifica in genere entro pochi giorni dall’interruzione del farmaco e dura alcune settimane. Tuttavia, sono possibili molte variazioni, inclusa l’insorgenza tardiva e/o la persistenza più lunga dei disturbi [9, 16, 68, 76].
Bhanji et al. [59] e Fava et al. [50] hanno documentato la persistenza dei sintomi fino a 1 anno dopo l’interruzione della paroxetina. Belise et al. [62] hanno descritto 3 casi di quelli che hanno definito come “disturbi persistenti post-astinenza indotti dalla paroxetina”. Tali disturbi sembrano essere abbastanza comuni sui siti Web dei pazienti [30] ma attendono un’adeguata esplorazione negli studi clinici.
I meccanismi fisiopatologici dei fenomeni di astinenza sono ancora ipotetici e necessitano di adeguate indagini neurobiologiche. Sono stati suggeriti numerosi meccanismi: una diminuzione della disponibilità di serotonina al termine del trattamento [82], una risposta allo stress comportamentale associata ad un aumento della densità del recettore N-metil- D-aspartato ippocampale [83] e vulnerabilità genetiche [84]. Gli studi sugli animali relativi all’uso a lungo termine dell’AD hanno implicazioni limitate, poiché non sono disponibili comportamenti chiari simili all’interruzione nei modelli animali [28].
Fava e Offidani [85] hanno interpretato i fenomeni di ritiro secondo il modello oppositivo della tolleranza. Il trattamento farmacologico continuato può reclutare processi che si oppongono agli effetti acuti iniziali di un farmaco e possono portare a una perdita di efficacia e/o a un decorso che non risponde al trattamento. Al termine del trattamento farmacologico, i processi oppositivi possono attivarsi per un certo tempo, determinando la comparsa di sintomi di astinenza e/o una maggiore vulnerabilità alla ricaduta e/o resistenza al trattamento (se viene ripristinato) e/o il passaggio a un decorso bipolare [85].
La comparsa di sintomi da astinenza dopo l’interruzione del trattamento con SSRI può quindi essere potenzialmente correlata a una serie di importanti fenomeni clinici [86]. Un editoriale pubblicato alla fine degli anni ’90 affermava che le reazioni all’interruzione dell’AD erano prevenibili e semplici da trattare [47]. Le prove che abbiamo appena raccolto indicano il contrario.
In primo luogo, la riduzione graduale degli SSRI sembra essere una strategia clinica ragionevole, ma non impedisce l’insorgenza di fenomeni di astinenza. Non abbiamo un insieme chiaro e specifico di caratteristiche sociodemografiche e cliniche che possono essere associate a una maggiore vulnerabilità.
In secondo luogo, il riconoscimento dei sintomi di astinenza richiede un’attenta esplorazione della potenziale sintomatologia (tabella 1 ) attraverso domande e/o strumenti specifici e la conoscenza dello stato di pretrattamento. I sintomi possono essere facilmente erroneamente identificati come segni di una ricaduta imminente. È probabile che i sintomi da astinenza abbiano un esordio precoce, mentre i sintomi ricorrenti generalmente si presentano con un ritorno graduale. Tuttavia, questa è solo una tendenza generale con disturbi dell’umore e non una regola, che comunque non si applica all’uso diffuso di SSRI nei disturbi d’ansia [87]. Il quadro clinico può essere complicato dal fatto che con l’SSRI possono verificarsi anche fenomeni di rebound (un rapido ritorno e un peggioramento dei sintomi originari del paziente) [86].
In terzo luogo, l’interruzione dell’SSRI può innescare fenomeni complessi, che possono o non possono essere correlati all’insorgenza della sintomatologia da astinenza, come ipomania o mania [85, 88] e disturbi post-astinenza persistenti [62]. Il termine comorbilità iatrogena si riferisce agli effetti duraturi che i trattamenti precedenti possono comportare (p. es., instabilità dell’umore ed elevata reattività agli stimoli ambientali nei disturbi post-astinenza persistenti), ben oltre il loro tempo di somministrazione [89, 90].
In quarto luogo, anche quando i sintomi da astinenza sono adeguatamente riconosciuti, la loro gestione clinica è ostacolata dalla complessità delle variabili coinvolte e dalla mancanza di una ricerca adeguata. Rassicurare i pazienti che è probabile che i sintomi siano di breve durata e non rappresentino una minaccia [26] è certamente un primo passo utile. Tuttavia, quando i sintomi persistono e sono angoscianti, la reintegrazione dello stesso AD che ha provocato il problema o la sua sostituzione con un SSRI a lunga durata d’azione come la fluoxetina [26] può solo posticipare e aggravare il problema [86].
Ci sono rapporti aneddotici sull’uso di clonazepam e altre benzodiazepine o stabilizzatori dell’umore, che, tuttavia, devono essere adeguatamente testati [15, 50, 59,62, 72]. Un’altra area di ricerca trascurata riguarda il ruolo dei sintomi di astinenza nella valutazione delle strategie di commutazione che sono sempre più utilizzate nel trattamento della resistenza dei disturbi dell’umore e dell’ansia [86, 91]. Gli effetti dei farmaci vengono attribuiti senza un’adeguata considerazione del ruolo confondente dei sintomi di astinenza.
Allo stesso modo, i disegni degli studi, come in un recente articolo sull’AD nella demenza [92], che valutano gli effetti dell’interruzione dell’AD per dedurre l’efficacia (cioè un aumento significativo dei sintomi depressivi nei pazienti la cui AD viene interrotta rispetto a quelli che continuare con il trattamento) sono viziati dalla mancata considerazione degli eventi di astinenza.
Il termine “sindrome da sospensione” ha progressivamente sostituito “sindrome da astinenza” nella letteratura sugli SSRI.
Questo cambiamento è stato fortemente sostenuto dall’industria farmaceutica [27, 88] e mirava a sottolineare che gli SSRI non causano dipendenza e che i sintomi sono sostanzialmente diversi dai fenomeni che si verificano con le benzodiazepine [24]. Tuttavia, Nielsen et al. [27] hanno dimostrato che ci sono somiglianze impressionanti tra SSRI e benzodiazepine a questo riguardo. Definire “sindromi da astinenza” come quelle relative alle benzodiazepine [27], ai farmaci antipsicotici [93] e agli antidepressivi triciclici [80] e “sindromi da sospensione” in quanto quelle di SSRI non sembrano riflettere l’evidenza in letteratura.
In effetti, l’uso di quest’ultimo termine ha minimizzato le potenziali vulnerabilità indotte dagli SSRI e ha fornito la base per indicazioni fuorvianti (ad esempio, l’AD è da preferire alle benzodiazepine nei disturbi d’ansia per mancanza di dipendenza) [94, 95]. I medici hanno familiarità con i fenomeni di astinenza che possono verificarsi da alcol, benzodiazepine, barbiturici, oppioidi e stimolanti [96]. I risultati di questa revisione indicano che è necessario aggiungere gli SSRI all’elenco dei farmaci che potenzialmente inducono fenomeni di astinenza. Il termine “sindrome da sospensione” riduce al minimo le vulnerabilità indotte da SSRI e dovrebbe essere sostituito da “sindrome da astinenza”.
Dichiarazione di divulgazione
Nessun autore ha accordi finanziari che potrebbero rappresentare potenziali conflitti di interesse per i risultati presentati.
Bibliografia
Vedi l’articolo originale disponibile a questo link