Anick Bérard PhD1, Michael Levin PhD2, Thomas Sadler PhD3,David Healy MD4
Pubblicato su Bioelectricity vol 1, n. 1, 2019
Traduzione in italiano a cura del Dott. Claudio Ajmone per GiùleManidaiBambini.org
Testo originale in inglese, disponibile a questo link
1. Faculty of Phamarcy, University of Montreal; Research center,CHU Sainte-Justine, Montreal, Quebrc, Canada.
2. Allen Discovery Center at Tufts University, Department of Biology, Medford, Massachusetts.
3. Department of Pediatrics, School of Medicine, University of Utah, Salt Lake City, Utah.
4. Department of Psychitry, Hergest Unit, Bangor, United Kingdom.
Riassunto
La segnalazione bioelettrica viene trasdotta dalle vie dei neurotrasmettitori in molti tipi di cellule. Uno dei mediatori chiave dei meccanismi di controllo bioelettrico è la serotonina e il suo trasportatore SERT, che è preso di mira da un’ampia classe di farmaci bloccanti (inibitori selettivi della ricaptazione della serotonina [SSRI]). Gli studi che mostrano un aumento del rischio di più malformazioni associate all’uso gestazionale di SSRI si sono accumulati, ma resta il dibattito sul fatto che l’SSRI come classe abbia il potenziale per generare queste malformazioni. Questa revisione evidenzia l’importanza della serotonina per lo sviluppo embrionale; l’effetto dell’inibizione della serotonina durante le prime fasi della gravidanza sul verificarsi di molteplici e diverse malformazioni che hanno dimostrato di verificarsi nelle gravidanze umane; che i rischi superano i benefici dell’uso di SSRI durante la gestazione nelle popolazioni di donne incinte da lievi a moderatamente depresse, che comprendono la maggior parte delle donne depresse in gravidanza; e che le malformazioni osservate nelle gravidanze umane costituiscono un modello di malformazioni coerente con i meccanismi d’azione noti degli SSRI. Presentiamo almeno tre meccanismi con cui SSRI può influenzare lo sviluppo. Questi studi evidenziano la rilevanza del meccanismo bioelettrico e dei neurotrasmettitori di base per la biomedicina.
Introduzione
I teratogeni sono fattori che alterano o interferiscono con lo sviluppo embrionale provocando malformazioni, morte, ritardo della crescita o deficit funzionali nell’embrione o nel feto.1 Che i farmaci possano agire come teratogeni umani è stato accettato dalle comunità mediche e scientifiche per >50 anni. Agenti come talidomide, acido retinoico e antiepilettici, per citarne alcuni, sono composti che sono teratogeni come dimostrato da metodi, principi e criteri epidemiologici. Recenti ricerche epidemiologiche hanno dimostrato che gli inibitori selettivi della ricaptazione della serotonina (SSRI), la classe più comunemente usata di antidepressivi, dal loro meccanismo comune che inibisce la ricaptazione della serotonina o della 5-idrossitriptamina (5-HT) da parte del trasportatore della serotonina (SERT o 5-HTT), aumentano il rischio di aborti spontanei, malformazioni congenite maggiori, ritardo della crescita intrauterina, prematurità e ritardo cognitivo.2-20
Oltre al fatto che si stanno accumulando dati che dimostrano il rischio di gravi malformazioni congenite associate all’uso di SSRI durante la gestazione, è stata messa in dubbio l’efficacia di questi farmaci per il trattamento della depressione. Ad esempio, a causa dell’aumento del metabolismo materno durante la gravidanza, il dosaggio del farmaco SSRI 21 deve essere aumentato per mantenere la stessa efficacia pregravidanza. 22 Tuttavia, le prove dimostrano che la maggior parte delle donne mantiene o riduce il dosaggio di SSRI una volta diagnosticata la gravidanza.21 Pertanto, se ci fossero benefici nell’uso di SSRI prima della gravidanza, questo non è più il caso durante la gravidanza. Inoltre, la maggior parte delle donne depresse è moderatamente depressa, 23 e il rischio per il nascituro dell’uso di SSRI supera i benefici in questa popolazione, dato che l’esercizio fisico o la psicoterapia sono ora noti per essere alternative efficaci all’assunzione dei farmaci.23
Secondo la classe farmacologica stabilita della Food and Drug Administration (FDA) degli Stati Uniti, 24 gli SSRI sono una classe farmacologica consolidata perché hanno tutti lo stesso meccanismo d’azione, che è quello di inibire la ricaptazione di 5-HT da parte di SERT, aumentando così le concentrazioni extracellulari del neurotrasmettitore. In base a questi criteri, i farmaci sertralina, paroxetina, citalopram, escitalopram e fluoxetina appartengono a questa classe farmacologica consolidata. 24 In effetti, tutti i farmaci con potenti effetti di inibizione della ricaptazione della serotonina costituiscono una classe – questo include gli SSRI ma anche la venlafaxina, la desvenlafaxina, la duloxetina e la clomipramina.
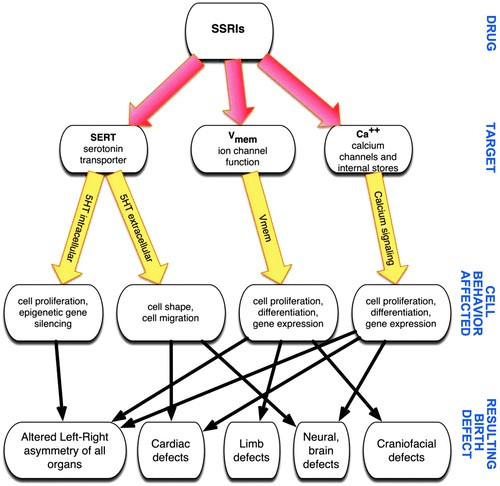
Questa revisione presenta le prove disponibili riguardanti gli effetti degli SSRI sul feto durante la gravidanza e il ruolo della 5-HT nel normale sviluppo embrionale. Noi postuliamo almeno tre tipi di meccanismi con cui gli SSRI possono influenzare lo sviluppo (Fig.1): alterando i livelli di serotonina endogena nei tessuti embrionali, alterazione della segnalazione dello sviluppo attraverso la modulazione dei canali ionici elettrogenici e perturbazione delle vie di segnalazione del calcio. Inoltre, vengono discussi l’impatto della depressione materna e l’efficacia e il rischio degli SSRI nella prevenzione o nel trattamento della depressione nelle donne in gravidanza. La sicurezza della prescrizione di SSRI per il trattamento della depressione e delle condizioni correlate nelle donne in età fertile è di fondamentale importanza per la salute pubblica, dati gli esiti potenzialmente gravi per il nascituro.
L’importanza della serotonina per il normale sviluppo embrionale
La serotonina non è solo un neurotrasmettitore, ma anche un mezzo profondamente importante per la comunicazione da cellula a cellula tra molti tipi di cellule durante l’embriogenesi. 25-27 È stato implicato in diversi eventi di sviluppo oltre ai suoi ruoli nella regolazione del sistema nervoso. 28-43 La maggior parte dei dati sul ruolo della serotonina durante l’embriogenesi sono derivati da sistemi modello, in cui possono essere eseguiti esperimenti funzionali definitivi che sono impossibili negli embrioni umani per ragioni etiche. Va tenuto presente che i meccanismi fondamentali della biologia cellulare e dei percorsi di sviluppo sono altamente conservati tra le specie di vertebrati; questo è il motivo per cui gli organismi dal lievito, al moscerino della frutta e alla rana sono responsabili di molte scoperte nella biomedicina umana (compresi i difetti alla nascita, la biologia delle cellule staminali e il cancro). Una gamma di modelli animali, inclusi mammiferi come roditori e conigli, insieme ad animali non mammiferi, come Xenopus (rana), pulcini e pesce zebra, forniscono informazioni vitali sui meccanismi comuni ed evolutivamente antichi che orchestrano i comportamenti delle singole cellule essenziali per il normale sviluppo.
Il pool di serotonina dell’embrione deriva da due fonti: zigotica e materna. Gli embrioni di mammiferi generano la propria serotonina molto presto, molto prima che compaia il sistema nervoso. Ad esempio, cellule staminali embrionali di topo sintetizzano 5-HT, 44 e sia 5-HT che SERT si trovano negli ovociti e negli embrioni allo stadio di scissione di molte specie. 45,46 Inoltre, la serotonina generata dalla madre viene trasmessa all’embrione in via di sviluppo attraverso l’assorbimento e il trasporto placentare. 43 Lavori recenti hanno dimostrato che la serotonina è una molecola di segnalazione chiave ed è un mezzo per la comunicazione tra le cellule durante l’embriogenesi. 28,29,35,36,42,47 Pertanto, una segnalazione appropriata richiede un delicato equilibrio e corrette concentrazioni di serotonina in posizioni specifiche. I livelli totali di 5-HT misurati nel sangue non sono sufficienti per rilevare squilibri in questo tipo di segnalazione perché i livelli rilevanti sono all’interno e adiacenti ai tipi di cellule chiave all’interno dell’embrione e non nella circolazione materna o fetale. Il fatto che gli SSRI attraversino prontamente la placenta 48 e il fatto che questi farmaci siano progettati per alterare le concentrazioni extracellulari di 5-HT creano una ricetta per interrompere questi delicati equilibri del neurotrasmettitore e, quindi, la sua capacità di agire come una molecola di segnalazione.
Segnali di serotonina in due modalità di base. Nella modalità extracellulare (Fig. 2A), la 5-HT arriva alla superficie delle cellule bersaglio per diffusione da posizioni esterne e attiva uno qualsiasi di una famiglia di sette recettori extracellulari della serotonina. 49 La fonte di serotonina può essere di tipo cellulare remoto, 29 o può effettivamente essere secreta e ricevuta dalla stessa cellula (segnalazione autocrina). Nella modalità intracellulare (Fig. 2B), la serotonina arriva via intracellulare tramite importazione mediata da SERT o attraverso canali di giunzione gap con le cellule vicine. 36,50-56 Livelli di divisione cellulare di controllo della serotonina intracellulare 57 dinamiche citoscheletriche, 58-60 secondi messaggeri (adenilato ciclasi e istone deacetilasi), 61-63 ed espressione genica dello sviluppo. Ciò avviene attraverso il legame alle proteine leganti la serotonina intracellulare, 64 inclusi Mad3 e 5-HT-R2, 65, 66 e la serotonilazione di una varietà di molecole chiave. 67-70
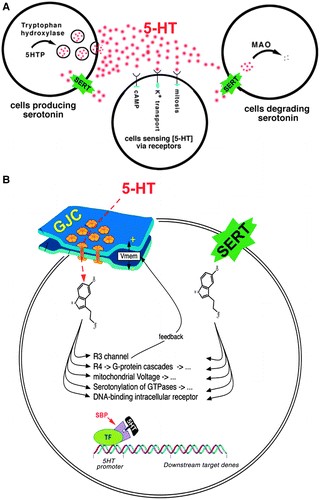
Figura. 2. Due modalità di base per i segnali di serotonina. (A) Modalità extracellulare. (B) modalità intracellulare.
La segnalazione della serotonina durante lo sviluppo partecipa a una serie di eventi di modellazione. Uno è l’istituzione della lateralità degli organi del corpo: il posizionamento invariante degli organi viscerali e del cuore. L’asimmetria coerente sinistra-destra (LR) è una caratteristica altamente conservata in anfibi, rettili, uccelli, pesci e mammiferi, che orientano tutti i loro cuori e organi viscerali con gli stessi orientamenti nel posizionamento e nella morfologia. In effetti, i segnali cellulari più elementari per stabilire la lateralità sono conservati tra molte specie diverse, comprese piante, nematodi, rane e umani. 47,71 Questa conservazione è importante perché significa che i meccanismi di base dell’asimmetria LR possono essere prontamente studiati negli organismi modello.72 Errori nello stabilire la lateralità provocano eterotassia e includono un’importante classe di difetti alla nascita umani con gravi implicazioni mediche per il paziente. 73-76
È stato dimostrato nei modelli di pulcino e rana che la segnalazione serotoninergica è necessaria affinché i lati sinistro e destro del corpo acquisiscano la loro identità e orientino adeguatamente organi asimmetrici come cuore, stomaco, fegato e altri. 28,35,36,42,65,77-79 Inoltre, la segnalazione serotoninergica controlla la proliferazione cellulare, la regolazione 80-85 della forma cellulare e dei modelli di movimento cellulare, 29,47,86-89 neurogenesi e schemi cerebrali, 90,91 morfogenesi del cuore, 92 sviluppo degli occhi, 93 e morfogenesi cranio-facciale. 39,94-96
Gli SSRI possono bloccare l’assorbimento della 5-HT da parte del cono ectoplacentare (placenta precoce nei roditori) e della placenta. 43 Èimportante sottolineare che la SERT, una proteina di membrana che trasporta la serotonina attraverso le membrane cellulari, agisce come un regolatore chiave della disponibilità di serotonina sia all’interno che all’esterno delle cellule. Sebbene il nome “inibitore della ricaptazione” per i composti che bloccano SERT si concentri sul trasporto di serotonina nelle cellule, SERT può anche funzionare al contrario per fornire una fonte di serotonina alle cellule circostanti. 97,98
Questo processo è fondamentale per la regolazione di alcuni tipi di derivati delle cellule staminali. 29 Pertanto, gli SSRI influenzano i meccanismi dipendenti dalla serotonina extracellulare (mediati dai tipi di recettori della membrana plasmatica 1–7) e i meccanismi dipendenti dalla serotonina intracellulare (marcatura epigenetica attraverso HDAC1 e serotonilazione di altre molecole di segnalazione). Non solo il sistema nervoso maturo, ma anche molte cellule embrionali iniziali utilizzano la serotonina come messaggero di segnalazione. 59,60,99-102 Pertanto, per progettazione e scopo, qualsiasi classe di farmaci SSRI influenzerà profondamente le concentrazioni di questa molecola chiave e quindi la segnalazione dipendente da 5-HT che è necessaria per completare l’embriogenesi normale.
Bioelettricità: un meccanismo teratogeno per gli SSRI in aggiunta alle vie serotoninergiche
Esiste un’altra modalità di azione mediante la quale gli SSRI possono perturbare l’embriogenesi, distinta dagli effetti primari sui livelli di SERT e serotonina. Numerosi studi hanno dimostrato che gli SSRI possono legarsi e modulare l’attività di numerosi canali ionici nelle cellule di mammifero, inclusi i canali del sodio, del cloruro e del potassio.103-115 Il legame a questi canali è rilevante per l’origine dei difetti alla nascita perché l’attività dei canali ionici, come la segnalazione serotoninergica, non è solo una funzione del sistema nervoso ma anche un meccanismo importante per coordinare i processi cellulari durante la morfogenesi embrionale di molti sistemi di organi. 116,117
I dati sulla bioelettricità dello sviluppo rivelano che i canali ionici creano campi elettrici endogeni modellati con precisione e gradienti di tensione che regolano la formazione del cuore, degli arti, del cervello, degli occhi e del viso. 118-127Le canalopatie umane (mutazioni che interrompono la segnalazione bioelettrica) hanno rivelato come l’interruzione dei canali ionici possa svolgere un ruolo nella causa dei difetti alla nascita, inclusa la sindrome di Andersen-Tawil, 128,129 malformazioni urogenitali, 130,131 Sindrome di Angelman, 132,133 Sindrome di Beckwith-Wiedemann, 134,136 e difetti del viso, 137 del cuore, del sistema nervoso centrale e del collo.138 Recentemente, Gelb e collaboratori 139 hanno scoperto numerose mutazioni del canale ionico, comprese alcune che coinvolgono canali direttamente modificati dagli SSRI, che provocano difetti alla nascita del cuore (inclusi difetti di lateralità predetti da precedenti lavori sulle rane 28,35,36,42,140-142) e dell’arto negli embrioni di topo. Questi dati confermano chiaramente che i risultati ottenuti dai modelli di rana sono direttamente rilevanti per lo sviluppo dei mammiferi.
I potenziali di riposo transmembrana (determinati da specifici canali ionici) regolano la proliferazione e la differenziazione in una gamma di popolazioni di cellule somatiche e staminali in vivo. 126,143 Le interazioni note degli SSRI con i canali ionici di sodio, potassio e cloruro 103,104,106,107,109,111,113-115 suggeriscono la probabilità che l’esposizione agli SSRI del feto perturbi la segnalazione bioelettrica ottimizzata che consente alle singole cellule di differenziarsi e disporsi in strutture anatomiche corrette. 144 Sulla base di questi effetti della 5-HT come molecola segnale che potenzialmente regola lo sviluppo di una varietà di sistemi di organi attraverso effetti sui processi cellulari generali, come la proliferazione e la migrazione, è facile capire come gli SSRI possano causare più tipi di difetti alla nascita. In effetti, questo risultato sembra essere esattamente ciò che si verifica, come dimostrato dagli studi epidemiologici. 5-9,11,13-15,145-147
A sua volta, questa molteplicità di difetti alla nascita “diluisce” i dati perché l’incidenza di ogni singolo difetto può essere bassa, rendendo difficile identificare associazioni statisticamente significative tra esposizione in utero al farmaco e teratogenicità. Tuttavia, la “serie” di difetti osservati dopo l’esposizione agli SSRI può rappresentare una singola classificazione di anomalie con un’origine comune, quindi un modello di malformazioni. Ad esempio, come affermato in precedenza, la 5-HT è un’importante molecola di segnalazione per stabilire la lateralità specificando l’asse sinistra-destra (LR) approssimativamente nei 14-16 giorni di gestazione nell’uomo (post concepimento). 28,35,36,42,65,77-79 La creazione di questo asse è essenziale per il normale sviluppo e le interruzioni in questo processo, come possono essere causati dagli SSRI, con conseguente eterotassia. Gli individui con questa condizione presentano anomalie nel posizionamento dei sistemi di organi, inclusi milza, cuore, fegato e intestino, e un’ampia varietà di difetti alla nascita. 75,148-152
L’organo più sensibile alle interruzioni nella segnalazione della lateralità è il cuore 73,151 e praticamente ogni tipo di difetto cardiaco può verificarsi quando questa segnalazione è alterata, inclusi difetto del setto atriale, difetto del setto ventricolare, ventricolo destro a doppia uscita, ventricoli sinistro ipoplastico, ipoplasia destra ventricoli, tetralogia di Fallot, ventricolo singolo, inversioni e isomerismi atriali, inversioni ventricolari e trasposizione delle grandi arterie tra gli altri. 73,149,153-155 Può anche verificarsi una varietà di altri difetti, in particolare difetti vascolari, come il ritorno venoso polmonare anomalo totale. 14,156 Esiste anche un legame tra anomalie della lateralità e difetti della linea mediana che è stato documentato nella letteratura clinica almeno dalla metà degli anni ’90.
Tutti i tipi di difetti della linea mediana sono stati osservati in pazienti con anomalie della lateralità, inclusi difetti del tubo neurale, labbro leporino e palato, gastroschisi, onfalocele, atresia e stenosi anale e disgenesia caudale. 75,148-152,156 In effetti, i difetti della linea mediana si verificano così comunemente quando la segnalazione della lateralità viene interrotta che se un paziente ha un difetto della linea mediana, è stato stimato che hanno 3 volte più probabilità di avere un problema di lateralità rispetto ai pazienti senza un difetto della linea mediana e 100 volte in più rispetto alla popolazione generale. 148,151 Inoltre, poiché molti pazienti non vengono mai valutati in modo specifico per problemi di lateralità, è probabile che questi tassi siano sottostimati. Ancora più importante, gli individui con difetti della linea mediana non richiedono che le anomalie della lateralità siano classificate come aventi interrotto la segnalazione della lateralità come eziologia primaria della loro malformazione della linea mediana.
Questo punto è stato dimostrato in studi su membri della famiglia con mutazioni note ai geni della lateralità. In tali famiglie, un’alta incidenza di membri della famiglia mostra solo una singola malformazione della linea mediana, come la palatoschisi o un difetto del tubo neurale, senza altre anomalie. 151,152,156 Il motivo per cui i difetti della linea mediana sono comuni è probabilmente dovuto al fatto che, man mano che lo sviluppo procede, i diversi assi, compreso quello anteriore-posteriore (cranio-caudale), dorso-ventrale e LR, devono essere coordinati nello specificare l’origine e la posizione del i diversi sistemi di organi. 152,157-159 Pertanto, se un asse, come quello LR, è anormale, interrompe lo sforzo coordinato e si traduce in una varietà di difetti, alcuni dei quali potrebbero non sembrare correlati direttamente agli effetti sull’asse mirato. Quindi, potrebbe verificarsi un difetto della linea mediana a causa di un’interruzione nella segnalazione della lateralità. Pertanto, gli SSRI possono produrre una varietà di difetti alla nascita attraverso un meccanismo comune di alterazione delle concentrazioni di 5-HT e attraverso un percorso comune di interruzione della segnalazione di 5-HT responsabile della creazione dell’asse LR a 14-16 giorni di gestazione. Questa spiegazione spiega prontamente la varietà di difetti apparentemente non correlati osservati alla nascita dopo l’esposizione agli SSRI in utero.
SSRI e malformazioni congenite maggiori negli esseri umani
I sintomi depressivi sono comuni durante la gravidanza e gli SSRI sono gli antidepressivi più utilizzati per il trattamento delle donne in gravidanza 21,160,161 Studi riguardanti gli effetti avversi dell’esposizione a SSRI durante la gestazione sul feto in via di sviluppo hanno indicato un aumento del rischio di varie malformazioni congenite, 2,5-10,18 ma permangono incongruenze tra i risultati degli studi. 11-13,162,163 Questi potrebbero essere potenzialmente spiegati da bias di indicazione in cui l’effetto del farmaco e l’indicazione sono correlati e non completamente spiegati, 6,145,164 o errori di classificazione in cui l’esposizione e / o la valutazione del risultato non sono state convalidate. 165
L’uso gestazionale di SSRI è stato associato ad un aumentato rischio di varie malformazioni congenite maggiori.2,5-14,18 Ciò è stato ripetutamente dimostrato in ampi studi basati sulla popolazione ben progettati con sufficiente potenza statistica. Infatti, negli ultimi 20 anni, i dati sul rischio di malformazioni associate all’esposizione intrauterina agli SSRI si sono accumulati, ancora di più dopo il 2005, quando è stato emesso l’allarme sul rischio di difetti cardiaci associati all’esposizione alla paroxetina durante la gravidanza. 166 Sebbene l’entità del rischio vari da uno studio all’altro e tra i sistemi di organi, rimane che già a metà degli anni ’90 erano disponibili segnali sufficienti sul rischio di malformazioni congenite maggiori sull’esposizione agli SSRI della gravidanza umana.
Nel complesso, gli SSRI come classe e i farmaci SSRI-specifici aumentano il rischio di malformazioni congenite maggiori di almeno il 30% durante la gravidanza (aumento del rischio del 30-130%), 2,7,9,10,13,15,18 il rischio aumenta anche con l’aumentare del dosaggio, il che è a sostegno di una relazione dose-risposta, 6,15 e una maggiore durata dell’uso durante la gravidanza, che è coerente con un effetto cumulativo. 10 Sebbene alcuni studi non abbiano potere statistico, la maggior parte delle stime del rapporto di rischio è > 1, indicando un aumento del rischio. Anche dopo aver considerato il potenziale di bias, confusione e riscontro casuale, la letteratura basata sull’evidenza dimostra che l’esposizione prenatale agli SSRI come classe causa un aumento del rischio di malformazioni congenite nei bambini esposti in utero durante il periodo critico dello sviluppo. Dato che le malformazioni maggiori sono rare, si dovrebbe dare più peso alle ripetizioni di reperti o difetti con meccanismi d’azione noti rispetto alla significatività statistica, che dipende esclusivamente dal numero di casi esposti. 164
Gli SSRI come classe aumentano il rischio di malformazioni cardiache maggiori di almeno il 60% rispetto al non utilizzo durante la gravidanza. 2,7,9,14,15,18,146 Le prove pubblicate sottoposte a revisione paritaria su sertralina, fluoxetina, citalopram, escitalopram e paroxetina dimostrano costantemente un aumento del rischio di malformazioni cardiache da un aumento del 9% a più di quattro volte il rischio osservato nei non utilizzatori. Sebbene alcuni difetti cardiaci siano più rari e richiederebbero un campione di dimensioni molto grandi, che sarebbe molto difficile da acquisire, esistono prove su alcuni tipi specifici di difetti cardiaci. Quindi, SSRI come classe e l’uso di farmaci specifici per SSRI durante la gestazione sono stati associati a un aumentato rischio di difetti del setto atriale e ventricolare, 2,5-9,11,14,15,18,145,164 ostruzione delle tracce di deflusso ventricolare destro e sinistro, 5,8,18 difetti tronconali, 5,8 trasposizione delle grandi arterie, 5 tetralogia di Fallot, 5 stenosi della valvola polmonare, 5 e arteriosi del dotto pervio. 14
È stato anche dimostrato che gli SSRI aumentano il rischio di craniosinostosi (gli odds ratio vanno da 1,94 a 2,5). 2,5,8,15,145 Da notare, il periodo critico di sviluppo della craniosinostosi può estendersi oltre il primo trimestre, come mostrato da Alwan et al. 5 che hanno stimato un aumento del 90% del rischio associato all’esposizione del secondo e terzo trimestre agli SSRI. Tuttavia, Berard et al. 145 ha mostrato che l’esposizione in qualsiasi momento durante la gravidanza non ha modificato i risultati. L’SSRI come classe aumenta anche il rischio di difetti gastrointestinali (onfalocele, gastroschisi, atresia esofagea, atresia anale, stenosi pilorica ipertrofica e reflusso vescicouretico) 5,8,14,15; difetti del tubo neurale (anencefalia e spina bifida) 5,8,11; labbro leporino con o senza palato 8,11,14; difetti degli arti 5,8,14,167; e altri difetti come ernia diaframmatica, 5,8 ipospadia, 8 testicoli ritenuti, 8 e malattia renale cistica.14 Tutti questi fenotipi sono potenziali esiti di segnali serotoninergici, bioelettrici e di calcio perturbati. Inoltre, vi sono prove coerenti che dimostrano che gli SSRI come classe raddoppiano almeno il rischio di ipertensione polmonare persistente del neonato. 168-171
Infine, è stato scoperto che gli SSRI come classe e tutti i farmaci specifici per SSRI aumentano il rischio di aborti spontanei. 3,4,172 Dato che gli embrioni con gravi malformazioni sono prevalentemente abortiti, 164 questo suggerisce che il vero impatto degli antidepressivi sull’insorgenza di difetti è molto più alto di quanto sarebbe evidente dall’esame degli embrioni sopravvissuti alla nascita. In sintesi, è stato costantemente dimostrato che gli SSRI considerati separatamente o come una classe aumentano il rischio di malformazioni congenite maggiori in generale e di malformazioni dei principali sistemi d’organo in particolare, anche dopo aver considerato la diversa entità degli effetti riportati negli studi. I difetti osservati alla nascita hanno origini embrionali simili e possono essere considerati un pattern di malformazioni come già spiegato.
Il ruolo della depressione
Recenti recensioni di problemi di salute mentale prenatale rilevano che il 35% delle donne incinte ha sintomi depressivi e si afferma che il 10% di loro sia depresso. 173 Un problema con questa formulazione è che avere sintomi, anche se soddisfano tutti i criteri operativi per la depressione, non significa necessariamente che una persona sia depressa. La prevalenza puntuale della depressione maggiore è del 3,8% alla fine del primo trimestre, del 4,9% alla fine del secondo trimestre e del 3,1% alla fine del terzo trimestre di gravidanza invece del 10-15% riportato di routine. 174 Quando vengono avanzate argomentazioni per il trattamento della depressione prenatale, si afferma che la depressione non trattata porta al fumo, all’assunzione di alcol e droghe, scarsa cura di sé, suicidio e depressione postnatale. 175 Inoltre, deducono che potrebbe esserci un effetto tossico diretto della depressione non trattata sul feto. 176 Infine, indicano gli effetti sullo sviluppo del bambino in età avanzata, sostenendo che questi sono sostanziali e deleteri. 177 Non sono noti effetti tossici diretti della depressione prenatale sul feto. Non sono noti cambiamenti endocrini legati alla maggior parte dei disturbi nervosi comuni che colpiscono le donne in gravidanza e che potrebbero interessare il feto. La depressione materna durante la gravidanza non è associata al rischio di malformazioni congenite, quindi non è un fattore di rischio per malformazioni. Tuttavia, gli stili di vita associati alla depressione materna, come il fumo, 178 consumo di alcol, 179 e la mancanza di acido folico, 180 sono stati implicati nel verificarsi di importanti malformazioni congenite. Pertanto, la depressione materna viene spesso utilizzata come premonitrice per gli stili di vita associati.
Le madri che sono depresse durante la gravidanza sono, tuttavia, ad aumentato rischio di depressione post-partum, 181 e hanno una minore attaccamento madre-bambino dopo il parto. 182 Se la depressione prenatale porta a una depressione postnatale, c’è sempre l’opportunità di trattare il disturbo depressivo vigorosamente in quel momento senza rischi per il feto. Tuttavia, la depressione deve essere monitorata durante la gestazione e un trattamento appropriato (esercizio fisico e psicoterapia) 183,184 deve essere considerato. Inoltre, gli SSRI vengono trasferiti nel latte materno se utilizzati durante il periodo postnatale e quindi hanno il potenziale per avere un impatto sui neonati durante questa finestra di tempo.
Efficacia degli SSRI durante la gravidanza
Fino all’avvento degli SSRI, il termine depressione in generale si riferiva a una condizione più grave rispetto a quella a cui si riferisce ora il disturbo depressivo maggiore (MDD). Questa condizione più grave era originariamente chiamata melanconia, per poi diventare depressione endogena. Sappiamo poco sui rischi di non curare disturbi depressivi classici o gravi di questo tipo. La melanconia è estremamente rara nelle donne in gravidanza o in età fertile. Gli SSRI non vengono somministrati per i disturbi depressivi classici o gravi poiché i farmaci non sono efficaci nel trattamento di queste condizioni. Questi farmaci sono meno efficaci dei vecchi antidepressivi come la clomipramina per i disturbi depressivi più gravi. Gli SSRI sono commercializzati e somministrati a donne con ansia e sintomi depressivi. La mancanza di prove sull’efficacia o l’efficacia della terapia con SSRI, insieme al fatto che numerosi studi hanno documentato i loro effetti dannosi sullo sviluppo embrionale e fetale impone di raccomandare interventi non farmacologici alternativi alle donne in gravidanza con il ricorso ai farmaci come opzione secondaria. Allo stato attuale, viene data poca considerazione ai trattamenti non farmacologici di provata efficacia, come l’esercizio 183 o psicoterapia. 184
Nel 2006, la FDA ha tenuto udienze sulla questione degli avvertimenti riguardanti il suicidio sulla base dei dati provenienti da studi su adulti di antidepressivi inclusi tutti gli SSRI. Questi studi in totale contenevano quasi 100.000 pazienti, > 50.000 dei quali erano pazienti depressi. A parte la questione degli atti suicidari, i dati di tutti gli studi clinici a breve termine controllati con placebo sugli adulti per il MDD negli ultimi 15-20 anni mostrano che gli antidepressivi in generale hanno un’efficacia minima. Quando i dati di tutti gli studi randomizzati vengono combinati, 5 pazienti su 10 rispondono ai farmaci, ma negli stessi studi 4 pazienti su 10 rispondono al placebo. 185 Pertanto, solo 1 paziente su 10 sottoposto al trattamento risponde in modo specifico al farmaco a cui è stato somministrato, mentre 5 su 10 non rispondono o rispondono negativamente. 185 L’elevata risposta al placebo significa che in molti casi la storia naturale dei disturbi depressivi deve risolversi spontaneamente; in altri casi, la dieta e l’igiene forniranno trattamenti efficaci o l’assistenza del medico del paziente per aiutare a risolvere i problemi a casa o al lavoro risolverà il problema. Pertanto, i risultati basati sull’evidenza dimostrano che in tutti i casi, non solo nel caso di pazienti in gravidanza, gli SSRI non sono un protocollo di trattamento efficace per la depressione e dovrebbero essere utilizzati solo per i pazienti che non rispondono a un approccio conservativo. Inoltre, le questioni riguardanti l’efficacia e il potenziale di danneggiare i bambini dovrebbero essere chiarite alle donne in gravidanza in modo che possano optare per un trattamento alternativo.
Nel caso in cui si giudichi che un particolare stato di ansia o depressione prenatale richieda un trattamento attivo piuttosto che semplicemente impiegare misure di monitoraggio, trattamenti come la terapia interpersonale (IPT) e la terapia cognitivo comportamentale, che per questo livello di gravità sono efficaci quanto il trattamento farmacologico, può essere considerato. Infatti, dato il ruolo dei fattori sociali associati agli stati nervosi riscontrati durante la gravidanza, l’IPT originatosi come trattamento per la depressione postnatale sembra essere particolarmente indicato per i disturbi prenatali. 186 Per i disturbi depressivi da moderati a gravi o malinconici, le linee guida come quelle emesse dal National Institute for Health and Clinical Excellence (NICE) raccomandano antidepressivi triciclici piuttosto che SSRI. 187
Conclusione
I criteri di Bradford Hill 188 sono utili per valutare la causalità tra un’esposizione e un risultato. Sebbene questi criteri siano utilizzati per valutare il nesso di causalità, non tutti devono essere soddisfatti per stabilire il nesso di causalità generale. L’evidenza indica che l’uso di SSRI durante la gravidanza interrompe e / o disturba eventi essenziali durante la fase embrionale e l’organogenesi, che avvia una cascata di eventi che causano aborti spontanei e malformazioni congenite maggiori. L’evidenza epidemiologica nell’uomo è coerente e i risultati sono stati replicati in diverse popolazioni di pazienti; è stata anche stabilita una dose-risposta. Malformazioni identificate che hanno tutte origini embrionali simili e quindi dimostrano un modello di malformazione. I dati meccanicistici dimostrano inequivocabilmente che tre principali percorsi noti per essere cruciali per la modellazione di molti sistemi di organi embrionali, la segnalazione serotoninergica, la segnalazione bioelettrica e la segnalazione del calcio possono essere perturbati dagli SSRI.
L’importanza di questi percorsi nella regolazione del comportamento cellulare e di molteplici sistemi di modellazione durante l’embriogenesi suggerisce chiaramente che gli SSRI hanno il potenziale per causare difetti alla nascita. Dato che tutti gli SSRI hanno un meccanismo d’azione simile, dovrebbero essere considerati come una classe di composti che producono gli stessi effetti negativi sullo sviluppo. L’importanza di questi percorsi nella regolazione del comportamento cellulare e di molteplici sistemi di modellazione durante l’embriogenesi suggerisce chiaramente che gli SSRI hanno il potenziale per causare difetti alla nascita. Dato che tutti gli SSRI hanno un meccanismo d’azione simile, dovrebbero essere considerati come una classe di composti che producono gli stessi effetti negativi sullo sviluppo. L’importanza di questi percorsi nella regolazione del comportamento cellulare e di molteplici sistemi di modellazione durante l’embriogenesi suggerisce chiaramente che gli SSRI hanno il potenziale per causare difetti alla nascita. Dato che tutti gli SSRI hanno un meccanismo d’azione simile, dovrebbero essere considerati come una classe di composti che producono gli stessi effetti negativi sullo sviluppo.
Non è stato dimostrato che la depressione materna aumenti il rischio di malformazioni congenite maggiori. La maggior parte delle donne incinte depresse presenta una depressione da lieve a moderata per la quale gli SSRI sono inefficaci. Al momento, il rapporto rischio-beneficio non supporta l’uso di SSRI durante la gravidanza. È importante monitorare la depressione, ma le terapie non farmacologiche, come l’esercizio fisico o la psicoterapia, dovrebbero essere considerate come trattamento di prima linea durante il periodo gestazionale. Più in generale, a causa della stretta relazione tra la segnalazione mediata dal canale ionico e le fasi di trasduzione del neurotrasmettitore a valle che operano durante lo sviluppo, i dati meccanicistici ed epidemiologici sugli SSRI servono come un esempio primario dell’interazione tra il lavoro di base nella bioelettricità dello sviluppo e la biomedicina.
Ringraziamenti
ML è grato per il supporto della March of Dimes e dell’American Heart Association.
Contributi degli autori
Il concetto e il design di questo studio sono stati realizzati da AB, ML, TS e DH; l’articolo è stato redatto da AB, ML, TS e DH; e la revisione critica dell’articolo e il contenuto intellettuale importante sono stati eseguiti da AB, ML, TS e DH Tutti i coautori hanno esaminato e approvato l’articolo prima della presentazione.
Disclaimer
L’articolo è stato inviato esclusivamente a questa rivista e non è pubblicato, in stampa o presentato altrove.
Dichiarazione di divulgazione dell’autore
Tutti gli autori sono consulenti per i querelanti nel contenzioso che coinvolge antidepressivi. AB è titolare di una cattedra di ricerca su farmaci e gravidanza del Fonds de la Recherche du Québec – Santé (FRQS).
Bibliografia
- Wilson JG. Teratogenic effects of environmental chemi- cals. Fed Proc 1977;36:1698–1703.
- Berard A, Zhao JP, Sheehy O. Antidepressant use during pregnancy and the risk of major congenital malformations in a cohort of depressed pregnant women: An updated analysis of the Quebec Pregnancy Cohort. BMJ Open 2017;7:e013372.
- Nakhai-Pour HR, Broy P, et al. Use of antidepressants during pregnancy and the risk of spontaneous abortion. CMAJ 2010;182:1031–1037.
- Einarson A, Choi J, Einarson TR, et al. Rates of sponta- neous and therapeutic abortions following use of antide- pressants in pregnancy: Results from a large prospective database. J Obstet Gynaecol Can 2009;31:452–456.
- Alwan S, Reefhuis J, Rasmussen SA, et al. Use of selec- tive serotonin-reuptake inhibitors in pregnancy and the risk of birth defects. N Engl J Med 2007;356:2684– 2692.
- Berard A, Ramos E, Rey E, et al. First trimester exposure to paroxetine and risk of cardiac malformations in infants: The importance of dosage. Birth Defects Res B Dev Re- prod Toxicol 2007;80:18–27.
- Kornum JB, Nielsen RB, Pedersen L, et al. Use of se- lective serotonin-reuptake inhibitors during early preg- nancy and risk of congenital malformations: Updated analysis. Clin Epidemiol 2010;2:29–36.
- Louik C, Lin AE, Werler MM, et al. First-trimester use of selective serotonin-reuptake inhibitors and the risk of birth defects. N Engl J Med 2007;356:2675–2683.
- Pedersen LH, Henriksen TB, Vestergaard M, et al. Selective serotonin reuptake inhibitors in pregnancy and congenital malformations: Population based cohort study. BMJ 2009;339:b3569.
- Wogelius P, Norgaard M, Gislum M, et al. Maternal use of selective serotonin reuptake inhibitors and risk of congenital malformations. Epidemiology 2006;17:701–704.
- Malm H, Artama M, Gissler M, et al. Selective serotonin reuptake inhibitors and risk for major congenital anoma- lies. Obstet Gynecol 2011;118:111–120.
- Nordeng H, van Gelder MM, Spigset O, et al. Pregnancy outcome after exposure to antidepressants and the role of maternal depression: Results from the Norwegian Mother and Child Cohort Study. J Clin Psychopharmacol 2012; 32:186–194.
- Reis M, Kallen B. Delivery outcome after maternal use of antidepressant drugs in pregnancy: An update using Swedish data. Psychol Med 2010;40:1723–1733.
- Colvin L, Slack-Smith L, Stanley FJ, et al. Dispensing patterns and pregnancy outcomes for women dispensed selective serotonin reuptake inhibitors in pregnancy. Birth Defects Res A Clin Mol Teratol 2011;91:142–152.
- Jimenez-Solem E, Andersen JT, Petersen M, et al. Ex- posure to selective serotonin reuptake inhibitors and the risk of congenital malformations: A nationwide cohort study. BMJ Open 2012;2; DOI:10.1136/bmjopen-2012- 001148.
- Ramos E, St-Andre M, Berard A. Association between antidepressant use during pregnancy and infants born small for gestational age. Can J Psychiatry 2010;55:643–652.
- Huybrechts KF, Sanghani RS, Avorn J, et al. Preterm birth and antidepressant medication use during preg- nancy: A systematic review and meta-analysis. PLoS One 2014;9:e92778.
- Berard A, Iessa N, Chaabane S, et al. The risk of major cardiac malformations associated with paroxetine use during the first trimester of pregnancy: A systematic re- view and meta-analysis. Br J Clin Pharmacol 2016;81: 589–604.
- Healy D, Le Noury J, Mangin D. Links between serotonin reuptake inhibition during pregnancy and neurodevelop- mental delay/spectrum disorders: A systematic review of epidemiological and physiological evidence. Int J Risk Saf Med 2016;28:125–141.
- Boukhris T, Berard A. Selective serotonin reuptake inhib- itor use during pregnancy and the risk of autism spectrum disorders: A review. J Pediatr Genet 2015;4:84–93.
- Ramos E, Oraichi D, Rey E, et al. Prevalence and pre- dictors of antidepressant use in a cohort of pregnant wo- men. BJOG 2007;114:1055–1064.
- Berard A, Gaedigk A, Sheehy O, et al. Association between CYP2D6 genotypes and the risk of antidepressant discontinuation, dosage modification and the occurrence of maternal depression during pregnancy. Front Pharma- col 2017;8:402.
- Shorter E. The 25th anniversary of the launch of Prozac gives pause for thought: Where did we go wrong? Br J Psychiatry 2014;204:331–332.
- FDA Established Pharmacologic Class (EPC). www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatory Information/LawsActsandRules/UCM428333.pdf (last accessed June 15, 2018).
- Buznikov GA, Lambert HW, Lauder JM. Serotonin and serotonin-like substances as regulators of early embryo- genesis and morphogenesis. Cell Tissue Res 2001;305: 177–186.
- Buznikov GA, Shmukler YB. Possible role of ‘‘prenervous’’ neurotransmitters in cellular interactions of early embryogenesis: A hypothesis. Neurochem Res 1981; 6:55–68.
- Levin M, Buznikov GA, Lauder JM. Of minds and embryos: Left-right asymmetry and the serotonergic controls of pre-neural morphogenesis. Dev Neurosci 2006;28:171– 185.
- Adams DS, Robinson KR, Fukumoto T, et al. Early, H+-V-ATPase-dependent proton flux is necessary for consistent left-right patterning of non-mammalian verte- brates. Development 2006;133:1657–1671.
- Blackiston D, Adams DS, Lemire JM, et al. Transmembrane potential of GlyCl-expressing instructor cells in- duces a neoplastic-like conversion of melanocytes via a serotonergic pathway. Dis Model Mech 2011;4:67–85.
- Choi DS, Birraux G, Launay JM, et al. The human serotonin 5-HT2B receptor: Pharmacological link between 5-HT2 and 5-HT1D receptors. FEBS Lett 1994;352:393–399.
- Choi DS, Colas JF, Kellermann O, et al. The mouse 5-HT2B receptor: Possible involvement in trophic functions of serotonin. Cell Mol Biol (Noisy-le-grand) 1994;40: 403–411.
- Choi DS, Kellermann O, Richard S, et al. Mouse 5-HT2B receptor-mediated serotonin trophic functions. Ann N Y Acad Sci 1998;861:67–73.
- Choi DS, Maroteaux L. Immunohistochemical locali- sation of the serotonin 5-HT2B receptor in mouse gut, cardiovascular system, and brain. FEBS Lett 1996;391: 45–51.
- Choi DS, Ward SJ, Messaddeq N, et al. 5-HT2B receptor- mediated serotonin morphogenetic functions in mouse cranial neural crest and myocardiac cells. Development 1997;124:1745–1755.
- Fukumoto T, Blakely R, Levin M. Serotonin transporter function is an early step in left-right patterning in chick and frog embryos. Dev Neurosci 2005;27:349–363.
- Fukumoto T, Kema IP, Levin M. Serotonin signaling is a very early step in patterning of the left-right axis in chick and frog embryos. Curr Biol 2005;15:794–803.
- Launay JM, Birraux G, Bondoux D, et al. Ras involve- ment in signal transduction by the serotonin 5-HT2B re- ceptor. J Biol Chem 1996;271:3141–3147.
- Rea AC, Vandenberg LN, Ball RE, et al. Light-activated serotonin for exploring its action in biological systems. Chem Biol 2013;20:1536–1546.
- Shuey DL, Sadler TW, Lauder JM. Serotonin as a regulator of craniofacial morphogenesis: Site specific mal- formations following exposure to serotonin uptake inhibitors. Teratology 1992;46:367–378.
- Shuey DL, Sadler TW, Tamir H, et al. Serotonin and morphogenesis. Transient expression of serotonin uptake and binding protein during craniofacial morphogenesis in the mouse. Anat Embryol (Berl) 1993;187:75–85.
- Shuey DL, Yavarone M, Sadler TW, et al. Serotonin and morphogenesis in the cultured mouse embryo. Adv Exp Med Biol 1990;265:205–215.
- Vandenberg LN, Lemire JM, Levin M. Serotonin has early, cilia-independent roles in Xenopus left-right pat- terning. Dis Model Mech 2013;6:261–268.
- Yavarone MS, Shuey DL, Sadler TW, et al. Serotonin uptake in the ectoplacental cone and placenta of the mouse. Placenta 1993;14:149–161.
- Walther DJ, Bader M. Serotonin synthesis in murine embryonic stem cells. Brain Res Mol Brain Res 1999;68: 55–63.
- Amireault P, Dube F. Serotonin and its antidepressant sensitive transport in mouse cumulus-oocyte complexes and early embryos. Biol Reprod 2005;73:358–365.
- Dube F, Amireault P. Local serotonergic signaling in mammalian follicles, oocytes and early embryos. Life Sci 2007;81:1627–1637.
- Lobikin M, Chernet B, Lobo D, et al. Resting potential, oncogene-induced tumorigenesis, and metastasis: The bio- electric basis of cancer in vivo. Phys Biol 2012;9:065002.
- Rampono J, Simmer K, Ilett KF, et al. Placental transfer of SSRI and SNRI antidepressants and effects on the neo- nate. Pharmacopsychiatry 2009;42:95–100.
- Noda M, Higashida H, Aoki S, et al. Multiple signal transduction pathways mediated by 5-HT receptors. Mol Neurobiol 2004;29:31–39.
- Blomstrand F, Aberg ND, Eriksson PS, et al. Extent of intercellular calcium wave propagation is related to gap junction permeability and level of connexin-43 expression in astrocytes in primary cultures from four brain regions. Neuroscience 1999;92:255–265.
- Esser AT, Smith KC, Weaver JC, et al. Mathematical model of morphogen electrophoresis through gap junc- tions. Dev Dyn 2006;235:2144–2159.
- Gairhe S, Bauer NN, Gebb SA, et al. Serotonin passes through myoendothelial gap junctions to promote pul- monary arterial smooth muscle cell differentiation. Am J Physiol Lung Cell Mol Physiol 2012;303:L767–L777.
- Hou M, Li Y, Paul DL. A novel, highly sensitive method for assessing gap junctional coupling. J Neurosci Methods 2013;220:18–23.
- Sun JD, Liu Y, Yuan YH, et al. Gap junction dysfunction in the prefrontal cortex induces depressive-like behaviors in rats. Neuropsychopharmacology 2012;37:1305–1320.
- Wolszon LR, Gao WQ, Passani MB, et al. Growth cone ‘‘collapsÈ’ in vivo: Are inhibitory interactions mediated by gap junctions? J Neurosci 1994;14:999–1010.
- Zhang Y, Levin M. Particle tracking model of electro- phoretic morphogen movement reveals stochastic dy- namics of embryonic gradient. Dev Dyn 2009;238:1923– 1935.
- Berg DA, Belnoue L, Song H, et al. Neurotransmitter- mediated control of neurogenesis in the adult vertebrate brain. Development 2013;140:2548–2561.
- Buskohl PR, Sun MJ, Thompson RP, et al. Serotonin potentiates transforming growth factor-beta3 induced biomechanical remodeling in avian embryonic atrioven- tricular valves. PLoS One 2012;7:e42527.
- Liu Y, Wei L, Laskin DL, et al. Role of protein transa- midation in serotonin-induced proliferation and migration of pulmonary artery smooth muscle cells. Am J Respir Cell Mol Biol 2011;44:548–555.
- Pai VP, Marshall AM, Hernandez LL, et al. Altered se- rotonin physiology in human breast cancers favors para- doxical growth and cell survival. Breast Cancer Res 2009; 11:R81.
- Kretsovali A, Hadjimichael C, Charmpilas N. Histone deacetylase inhibitors in cell pluripotency, differentiation, and reprogramming. Stem Cells Int 2012;2012:184154.
- Menegola E, Di Renzo F, Broccia ML, et al. Inhibition of histone deacetylase as a new mechanism of teratogenesis. Birth Defects Res C Embryo Today 2006;78:345–353.
- Tresguerres M, Levin LR, Buck J. Intracellular cAMP signaling by soluble adenylyl cyclase. Kidney Int 2011; 79:1277–1288.
- Del Rio MJ, Velez-Pardo C, Ebinger G, et al. Serotonin binding proteins ‘‘SBP’’: Target proteins and tool for in vitro neurotoxicity studies. Gen Pharmacol 1995;26: 1633–1641.
- Carneiro K, Donnet C, Rejtar T, et al. Histone deacetylase activity is necessary for left-right patterning during ver- tebrate development. BMC Dev Biol 2011;11:29.
- Cornea-Hebert V, Riad M, Wu C, et al. Cellular and subcellular distribution of the serotonin 5-HT2A receptor in the central nervous system of adult rat. J Comp Neurol 1999;409:187–209.
- Hummerich R, Schloss P. Serotonin—more than a neu- rotransmitter: Transglutaminase-mediated serotonylation of C6 glioma cells and fibronectin. Neurochem Int 2010; 57:67–75.
- Paulmann N, Grohmann M, Voigt JP, et al. Intracellular serotonin modulates insulin secretion from pancreatic beta-cells by protein serotonylation. PLoS Biol 2009;7: e1000229.
- Walther DJ, Peter JU, Winter S, et al. Serotonylation of small GTPases is a signal transduction pathway that triggers platelet alpha-granule release. Cell 2003;115: 851–862.
- Watts SW, Priestley JR, Thompson JM. Serotonylation of vascular proteins important to contraction. PLoS One 2009;4:e5682.
- Lobikin M, Wang G, Xu J, et al. Early, nonciliary role for microtubule proteins in left-right patterning is conserved across kingdoms. Proc Natl Acad Sci U S A 2012;109: 12586–12591.
- Levin M, Palmer AR. Left-right patterning from the inside out: Widespread evidence for intracellular control. Bioessays 2007;29:271–287.
- Casey B. Two rights make a wrong: Human left-right malformations. Hum Mol Genet 1998;7:1565–1571.
- Casey B, Hackett BP. Left-right axis malformations in man and mouse. Curr Opin Genet Dev 2000;10:257–261.
- Kosaki K, Casey B. Genetics of human left-right axis malformations. Semin Cell Dev Biol 1998;9:89–99.
- Peeters H, Devriendt K. Human laterality disorders. Eur J Med Genet 2006;49:349–362.
- Beyer T, Danilchik M, Thumberger T, et al. Serotonin signaling is required for Wnt-dependent GRP specification and leftward flow in Xenopus. Curr Biol 2012;22:33–39.
- Garic-Stankovic A, Hernandez M, Flentke GR, et al. A ryanodine receptor-dependent Ca(i)(2+) asymmetry at Hensen’s node mediates avian lateral identity. Develop- ment 2008;135:3271–3280.
- Vandenberg LN, Levin M. Polarity proteins are requie for left-right axis orientation and twin-twin instruction. Genesis 2012;50:219–234.
- Deraet M, Manivet P, Janoshazi A, et al. The natural mu- tation encoding a C terminus-truncated 5-hydroxytryptamine 2B receptor is a gain of proliferative functions. Mol Phar- macol 2005;67:983–991.
- Furrer K, Rickenbacher A, Tian Y, et al. Serotonin reverts age-related capillarization and failure of regeneration in the liver through a VEGF-dependent pathway. Proc Natl Acad Sci U S A 2011;108:2945–2950.
- Gustafsson BI, Thommesen L, Stunes AK, et al. Serotonin and fluoxetine modulate bone cell function in vitro. J Cell Biochem 2006;98:139–151.
- Lee SL, Wang WW, Lanzillo JJ, et al. Serotonin produces both hyperplasia and hypertrophy of bovine pulmonary artery smooth muscle cells in culture. Am J Physiol 1994; 266:L46–L52.
- Lesurtel M, Graf R, Aleil B, et al. Platelet-derived sero- tonin mediates liver regeneration. Science 2006;312:104– 107.
- Sari Y, Zhou FC. Serotonin and its transporter on prolif- eration of fetal heart cells. Int J Dev Neurosci 2003;21: 417–424.
- Colas JF, Launay JM, Maroteaux L. Maternal and zygotic control of serotonin biosynthesis are both necessary for Drosophila germband extension. Mech Dev 1999;87:67– 76.
- Colas JF, Launay JM, Vonesch JL, et al. Serotonin syn- chronises convergent extension of ectoderm with mor- phogenetic gastrulation movements in Drosophila. Mech Dev 1999;87:77–91.
- Moiseiwitsch JR, Lauder JM. Serotonin regulates mouse cranial neural crest migration. Proc Natl Acad Sci U S A 1995;92:7182–7186.
- Schaerlinger B, Launay JM, Vonesch JL, et al. Gain of affinity point mutation in the serotonin receptor gene 5- HT2Dro accelerates germband extension movements during Drosophila gastrulation. Dev Dyn 2007;236:991– 999.
- Cote F, Fligny C, Bayard E, et al. Maternal serotonin is crucial for murine embryonic development. Proc Natl Acad Sci U S A 2007;104:329–334.
- Zhang Y, Benton JL, Beltz BS. 5-HT receptors mediate lineage-dependent effects of serotonin on adult neuro- genesis in Procambarus clarkii. Neural Dev 2011;6:2.
- Nebigil CG, Choi DS, Dierich A, et al. Serotonin 2B re- ceptor is required for heart development. Proc Natl Acad Sci U S A 2000;97:9508–9513.
- De Lucchini S, Ori M, Cremisi F, et al. 5-HT2B-mediated serotonin signaling is required for eye morphogenesis in Xenopus. Mol Cell Neurosci 2005;29:299–312.
- Bhasin N, LaMantia AS, Lauder JM. Opposing regulation of cell proliferation by retinoic acid and the serotonin2B receptor in the mouse frontonasal mass. Anat Embryol (Berl) 2004;208:135–143.
- Lauder JM, Zimmerman EF. Sites of serotonin uptake in epithelia of the developing mouse palate, oral cavity, and face: Possible role in morphogenesis. J Craniofac Genet Dev Biol 1988;8:265–276.
- Moiseiwitsch JR, Lauder JM. Regulation of gene expression in cultured embryonic mouse mandibular mes- enchyme by serotonin antagonists. Anat Embryol (Berl) 1997;195:71–78.
- Adams SV, DeFelice LJ. Flux coupling in the human serotonin transporter. Biophys J 2002;83:3268–3282.
- Hilber B, Scholze P, Dorostkar MM, et al. Serotonin- transporter mediated efflux: A pharmacological analysis of amphetamines and non-amphetamines. Neuropharma- cology 2005;49:811–819.
- Dizeyi N, Bjartell A, Nilsson E, et al. Expression of serotonin receptors and role of serotonin in human prostate cancer tissue and cell lines. Prostate 2004;59:328–336.
- Meredith EJ, Holder MJ, Chamba A, et al. The serotonin transporter (SLC6A4) is present in B-cell clones of di- verse malignant origin: Probing a potential anti-tumor target for psychotropics. FASEB J 2005;19:1187–1189.
- Slominski A, Pisarchik A, Zbytek B, et al. Functional activity of serotoninergic and melatoninergic systems expressed in the skin. J Cell Physiol 2003;196:144–153.
- Slominski A, Wortsman J, Tobin DJ. The cutaneous serotoninergic/melatoninergic system: Securing a place un- der the sun. FASEB J 2005;19:176–194.
- Aldana BI, Sitges M. Sertraline inhibits pre-synaptic Na(+) channel-mediated responses in hippocampus- isolated nerve endings. J Neurochem 2012;121:197–205.
- Chien JM, Chou CT, Pan CC, et al. The mechanism of sertraline-induced [Ca2+]i rise in human OC2 oral cancer cells. Hum Exp Toxicol 2011;30:1635–1643.
- Feuerbach D, Lingenhohl K, Dobbins P, et al. Coupling of human nicotinic acetylcholine receptors alpha 7 to cal- cium channels in GH3 cells. Neuropharmacology 2005; 48:215–227.
- Fonseca-Magalhaes PA, Sousa DF, de Siqueira RJ, et al. Inhibitory effects of sertraline in rat isolated perfused kidneys and in isolated ring preparations of rat arteries. J Pharm Pharmacol 2011;63:1186–1194.
- Fryer JD, Lukas RJ. Antidepressants noncompetitively inhibit nicotinic acetylcholine receptor function. J Neu- rochem 1999;72:1117–1124.
- Huang CJ, Harootunian A, Maher MP, et al. Character- ization of voltage-gated sodium-channel blockers by electrical stimulation and fluorescence detection of membrane potential. Nat Biotechnol 2006;24:439–446.
- Huang CJ, Kuo DH, Chang KH, et al. Effect of the anti- depressant sertraline on Ca2+ fluxes in Madin-Darby ca- nine renal tubular cells. J Recept Signal Transduct Res 2009;29:342–348.
- Kalyoncu NI, Ozyavuz R, Karaoglu S. Sertraline inhibits the contractile responses to noradrenaline, KCl and electrical field stimulation of rat isolated vas deferens. J Auton Pharmacol 1999;19:365–369.
- Kobayashi T, Washiyama K, Ikeda K. Inhibition of G protein-activated inwardly rectifying K+ canne by different classes of antidepressants. PLoS One 2011;6:e28208.
- Lee HA, Kim KS, Hyun SA, et al. Wide spectrum of inhibitory effects of sertraline on cardiac ion channels. Korean J Physiol Pharmacol 2012;16:327–332.
- Maertens C, Droogmans G, Verbesselt R, et al. Block of volume-regulated anion channels by selective serotonin reuptake inhibitors. Naunyn Schmiedebergs Arch Phar- macol 2002;366:158–165.
- Ohno Y, Hibino H, Lossin C, et al. Inhibition of astroglial Kir4.1 channels by selective serotonin reuptake inhibitors. Brain Res 2007;1178:44–51.
- Wang GK, Mitchell J, Wang SY. Block of persistent late Na+ currents by antidepressant sertraline and paroxetine. J Membr Biol 2008;222:79–90.
- Bates E. Ion channels in development and cancer. Annu Rev Cell Dev Biol 2015;31:231–247.
- Levin M, Martyniuk CJ. The bioelectric code: An ancient computational medium for dynamic control of growth and form. Biosystems 2018;164:76–93.
- Hatten ME, Liem RK, Mason CA. Weaver mouse cere- bellar granule neurons fail to migrate on wild-type astro- glial processes in vitro. J Neurosci 1986;6:2676–2683
- Levin M. Bioelectric mechanisms in regeneration: Unique aspects and future perspectives. Semin Cell Dev Biol 2009;20:543–556.
- Levin M. Reprogramming cells and tissue patterning via bioelectrical pathways: Molecular mechanisms and bio- medical opportunities. Wiley Interdiscip Rev Syst Biol Med 2013;5:657–676.
- Levin M, Stevenson CG. Regulation of cell behavior and tissue patterning by bioelectrical signals: Challenges and opportunities for biomedical engineering. Annu Rev Biomed Eng 2012;14:295–323.
- Patil N, Cox DR, Bhat D, et al. A potassium channel mu- tation in weaver mice implicates membrane excitability in granule cell differentiation. Nat Genet 1995;11:126–129.
- Rakic P, Sidman RL. Sequence of developmental abnormalities leading to granule cell deficit in cerebellar cortex of weaver mutant mice. J Comp Neurol 1973;152:103–132.
- Rakic P, Sidman RL. Weaver mutant mouse cerebellum: Defective neuronal migration secondary to abnormality of Bergmann glia. Proc Natl Acad Sci U S A 1973;70:240–244.
- Sundelacruz S, Levin M, Kaplan DL. Role of membrane potential in the regulation of cell proliferation and dif- ferentiation. Stem Cell Rev 2009;5:231–246.
- Tseng A, Levin M. Cracking the bioelectric code: Probing endogenous ionic controls of pattern formation. Commun Integr Biol 2013;6:e22595.
- Teng GQ, Zhao X, Lees-Miller JP, et al. Homozygous missense N629D hERG (KCNH2) potassium channel mutation causes developmental defects in the right ven- tricle and its outflow tract and embryonic lethality. Circ Res 2008;103:1483–1491.
- Bendahhou S, Donaldson MR, Plaster NM, et al. Defective potassium channel Kir2.1 trafficking underlies Andersen-Tawil syndrome. J Biol Chem 2003;278:51779– 51785.
- Dahal GR, Rawson J, Gassaway B, et al. An inwardlyrectifying K+ channel is required for patterning. Devel- opment 2012;139:3653–3664.
- Uzun S, Gokce S, Wagner K. Cystic fibrosis transmem- brane conductance regulator gene mutations in infertile males with congenital bilateral absence of the vas defer- ens. Tohoku J Exp Med 2005;207:279–285.
- Wilschanski M, Dupuis A, Ellis L, et al. Mutations in the cystic fibrosis transmembrane regulator gene and in vivo transepithelial potentials. Am J Respir Crit Care Med 2006;174:787–794.
- Culiat CT, Stubbs LJ, Woychik RP, et al. Deficiency of the beta 3 subunit of the type A gamma-aminobutyric acid receptor causes cleft palate in mice. Nat Genet 1995;11: 344–346.
- Galanopoulou AS. Mutations affecting GABAergic sig- naling in seizures and epilepsy. Pflugers Arch 2010;460: 505–523.
- Lee MP, Ravenel JD, Hu RJ, et al. Targeted disruption of the Kvlqt1 gene causes deafness and gastric hyperplasia in mice. J Clin Invest 2000;106:1447–1455.
- Moore ES, Ward RE, Escobar LF, et al. Heterogeneity in Wiedemann-Beckwith syndrome: Anthropometric evi- dence. Am J Med Genet 2000;90:283–290.
- Weksberg R, Nishikawa J, Caluseriu O, et al. Tumor de- velopment in the Beckwith-Wiedemann syndrome is as sociated with a variety of constitutional molecular 11p15 alterations including imprinting defects of KCNQ1OT1. Hum Mol Genet 2001;10:2989–3000.
- Gloyn AL, Pearson ER, Antcliff JF, et al. Activating mutations in the gene encoding the ATP-sensitive potassium-channel subunit Kir6.2 and permanent neonatal diabetes. N Engl J Med 2004;350:1838–1849.
- Fonager K, Larsen H, Pedersen L, et al. Birth outcomes in women exposed to anticonvulsant drugs. Acta Neurol Scand 2000;101:289–294.
- Pediatric Cardiac Genomics C, Gelb B, Brueckner M, et al. The Congenital Heart Disease Genetic Network Study: Rationale, design, and early results. Circ Res 2013; 112:698–706.
- Aw S, Adams DS, Qiu D, et al. H,K-ATPase protein lo- calization and Kir4.1 function reveal concordance of three axes during early determination of left-right asymmetry. Mech Dev 2008;125:353–372.
- Aw S, Koster JC, Pearson W, et al. The ATP-sensitive K(+)-channel (K(ATP)) controls early left-right patterning in Xenopus and chick embryos. Dev Biol 2010;346:39–53.
- Morokuma J, Blackiston D, Levin M. KCNQ1 and KCNE1 K+ channel components are involved in early left-right patterning in Xenopus laevis embryos. Cell Physiol Biochem 2008;21:357–372.
- Levin M. Molecular bioelectricity in developmental bi- ology: New tools and recent discoveries: Control of cell behavior and pattern formation by transmembrane poten- tial gradients. Bioessays 2012;34:205–217.
- Hernandez-Diaz S, Levin M. Alteration of bioelectrically- controlled processes in the embryo: A teratogenic mecha- nism for anticonvulsants. Reprod Toxicol 2014;47:111–114.
- Berard A, Zhao JP, Sheehy O. Sertraline use during pregnancy and the risk of major malformations. Am J Obstet Gynecol 2015;212:795 e791–e795 e712.
- Diav-Citrin O, Shechtman S, Weinbaum D, et al. Parox- etine and fluoxetine in pregnancy: A prospective, multi- centre, controlled, observational study. Br J Clin Pharmacol 2008;66:695–705.
- Bakker MK, Kerstjens-Frederikse WS, Buys CH, et al. First-trimester use of paroxetine and congenital heart de-fects: A population-based case-control study. Birth De- fects Res A Clin Mol Teratol 2010;88:94–100.
- Martinez-Frias ML, Urioste M, Bermejo E, et al. Primary midline developmental field. II. Clinical/epidemiological analysis of alteration of laterality (normal body symmetry and asymmetry). Am J Med Genet 1995;56:382–388.
- Gebbia M, Ferrero GB, Pilia G, et al. X-linked situs ab- normalities result from mutations in ZIC3. Nat Genet 1997;17:305–308.
- Ticho BS, Goldstein AM, Van Praagh R. Extracardiac anomalies in the heterotaxy syndromes with focus on anomalies of midline-associated structures. Am J Cardiol 2000;85:729–734.
- Morelli SH, Young L, Reid B, et al. Clinical analysis of families with heart, midline, and laterality defects. Am J Med Genet 2001;101:388–392.
- Bisgrove BW, Morelli SH, Yost HJ. Genetics of human laterality disorders: Insights from vertebrate model sys- tems. Annu Rev Genomics Hum Genet 2003;4:1–32.
- Ramsdell AF. Left-right asymmetry and congenital cardiac defects: Getting to the heart of the matter in vertebrate left- right axis determination. Dev Biol 2005;288:1–20.
- Ramsdell AF, Bernanke JM, Trusk TC. Left-right lineage analysis of the embryonic Xenopus heart reveals a novel framework linking congenital cardiac defects and later- ality disease. Development 2006;133:1399–1410.
- Bamforth SD, Braganca J, Farthing CR, et al. Cited2 controls left-right patterning and heart development through a Nodal-Pitx2c pathway. Nat Genet 2004;36: 1189–1196.
- Ware SM, Peng J, Zhu L, et al. Identification and func- tional analysis of ZIC3 mutations in heterotaxy and re- lated congenital heart defects. Am J Hum Genet 2004;74: 93–105.
- Levin M. Left-right asymmetry in embryonic development: A comprehensive review. Mech Dev 2005;122:3–25.
- Takaoka K, Yamamoto M, Hamada H. Origin of body axes in the mouse embryo. Curr Opin Genet Dev 2007;17: 344–350.
- Aw S, Levin M. Is left-right asymmetry a form of planar cell polarity? Development 2009;136:355–366.
- Cooper WO, Willy ME, Pont SJ, et al. Increasing use of antidepressants in pregnancy. Am J Obstet Gynecol 2007; 196:544 e541–e545.
- Jimenez-Solem E, Andersen JT, Petersen M, et al. Prevalence of antidepressant use during pregnancy in Den- mark, a nation-wide cohort study. PLoS One 2013;8: e63034.
- Huybrechts KF, Palmsten K, Avorn J, et al. Antidepressant use in pregnancy and the risk of cardiac de- fects. N Engl J Med 2014;370:2397–2407.
- Margulis AV, Abou-Ali A, Strazzeri MM, et al. Use of selective serotonin reuptake inhibitors in pregnancy and cardiac malformations: A propensity-score matched co- hort in CPRD. Pharmacoepidemiol Drug Saf 2013;22: 942–951.
- Berard A. Paroxetine exposure during pregnancy and the risk of cardiac malformations: What is the evidence? Birth Defects Res A Clin Mol Teratol 2010;88:171–174.
- Berard A, Chaabane S, Boukhris T. Antidepressant use in pregnancy and the risk of cardiac defects. N Engl J Med 2014;371:1167–1168.
- FDA advising of risk of birth defects with Paxil. News release of the Food and Drug Administration, December 8, 2005www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ 2005/ucm108527.htm (last accessed June 15, 2018).
- Yazdy MM, Mitchell AA, Louik C, et al. Use of selective serotonin-reuptake inhibitors during pregnancy and the risk of clubfoot. Epidemiology 2014;25:859–865.
- Chambers CD, Hernandez-Diaz S, Van Marter LJ, et al. Selective serotonin-reuptake inhibitors and risk of per- sistent pulmonary hypertension of the newborn. N Engl J Med 2006;354:579–587.
- Kallen B, Olausson PO. Maternal use of selective serotonin re-uptake inhibitors and persistent pulmonary hy- pertension of the newborn. Pharmacoepidemiol Drug Saf 2008;17:801–806.
- Kieler H, Artama M, Engeland A, et al. Selective sero- tonin reuptake inhibitors during pregnancy and risk of persistent pulmonary hypertension in the newborn: Po- pulation based cohort study from the five Nordic coun- tries. BMJ 2012;344:d8012.
- Berard A, Sheehy O, Zhao JP, et al. SSRI and SNRI use during pregnancy and the risk of persistent pulmonary hypertension of the newborn. Br J Clin Pharmacol 2017; 83:1126–1133.
- Broy P, Berard A. Gestational exposure to antidepressants nd the risk of spontaneous abortion: A review. Curr Drug Deliv 2010;7:76–92.
- Coverdale JH, McCullough LB, Chervenak FA. The eth- ics of randomized placebo-controlled trials of antide- pressants with pregnant women: A systematic review. Obstet Gynecol 2008;112:1361–1368.
- Gavin NI, Gaynes BN, Lohr KN, et al. Perinatal depres- sion: A systematic review of prevalence and incidence. Obstet Gynecol 2005;106:1071–1083.
- Wisner KL, Sit DK, Hanusa BH, et al. Major depression and antidepressant treatment: Impact on pregnancy and neonatal outcomes. Am J Psychiatry 2009;166:557–566.
- Cohen LS, Altshuler LL, Harlow BL, et al. Relapse of major depression during pregnancy in women who maintain or discontinue antidepressant treatment. JAMA 2006;295:499–507.
- Nulman I, Koren G, Rovet J, et al. Neurodevelopment of children following prenatal exposure to venlafaxine, se- lective serotonin reuptake inhibitors, or untreated maternal depression. Am J Psychiatry 2012;169:1165–1174.
- Honein MA, Rasmussen SA, Reefhuis J, et al. Maternal smoking and environmental tobacco smoke exposure and the risk of orofacial clefts. Epidemiology 2007;18:226– 233.
- Jones KL. The effects of alcohol on fetal development.Birth Defects Res C Embryo Today 2011;93:3–11.
- Czeizel AE, Dudas I. Prevention of the first occurrence of neural-tube defects by periconceptional vitamin supple- mentation. N Engl J Med 1992;327:1832–1835.
- Toohey J. Depression during pregnancy and postpartum. Clin Obstet Gynecol 2012;55:788–797.
- Dubber S, Reck C, Muller M, et al. Postpartum bonding: The role of perinatal depression, anxiety and maternal- fetal bonding during pregnancy. Arch Womens Ment Health 2015;18:187–195.
- Dunn AL, Trivedi MH, Kampert JB, et al. Exercise treatment for depression: Efficacy and dose response. Am J Prev Med 2005;28:1–8.
- Stuart S, Koleva H. Psychological treatments for perinatal depression. Best Pract Res Clin Obstet Gynaecol 2014;28: 61–70.
- Stone MB, Jones L (2006). Clinical review: Relationship between antidepressant drugs and suicidality in adults. https://baumhedlundlaw.com/pdf/dolin-trial-exhibits/JX-13- Clinical-Review-Relationship-Between-Antidepressant- Drugs-and-Suicidality-in-Adults.pdf (last accessed June 15, 2018).
- Miniati M, Callari A, Calugi S, et al. Interpersonal psy- chotherapy for postpartum depression: A systematic re- view. Arch Womens Ment Health 2014;17:257–268.
- Antenatal and postnatal mental health: clinical management and service guidance NICE clinical guideline 192. www.nice.org.uk/guidance/cg45 (last accessed June 15, 2018).
- Hill AB. The environment and disease: Association or causation? Proc R Soc Med 1965;58:295–300.
- Levin M, Palmer AR. Left-right patterning from the inside out: Widespread evidence for intracellular control. Bioessays 2007;29:271–287.Casey B. Two rights make a wrong: Human left-rightmalformations. Hum Mol Genet 1998;7:1565–1571.
- Casey B, Hackett BP. Left-right axis malformations in man and mouse. Curr Opin Genet Dev 2000;10:257–261.
- Kosaki K, Casey B. Genetics of human left-right axis malformations. Semin Cell Dev Biol 1998;9:89–99.
- Peeters H, Devriendt K. Human laterality disorders. Eur J Med Genet 2006;49:349–362.
- Beyer T, Danilchik M, Thumberger T, et al. Serotoninsignaling is required for Wnt-dependent GRP specification and leftward flow in Xenopus. Curr Biol 2012;22:33–39.
- Garic-Stankovic A, Hernandez M, Flentke GR, et al. A ryanodine receptor-dependent Ca(i)(2+) asymmetry at Hensen’s node mediates avian lateral identity. Develop- ment 2008;135:3271–3280.
- Vandenberg LN, Levin M. Polarity proteins are required
- for left-right axis orientation and twin-twin instruction. Genesis 2012;50:219–234.
- Deraet M, Manivet P, Janoshazi A, et al. The natural mu- tation encoding a C terminus-truncated 5-hydroxytryptamine 2B receptor is a gain of proliferative functions. Mol Phar- macol 2005;67:983–991.
- Furrer K, Rickenbacher A, Tian Y, et al. Serotonin reverts age-related capillarization and failure of regeneration in the liver through a VEGF-dependent pathway. Proc Natl Acad Sci U S A 2011;108:2945–2950.
- Gustafsson BI, Thommesen L, Stunes AK, et al. Serotonin and fluoxetine modulate bone cell function in vitro. J Cell Biochem 2006;98:139–151.
- Lee SL, Wang WW, Lanzillo JJ, et al. Serotonin produces both hyperplasia and hypertrophy of bovine pulmonary artery smooth muscle cells in culture. Am J Physiol 1994; 266:L46–L52.
- Lesurtel M, Graf R, Aleil B, et al. Platelet-derived sero- tonin mediates liver regeneration. Science 2006;312:104– 107.
- Sari Y, Zhou FC. Serotonin and its transporter on prolif- eration of fetal heart cells. Int J Dev Neurosci 2003;21: 417–424.
- Colas JF, Launay JM, Maroteaux L. Maternal and zygotic control of serotonin biosynthesis are both necessary for Drosophila germband extension. Mech Dev 1999;87:67– 76.
- Colas JF, Launay JM, Vonesch JL, et al. Serotonin syn- chronises convergent extension of ectoderm with mor- phogenetic gastrulation movements in Drosophila. Mech Dev 1999;87:77–91.
- Moiseiwitsch JR, Lauder JM. Serotonin regulates mouse cranial neural crest migration. Proc Natl Acad Sci U S A 1995;92:7182–7186.
- Schaerlinger B, Launay JM, Vonesch JL, et al. Gain of affinity point mutation in the Cote F,serotonin receptor gene 5- HT2Dro accelerates germband extension movements during Drosophila gastrulation. Dev Dyn 2007;236:991– 999.
- Cote F, Fligny C, Bayard E, et al. Maternal serotonin is crucial for murine embryonic development. Proc Natl Acad Sci U S A 2007;104:329–334.
- Zhang Y, Benton JL, Beltz BS. 5-HT receptors mediatelineage-dependent effects of serotonin on adult neuro- genesis in Procambarus clarkii. Neural Dev 2011;6:2.
Corrispondenza al Anick Be´rard, PhD Faculty of Pharmacy University of Montreal Research Center CHU Sainte-Justine 3175 Coˆ te-Sainte-Catherine Montreal, Quebec, H3T 1C5 Canada Email: anick.berard@umontreal.ca



